题目
“碳达峰•碳中和”是我国社会发展重大战略之一,CH4还原CO2是实现“双碳”经济的有效途径之一,相关的主要反应有:Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)ΔH1=+247kJ•mol-1,K1Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH2=+41kJ•mol-1,K2请回答:(1)有利于提高CO2平衡转化率的条件是 ____ 。A.低温低压B.低温高压C.高温低压D.高温高压(2)反应CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g)的ΔH= ____ kJ•mol-1,K= ____ (用K1,K2表示)。(3)恒压、750℃时,CH4和CO2按物质的量之比1:3投料,反应经如图流程(主要产物已标出)可实现CO2高效转化。(H)_(4)+C(O)_(2) (O)_(3) He-|||-Fe-|||-i ii ii-|||-CaO +(H)_(e)-|||-+(H)_(2) +C(O)_(2) Fe3O4 H2O①下列说法正确的是 ____ 。A.Fe3O4可循环利用,CaO不可循环利用B.过程ii,CaO吸收CO2可促使Fe3O4氧化CO的平衡正移C.过程ii产生的H2O最终未被CaO吸收,在过程ii被排出D.相比于反应Ⅰ,该流程的总反应还原1molCO2需吸收的能量更多②过程ii平衡后通入He,测得一段时间内CO物质的量上升,根据过程iii,结合平衡移动原理,解释CO物质的量上升的原因 ____ 。(4)CH4还原能力(R)可衡量CO2转化效率,R=(Δn(CO_(2)))/(Δn(CH_(4)))(同一时段内CO2与CH4的物质的量变化量之比)。①常压下CH4和CO2按物质的量之比1:3投料,某一时段内CH4和CO2的转化率随温度变化如图1,请在图2中画出400~1000℃之间R的变化趋势,并标明1000℃时R值。(H)_(4)+C(O)_(2) (O)_(3) He-|||-Fe-|||-i ii ii-|||-CaO +(H)_(e)-|||-+(H)_(2) +C(O)_(2) Fe3O4 H2O②催化剂X可提高R值,另一时段内CH4转化率、R值随温度变化如下表: 温度/℃ 480 500 520 550 CH4转化率/% 7.9 11.5 20.2 34.8 R 2.6 2.4 2.1 1.8 下列说法不正确的是 ____ 。A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率B.温度越低,含氢产物中H2O占比越高C.温度升高,CH4转化率增加,CO2转化率降低,R值减小D.改变催化剂提高CH4转化率,R值不一定增大
“碳达峰•碳中和”是我国社会发展重大战略之一,CH4还原CO2是实现“双碳”经济的有效途径之一,相关的主要反应有:
Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)ΔH1=+247kJ•mol-1,K1
Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH2=+41kJ•mol-1,K2
请回答:
(1)有利于提高CO2平衡转化率的条件是 ____ 。
A.低温低压
B.低温高压
C.高温低压
D.高温高压
(2)反应CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g)的ΔH= ____ kJ•mol-1,K= ____ (用K1,K2表示)。
(3)恒压、750℃时,CH4和CO2按物质的量之比1:3投料,反应经如图流程(主要产物已标出)可实现CO2高效转化。
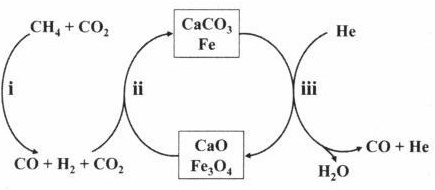
①下列说法正确的是 ____ 。
A.Fe3O4可循环利用,CaO不可循环利用
B.过程ii,CaO吸收CO2可促使Fe3O4氧化CO的平衡正移
C.过程ii产生的H2O最终未被CaO吸收,在过程ii被排出
D.相比于反应Ⅰ,该流程的总反应还原1molCO2需吸收的能量更多
②过程ii平衡后通入He,测得一段时间内CO物质的量上升,根据过程iii,结合平衡移动原理,解释CO物质的量上升的原因 ____ 。
(4)CH4还原能力(R)可衡量CO2转化效率,R=$\frac{Δn(CO_{2})}{Δn(CH_{4})}$(同一时段内CO2与CH4的物质的量变化量之比)。
①常压下CH4和CO2按物质的量之比1:3投料,某一时段内CH4和CO2的转化率随温度变化如图1,请在图2中画出400~1000℃之间R的变化趋势,并标明1000℃时R值。
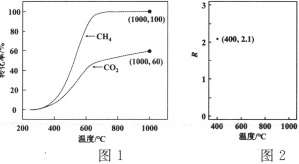
②催化剂X可提高R值,另一时段内CH4转化率、R值随温度变化如下表:
下列说法不正确的是 ____ 。
A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中H2O占比越高
C.温度升高,CH4转化率增加,CO2转化率降低,R值减小
D.改变催化剂提高CH4转化率,R值不一定增大
Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)ΔH1=+247kJ•mol-1,K1
Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH2=+41kJ•mol-1,K2
请回答:
(1)有利于提高CO2平衡转化率的条件是 ____ 。
A.低温低压
B.低温高压
C.高温低压
D.高温高压
(2)反应CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g)的ΔH= ____ kJ•mol-1,K= ____ (用K1,K2表示)。
(3)恒压、750℃时,CH4和CO2按物质的量之比1:3投料,反应经如图流程(主要产物已标出)可实现CO2高效转化。

①下列说法正确的是 ____ 。
A.Fe3O4可循环利用,CaO不可循环利用
B.过程ii,CaO吸收CO2可促使Fe3O4氧化CO的平衡正移
C.过程ii产生的H2O最终未被CaO吸收,在过程ii被排出
D.相比于反应Ⅰ,该流程的总反应还原1molCO2需吸收的能量更多
②过程ii平衡后通入He,测得一段时间内CO物质的量上升,根据过程iii,结合平衡移动原理,解释CO物质的量上升的原因 ____ 。
(4)CH4还原能力(R)可衡量CO2转化效率,R=$\frac{Δn(CO_{2})}{Δn(CH_{4})}$(同一时段内CO2与CH4的物质的量变化量之比)。
①常压下CH4和CO2按物质的量之比1:3投料,某一时段内CH4和CO2的转化率随温度变化如图1,请在图2中画出400~1000℃之间R的变化趋势,并标明1000℃时R值。

②催化剂X可提高R值,另一时段内CH4转化率、R值随温度变化如下表:
| 温度/℃ | 480 | 500 | 520 | 550 |
| CH4转化率/% | 7.9 | 11.5 | 20.2 | 34.8 |
| R | 2.6 | 2.4 | 2.1 | 1.8 |
A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中H2O占比越高
C.温度升高,CH4转化率增加,CO2转化率降低,R值减小
D.改变催化剂提高CH4转化率,R值不一定增大
题目解答
答案
解:(1)反应Ⅰ是一个反应前后气体条件增大的吸热反应、反应Ⅱ是一个反应前后气体体积不变的吸热反应,升高温度、减小压强有利于反应Ⅰ平衡正向移动,所以要提高CO2的转化率,应该选取高温、低压条件,
故答案为:C;
(2)Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)ΔH1=+247kJ•mol-1,K1=$\frac{{c}^{2}(CO)•{c}^{2}({H}_{2})}{c(C{H}_{4})•c(C{O}_{2})}$;Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH2=+41kJ•mol-1,K2=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$;将反应Ⅰ+2Ⅱ得反应CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g)ΔH=△H1+2△H2=[(+247)+2×(+41)]kJ/mol=+329kJ/mol,K=$\frac{{c}^{4}(CO)•{c}^{2}({H}_{2}O)}{c(C{H}_{4})•{c}^{3}(C{O}_{2})}$=$\frac{{c}^{2}(CO)•{c}^{2}({H}_{2})}{c(C{H}_{4})•c(C{O}_{2})}$×($\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$)2=K1•K22,
故答案为:+329;K1•K22;
(3)①A.根据图知,Fe3O4、CaO在过程ii中作反应物、过程iii中作生成物,所以CaO、Fe3O4可循环利用,故A错误;
B.过程ii,CO2和CaO反应生成CaCO3,导致c(CO2)降低,可促使Fe3O4氧化CO的平衡正移,故B正确;
C.过程ii中CaO吸收CO2而产生的H2O最终未被CaO吸收,所以H2O在过程ii被排出,故C正确;
D.焓变只与反应物和生成物的总能量差有关,与反应过程无关,所以相比于反应Ⅰ,该流程的总反应还原1molCO2需吸收的能量一样多,故D错误;
故答案为:BC;
②通入He,恒压条件下,CaCO3分解压强减小,CaCO3分解平衡正移,导致$\frac{c(C{O}_{2})}{c(CO)}$增大,促进Fe还原CO2平衡正移,CO物质的量上升,
故答案为:通入He,CaCO3分解平衡正移,导致$\frac{c(C{O}_{2})}{c(CO)}$增大,促进Fe还原CO2平衡正移;
(4)①根据图1知,1000℃时CH4的转化率为100%,则△n(CH4)=1mol,CO2的转化率为60%,△n(CO2)=3mol×60%=1.8mol,R=$\frac{Δn(CO_{2})}{Δn(CH_{4})}$=$\frac{1.8mol}{1mol}$=1.8,所以400~1000℃之间R的变化趋势如图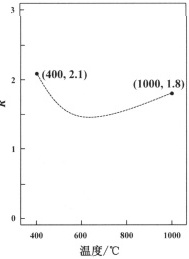 ,
,
故答案为: ;
;
②A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率,使单位时间内反应Ⅱ中CO2的转化率增大,△n(CO2)增大的倍数大于△n(CH4)增大的倍数,所以R提高,故A正确;
B.根据表知,温度越低,CH4的转化率越低,R越大,△n(CO2)增大的倍数比△n(CH4)大,根据氢原子守恒知,含氢产物中H2O占比越高,故B正确;
C.两个反应都是吸热反应,温度升高,CH4转化率增加,CO2转化率增大,两个反应中CO2转化率都增大,增大倍数多,则R值增大,故C错误;
D.改变催化剂使反应有选择性按反应Ⅰ而提高CH4转化率,如果CO2转化率减小,R值不一定增大,故D正确;
故答案为:C。
故答案为:C;
(2)Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)ΔH1=+247kJ•mol-1,K1=$\frac{{c}^{2}(CO)•{c}^{2}({H}_{2})}{c(C{H}_{4})•c(C{O}_{2})}$;Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH2=+41kJ•mol-1,K2=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$;将反应Ⅰ+2Ⅱ得反应CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g)ΔH=△H1+2△H2=[(+247)+2×(+41)]kJ/mol=+329kJ/mol,K=$\frac{{c}^{4}(CO)•{c}^{2}({H}_{2}O)}{c(C{H}_{4})•{c}^{3}(C{O}_{2})}$=$\frac{{c}^{2}(CO)•{c}^{2}({H}_{2})}{c(C{H}_{4})•c(C{O}_{2})}$×($\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$)2=K1•K22,
故答案为:+329;K1•K22;
(3)①A.根据图知,Fe3O4、CaO在过程ii中作反应物、过程iii中作生成物,所以CaO、Fe3O4可循环利用,故A错误;
B.过程ii,CO2和CaO反应生成CaCO3,导致c(CO2)降低,可促使Fe3O4氧化CO的平衡正移,故B正确;
C.过程ii中CaO吸收CO2而产生的H2O最终未被CaO吸收,所以H2O在过程ii被排出,故C正确;
D.焓变只与反应物和生成物的总能量差有关,与反应过程无关,所以相比于反应Ⅰ,该流程的总反应还原1molCO2需吸收的能量一样多,故D错误;
故答案为:BC;
②通入He,恒压条件下,CaCO3分解压强减小,CaCO3分解平衡正移,导致$\frac{c(C{O}_{2})}{c(CO)}$增大,促进Fe还原CO2平衡正移,CO物质的量上升,
故答案为:通入He,CaCO3分解平衡正移,导致$\frac{c(C{O}_{2})}{c(CO)}$增大,促进Fe还原CO2平衡正移;
(4)①根据图1知,1000℃时CH4的转化率为100%,则△n(CH4)=1mol,CO2的转化率为60%,△n(CO2)=3mol×60%=1.8mol,R=$\frac{Δn(CO_{2})}{Δn(CH_{4})}$=$\frac{1.8mol}{1mol}$=1.8,所以400~1000℃之间R的变化趋势如图
 ,
,故答案为:
 ;
;②A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率,使单位时间内反应Ⅱ中CO2的转化率增大,△n(CO2)增大的倍数大于△n(CH4)增大的倍数,所以R提高,故A正确;
B.根据表知,温度越低,CH4的转化率越低,R越大,△n(CO2)增大的倍数比△n(CH4)大,根据氢原子守恒知,含氢产物中H2O占比越高,故B正确;
C.两个反应都是吸热反应,温度升高,CH4转化率增加,CO2转化率增大,两个反应中CO2转化率都增大,增大倍数多,则R值增大,故C错误;
D.改变催化剂使反应有选择性按反应Ⅰ而提高CH4转化率,如果CO2转化率减小,R值不一定增大,故D正确;
故答案为:C。