题目
16.某催化氧化还原反应的机理被认为是-|||-^3++(Cu)^2+=!=!= (V)^4++(Cu)^+ (慢反应)-|||-^++(Fe)^3+=!=!= (Fe)^2++(Cu)^2+ (快反应)-|||-可知该反应的催化剂是-|||-(A) ^3+ (B) ^2+ (C) ^+ (D) ^3+

题目解答
答案
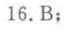
解析
步骤 1:分析反应机理
在给出的反应机理中,有两个反应步骤。第一个反应是慢反应,第二个反应是快反应。催化剂是参与反应但最终不被消耗的物质,因此我们需要找出在反应前后没有被消耗的物质。
步骤 2:确定催化剂
在第一个反应中,${V}^{3+}$ 被氧化成 ${V}^{4+}$,${Cu}^{2+}$ 被还原成 ${Cu}^{+}$。在第二个反应中,${Cu}^{+}$ 被氧化成 ${Cu}^{2+}$,${Fe}^{3+}$ 被还原成 ${Fe}^{2+}$。因此,${Cu}^{2+}$ 在反应前后没有被消耗,它在第一个反应中被还原成 ${Cu}^{+}$,在第二个反应中又被氧化回 ${Cu}^{2+}$,所以 ${Cu}^{2+}$ 是催化剂。
在给出的反应机理中,有两个反应步骤。第一个反应是慢反应,第二个反应是快反应。催化剂是参与反应但最终不被消耗的物质,因此我们需要找出在反应前后没有被消耗的物质。
步骤 2:确定催化剂
在第一个反应中,${V}^{3+}$ 被氧化成 ${V}^{4+}$,${Cu}^{2+}$ 被还原成 ${Cu}^{+}$。在第二个反应中,${Cu}^{+}$ 被氧化成 ${Cu}^{2+}$,${Fe}^{3+}$ 被还原成 ${Fe}^{2+}$。因此,${Cu}^{2+}$ 在反应前后没有被消耗,它在第一个反应中被还原成 ${Cu}^{+}$,在第二个反应中又被氧化回 ${Cu}^{2+}$,所以 ${Cu}^{2+}$ 是催化剂。