题目
氧化钴(Co2O3)粉体材料在工业、电子、电讯等领域都有着广阔的应用前景。以铜钴矿石(主要成分为CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,还有少量Fe2O3、MgO和CaO等)为原料制备氧化钴(Co2O3)的工艺流程如图所示:过量稀H2SO4-|||-和过量Na2SO3 NaClO-|||-铜钴 浸泡 → 除铜 滤液 和Na2CO3 滤液 足量NaF 滤液 浓Na2CO2 滤渣 盐酸,溶液-|||-即石 一 五 面 CoCO-|||-滤渣1 滤渣2 滤渣3 (NH4)2C2O IV-|||-Co2O CoC2O4·2H2O已知:常温下Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36,Ksp(CaF2)=5.3×10-9,Ksp(MgF2)=5.2×10-11。回答下列问题:(1)“浸泡”过程中,为提高浸出速率,可采取的措施有 ____ (填序号)。a.升高温度 b.粉碎矿石 c.通入空气进行搅拌 d.提高稀硫酸浓度(2)“浸泡”过程中,所得滤渣1中的物质是 ____ ,步骤I中NaClO3的作用是 ____ 。(3)“除铜”过程中,加入FeS固体得到更难溶的CuS,计算常温下该“除铜”反应的平衡常数K= ____ 。(4)过程Ⅲ中加入浓Na2CO3得到滤渣后又加入盐酸溶解,其目的是 ____ 。(5)CoC2O4•2H2O在空气中加热煅烧得到Co2O3的化学方程式是 ____ 。实验表明,CoC2O4•2H2O固体在空气中受热分解所得产物(CoC2O4、Co3O4、Co2O3、CoO)会因受热温度变化而不同,具体来说,一定质量的CoC2O4•2H2O固体受热温度越高,煅烧产物质量越小。已知以下四组温度可分别获得一种产物,请选择出该工艺中制备氧化钴(Co2O3)的煅烧温度 ____ (填序号)。a.250-300℃b.550-650℃c.780-820℃d.910-950℃
氧化钴(Co2O3)粉体材料在工业、电子、电讯等领域都有着广阔的应用前景。以铜钴矿石(主要成分为CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,还有少量Fe2O3、MgO和CaO等)为原料制备氧化钴(Co2O3)的工艺流程如图所示:
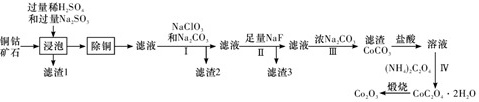
已知:常温下Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36,Ksp(CaF2)=5.3×10-9,Ksp(MgF2)=5.2×10-11。
回答下列问题:
(1)“浸泡”过程中,为提高浸出速率,可采取的措施有 ____ (填序号)。
a.升高温度 b.粉碎矿石 c.通入空气进行搅拌 d.提高稀硫酸浓度
(2)“浸泡”过程中,所得滤渣1中的物质是 ____ ,步骤I中NaClO3的作用是 ____ 。
(3)“除铜”过程中,加入FeS固体得到更难溶的CuS,计算常温下该“除铜”反应的平衡常数K= ____ 。
(4)过程Ⅲ中加入浓Na2CO3得到滤渣后又加入盐酸溶解,其目的是 ____ 。
(5)CoC2O4•2H2O在空气中加热煅烧得到Co2O3的化学方程式是 ____ 。实验表明,CoC2O4•2H2O固体在空气中受热分解所得产物(CoC2O4、Co3O4、Co2O3、CoO)会因受热温度变化而不同,具体来说,一定质量的CoC2O4•2H2O固体受热温度越高,煅烧产物质量越小。已知以下四组温度可分别获得一种产物,请选择出该工艺中制备氧化钴(Co2O3)的煅烧温度 ____ (填序号)。
a.250-300℃
b.550-650℃
c.780-820℃
d.910-950℃

已知:常温下Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36,Ksp(CaF2)=5.3×10-9,Ksp(MgF2)=5.2×10-11。
回答下列问题:
(1)“浸泡”过程中,为提高浸出速率,可采取的措施有 ____ (填序号)。
a.升高温度 b.粉碎矿石 c.通入空气进行搅拌 d.提高稀硫酸浓度
(2)“浸泡”过程中,所得滤渣1中的物质是 ____ ,步骤I中NaClO3的作用是 ____ 。
(3)“除铜”过程中,加入FeS固体得到更难溶的CuS,计算常温下该“除铜”反应的平衡常数K= ____ 。
(4)过程Ⅲ中加入浓Na2CO3得到滤渣后又加入盐酸溶解,其目的是 ____ 。
(5)CoC2O4•2H2O在空气中加热煅烧得到Co2O3的化学方程式是 ____ 。实验表明,CoC2O4•2H2O固体在空气中受热分解所得产物(CoC2O4、Co3O4、Co2O3、CoO)会因受热温度变化而不同,具体来说,一定质量的CoC2O4•2H2O固体受热温度越高,煅烧产物质量越小。已知以下四组温度可分别获得一种产物,请选择出该工艺中制备氧化钴(Co2O3)的煅烧温度 ____ (填序号)。
a.250-300℃
b.550-650℃
c.780-820℃
d.910-950℃
题目解答
答案
解:(1)“浸泡”过程中可以加快反应速率和提高原料利用率的方法是升温、粉碎矿石、适当增加稀硫酸浓度,
故答案为:abd;
(2)结合分析可知,“浸泡”过程中,所得滤渣1中的物质是SiO2、CaSO4,沉铜后加入NaClO3将Fe2+氧化为Fe3+,加入Na2CO3调pH,可以使Fe3+沉淀,
故答案为:SiO2、CaSO4;将Fe2+氧化为Fe3+,使Fe3+沉淀;
(3)“除铜”过程中的反应为Cu2++FeS=CuS+Fe2+,该反应的平衡常数为$\frac{c(Fe{}^{2+})}{c(Cu{}^{2+})}$=$\frac{c(Fe{}^{2+})}{c(Cu{}^{2+})}$×$\frac{c(S{}^{2-})}{c(S{}^{2-})}$=$\frac{K{}_{sp}(FeS)}{K{}_{sp}(CuS)}$=1.0×1018,
故答案为:1.0×1018;
(4)过程Ⅲ中加入浓Na2CO3得到滤渣后又加入盐酸溶解,其目的是富集Co2+,
故答案为:富集Co2+;
(5)由题中可知CoC2O4•2H2O在空气中高温煅烧得到Co2O3,CoC2O4中Co的化合价为+2价,生成Co2O3(Co的化合价为+3价),化合价升高,说明空气中的O2作为氧化剂参与了反应,而C2O42-具有一定还原性也被O2氧化成CO2,故产物分别为Co2O3和CO2,根据元素守恒,可推测出产物中还有H2O生成,再根据电子守恒和原子守恒法,最终可得知反应方程式为4CoC2O4•2H2O+3O2$\frac{\underline{\;高温\;}}{\;}$2Co2O3+8CO2+8H2O,根据元素守恒可知,煅烧温度越高,物质含有的氧元素越少,对应的分解物质分别为CoC2O4、Co2O3、Co3O4、CoO,故应选择b,
故答案为:4CoC2O4•2H2O+3O2$\frac{\underline{\;高温\;}}{\;}$2Co2O3+8CO2+8H2O;b。
故答案为:abd;
(2)结合分析可知,“浸泡”过程中,所得滤渣1中的物质是SiO2、CaSO4,沉铜后加入NaClO3将Fe2+氧化为Fe3+,加入Na2CO3调pH,可以使Fe3+沉淀,
故答案为:SiO2、CaSO4;将Fe2+氧化为Fe3+,使Fe3+沉淀;
(3)“除铜”过程中的反应为Cu2++FeS=CuS+Fe2+,该反应的平衡常数为$\frac{c(Fe{}^{2+})}{c(Cu{}^{2+})}$=$\frac{c(Fe{}^{2+})}{c(Cu{}^{2+})}$×$\frac{c(S{}^{2-})}{c(S{}^{2-})}$=$\frac{K{}_{sp}(FeS)}{K{}_{sp}(CuS)}$=1.0×1018,
故答案为:1.0×1018;
(4)过程Ⅲ中加入浓Na2CO3得到滤渣后又加入盐酸溶解,其目的是富集Co2+,
故答案为:富集Co2+;
(5)由题中可知CoC2O4•2H2O在空气中高温煅烧得到Co2O3,CoC2O4中Co的化合价为+2价,生成Co2O3(Co的化合价为+3价),化合价升高,说明空气中的O2作为氧化剂参与了反应,而C2O42-具有一定还原性也被O2氧化成CO2,故产物分别为Co2O3和CO2,根据元素守恒,可推测出产物中还有H2O生成,再根据电子守恒和原子守恒法,最终可得知反应方程式为4CoC2O4•2H2O+3O2$\frac{\underline{\;高温\;}}{\;}$2Co2O3+8CO2+8H2O,根据元素守恒可知,煅烧温度越高,物质含有的氧元素越少,对应的分解物质分别为CoC2O4、Co2O3、Co3O4、CoO,故应选择b,
故答案为:4CoC2O4•2H2O+3O2$\frac{\underline{\;高温\;}}{\;}$2Co2O3+8CO2+8H2O;b。