题目
挥发性液体A和B可形成理想液态混合物。某温度时溶液上方的蒸气总压为 .41times (10)^4Pa 气、液两相-|||-中A的摩尔分数分别为0.45和0.65。求此温度下纯A和纯B的饱和蒸气压。

题目解答
答案
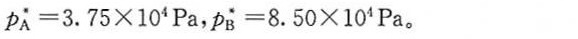
解析
步骤 1:确定理想液态混合物的蒸气压公式
理想液态混合物的蒸气压公式为:${P}_{总}={P}_{A}+{P}_{B}={P}_{A}'{x}_{A}+{P}_{B}'{x}_{B}$,其中${P}_{A}'$和${P}_{B}'$分别为纯A和纯B的饱和蒸气压,${x}_{A}$和${x}_{B}$分别为A和B在液相中的摩尔分数。
步骤 2:根据题目条件列出方程
题目给出的条件是:${P}_{总}=5.41\times {10}^{4}Pa$,${x}_{A}=0.65$,${x}_{B}=1-{x}_{A}=0.35$,${y}_{A}=0.45$,${y}_{B}=1-{y}_{A}=0.55$。根据理想液态混合物的蒸气压公式,可以列出方程:$5.41\times {10}^{4}Pa={P}_{A}'\times 0.65+{P}_{B}'\times 0.35$。
步骤 3:利用拉乌尔定律计算纯A和纯B的饱和蒸气压
拉乌尔定律指出,对于理想液态混合物,气相中各组分的分压与其在液相中的摩尔分数成正比,即${P}_{A}={P}_{A}'{x}_{A}$,${P}_{B}={P}_{B}'{x}_{B}$。根据题目条件,可以列出方程:${P}_{A}={P}_{A}'\times 0.65$,${P}_{B}={P}_{B}'\times 0.35$。由于${y}_{A}=\frac{{P}_{A}}{{P}_{总}}$,${y}_{B}=\frac{{P}_{B}}{{P}_{总}}$,可以得到${P}_{A}={P}_{总}\times {y}_{A}=5.41\times {10}^{4}Pa\times 0.45$,${P}_{B}={P}_{总}\times {y}_{B}=5.41\times {10}^{4}Pa\times 0.55$。将${P}_{A}$和${P}_{B}$的值代入拉乌尔定律的方程中,可以解出${P}_{A}'$和${P}_{B}'$的值。
理想液态混合物的蒸气压公式为:${P}_{总}={P}_{A}+{P}_{B}={P}_{A}'{x}_{A}+{P}_{B}'{x}_{B}$,其中${P}_{A}'$和${P}_{B}'$分别为纯A和纯B的饱和蒸气压,${x}_{A}$和${x}_{B}$分别为A和B在液相中的摩尔分数。
步骤 2:根据题目条件列出方程
题目给出的条件是:${P}_{总}=5.41\times {10}^{4}Pa$,${x}_{A}=0.65$,${x}_{B}=1-{x}_{A}=0.35$,${y}_{A}=0.45$,${y}_{B}=1-{y}_{A}=0.55$。根据理想液态混合物的蒸气压公式,可以列出方程:$5.41\times {10}^{4}Pa={P}_{A}'\times 0.65+{P}_{B}'\times 0.35$。
步骤 3:利用拉乌尔定律计算纯A和纯B的饱和蒸气压
拉乌尔定律指出,对于理想液态混合物,气相中各组分的分压与其在液相中的摩尔分数成正比,即${P}_{A}={P}_{A}'{x}_{A}$,${P}_{B}={P}_{B}'{x}_{B}$。根据题目条件,可以列出方程:${P}_{A}={P}_{A}'\times 0.65$,${P}_{B}={P}_{B}'\times 0.35$。由于${y}_{A}=\frac{{P}_{A}}{{P}_{总}}$,${y}_{B}=\frac{{P}_{B}}{{P}_{总}}$,可以得到${P}_{A}={P}_{总}\times {y}_{A}=5.41\times {10}^{4}Pa\times 0.45$,${P}_{B}={P}_{总}\times {y}_{B}=5.41\times {10}^{4}Pa\times 0.55$。将${P}_{A}$和${P}_{B}$的值代入拉乌尔定律的方程中,可以解出${P}_{A}'$和${P}_{B}'$的值。