题目
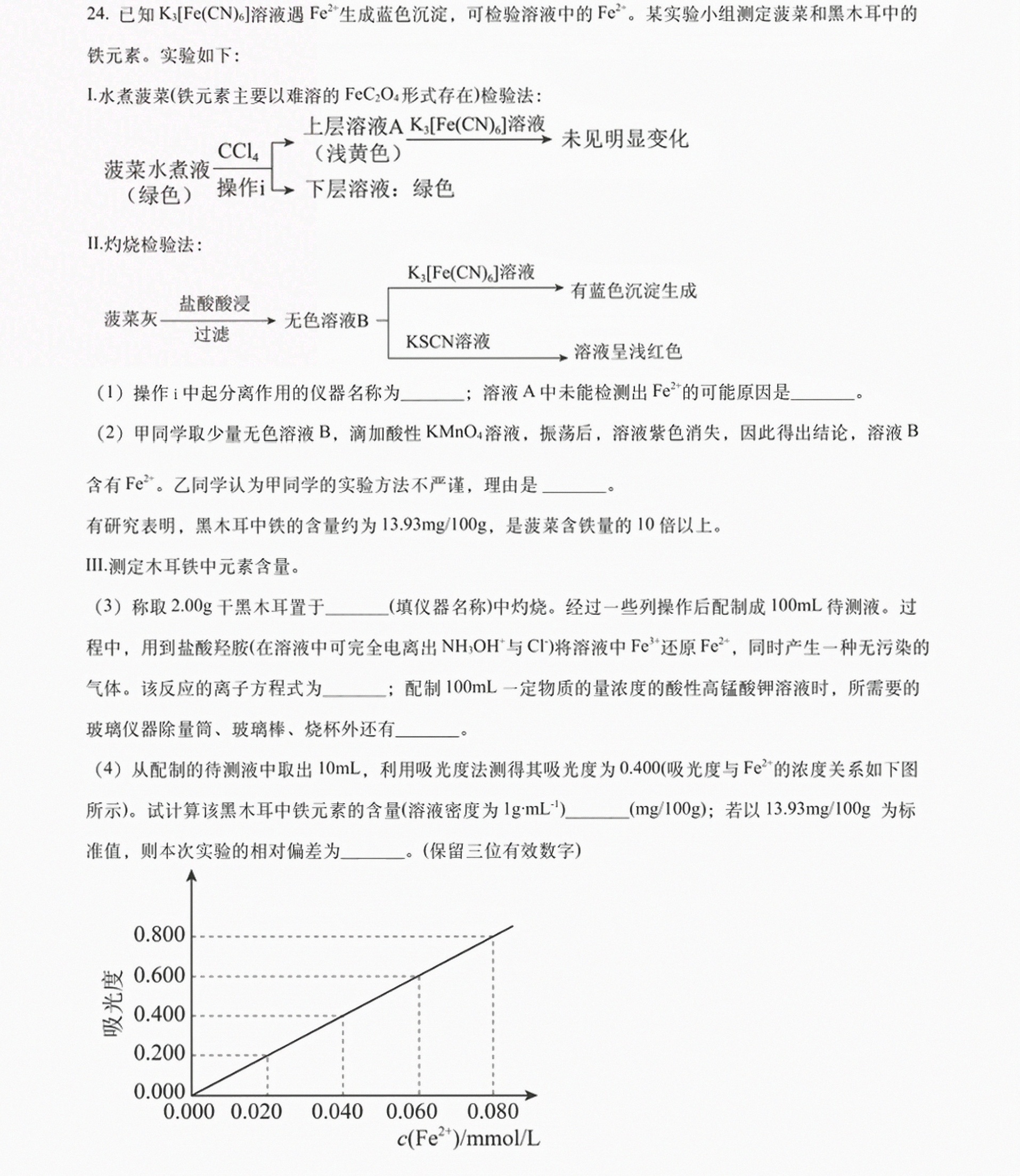
24.已知K3[Fe(CN)G]溶液遇 (e)^2+ 生成蓝色沉淀,可检验溶液中的 (e)^2+ 某实验小组测定波菜和黑木耳中的-|||-铁元素。实验如下:-|||-1.水煮菠菜(铁元素主要以难溶的FeC2O4形式存在)检验法:-|||-上层溶液AK3[Fe (CN)6]溶液-|||-菠菜水煮液 CCl4 (浅黄色) 未见明显变化-|||-(绿色) 操作i 下层溶液:绿色-|||-Ⅱ.烧烧检验法:-|||-K3[Fe(CN)6]溶液-|||-菠菜灰一盐酸酸浸 有蓝色沉淀生成-|||-过滤 KSCN溶液 溶液呈浅红色-|||-无色溶液B-|||-(1)操作i中起分离作用的仪器名称为 __ 溶液A中未能检测出 ^2+ 的可能原因是 __ 。-|||-(2)甲同学取少量无色溶液B,滴加酸性KMnO4溶液,振荡后,溶液紫色消失,因此得出结论,溶液B-|||-含有 (e)^2+ 乙同学认为甲同学的实验方法不严谨,理由是 __ 。-|||-有研究表明,黑木耳中铁的含量约为 .93mg/100g, 是菠菜含铁量的10倍以上。-|||-Ⅲ.测定木耳铁中元素含量。-|||-(3)称取2.00g干黑木耳置于 __ (填仪器名称)中灼烧。经过一些列操作后配制成100mL待测液。过-|||-程中,用到盐酸羟胺(在溶液中可完全电离出 (H)_(3)OH 与 ^- 将溶液中 (e)^3+3 还原 (e)^2+ 同时产生一种无污染的-|||-气体。该反应的离子方程式为 __ 配制100mL一定物质的量浓度的酸性高锰酸钾溶液时,所需要的-|||-玻璃仪器除量筒、玻璃棒、烧杯外还有 __ 。-|||-(4)从配制的待测液中取出10mL,利用吸光度法测得其吸光度为0.400(吸光度与 (e)^2+t 的浓度关系如下图-|||-所示)。试计算该黑木耳中铁元素的含量(溶液密度为 lg gcdot (L)^-1 __ (mg/100g); 若以 13.93mg/100g 为标-|||-准值,则本次实验的相对偏差为 __ (保留三位有效数字)-|||-0.800-|||-0.600-|||-0.400-|||-0.200-|||-0.000-|||-0.000 0.020 0.040 0.060 0.080-|||-c(Fe^(2+))/mmol/L
题目解答
答案
