题目
今有300K, 104365Pa的湿烃类混合气体(含水蒸气的), 其中水蒸气的分压力是25.5mmHg. 欲得到1000mol脱除水以后的干烃类混合气体, 试求应从湿混合气体中除去H2O的物质的量n(H2O)以及所需湿烃类混合气体的初始体积V. (参考答案)
今有300K, 104365Pa的湿烃类混合气体(含水蒸气的), 其中水蒸气的分压力是25.5mmHg. 欲得到1000mol脱除水以后的干烃类混合气体, 试求应从湿混合气体中除去H2O的物质的量n(H2O)以及所需湿烃类混合气体的初始体积V. (参考答案)
题目解答
答案
解:所需湿烃类混合气体中水的摩尔分数y(H2O) 为
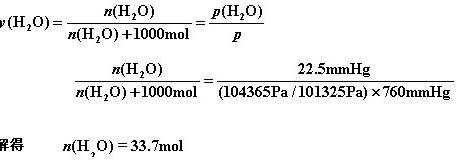

解析
步骤 1:计算湿烃类混合气体中水蒸气的摩尔分数
根据道尔顿分压定律,湿烃类混合气体中水蒸气的分压力与总压力之比等于水蒸气的摩尔分数。首先,将水蒸气的分压力从mmHg转换为Pa,然后计算水蒸气的摩尔分数。
步骤 2:计算湿烃类混合气体中水蒸气的摩尔数
根据湿烃类混合气体中水蒸气的摩尔分数和干烃类混合气体的摩尔数,计算湿烃类混合气体中水蒸气的摩尔数。
步骤 3:计算湿烃类混合气体的初始体积
将湿烃类混合气体看作理想气体,根据理想气体状态方程计算湿烃类混合气体的初始体积。
【答案】
步骤 1:计算湿烃类混合气体中水蒸气的摩尔分数
水蒸气的分压力为25.5mmHg,总压力为104365Pa。将水蒸气的分压力从mmHg转换为Pa,得到:
$p({H}_{2}O)=25.5mmHg\times \dfrac {101325Pa}{760mmHg}=3375Pa$
湿烃类混合气体中水蒸气的摩尔分数为:
$\varphi ({H}_{2}O)=\dfrac {p({H}_{2}O)}{p}=\dfrac {3375Pa}{104365Pa}=0.0323$
步骤 2:计算湿烃类混合气体中水蒸气的摩尔数
湿烃类混合气体中水蒸气的摩尔数为:
$n({H}_{2}O)=\varphi ({H}_{2}O)\times n_{总}=(1-\varphi ({H}_{2}O))\times n_{干}$
$n({H}_{2}O)=(1-0.0323)\times 1000mol=33.7mol$
步骤 3:计算湿烃类混合气体的初始体积
将湿烃类混合气体看作理想气体,根据理想气体状态方程计算湿烃类混合气体的初始体积:
$V=\dfrac {nRT}{p}=\dfrac {(1000+33.7)mol\times 8.314J/(mol\cdot K)\times 300K}{104365Pa}=25.4m^{3}$
根据道尔顿分压定律,湿烃类混合气体中水蒸气的分压力与总压力之比等于水蒸气的摩尔分数。首先,将水蒸气的分压力从mmHg转换为Pa,然后计算水蒸气的摩尔分数。
步骤 2:计算湿烃类混合气体中水蒸气的摩尔数
根据湿烃类混合气体中水蒸气的摩尔分数和干烃类混合气体的摩尔数,计算湿烃类混合气体中水蒸气的摩尔数。
步骤 3:计算湿烃类混合气体的初始体积
将湿烃类混合气体看作理想气体,根据理想气体状态方程计算湿烃类混合气体的初始体积。
【答案】
步骤 1:计算湿烃类混合气体中水蒸气的摩尔分数
水蒸气的分压力为25.5mmHg,总压力为104365Pa。将水蒸气的分压力从mmHg转换为Pa,得到:
$p({H}_{2}O)=25.5mmHg\times \dfrac {101325Pa}{760mmHg}=3375Pa$
湿烃类混合气体中水蒸气的摩尔分数为:
$\varphi ({H}_{2}O)=\dfrac {p({H}_{2}O)}{p}=\dfrac {3375Pa}{104365Pa}=0.0323$
步骤 2:计算湿烃类混合气体中水蒸气的摩尔数
湿烃类混合气体中水蒸气的摩尔数为:
$n({H}_{2}O)=\varphi ({H}_{2}O)\times n_{总}=(1-\varphi ({H}_{2}O))\times n_{干}$
$n({H}_{2}O)=(1-0.0323)\times 1000mol=33.7mol$
步骤 3:计算湿烃类混合气体的初始体积
将湿烃类混合气体看作理想气体,根据理想气体状态方程计算湿烃类混合气体的初始体积:
$V=\dfrac {nRT}{p}=\dfrac {(1000+33.7)mol\times 8.314J/(mol\cdot K)\times 300K}{104365Pa}=25.4m^{3}$