题目
称取含惰性杂质的混合碱(Na2CO3和NaOH或NaHCO3和Na2CO3的混合物)试样1.2000 g,溶于水后,用0.5000 mol·L-1 HCl标准溶液滴至酚酞褪色,用去30.00 mL。然后加人甲基橙指示剂,用HCl继续滴至橙色出现,又用去5.00 mL。问试样由何种碱组成?各组分的质量分数为多少?[M(NaOH)=40.00g·mol-1,M(NaHCO3)=84.01 g·mol-1,M(Na2CO3)=106.0g·mol-1]
称取含惰性杂质的混合碱(Na2CO3和NaOH或NaHCO3和Na2CO3的混合物)试样1.2000 g,溶于水后,用0.5000 mol·L-1 HCl标准溶液滴至酚酞褪色,用去30.00 mL。然后加人甲基橙指示剂,用HCl继续滴至橙色出现,又用去5.00 mL。问试样由何种碱组成?各组分的质量分数为多少?
[M(NaOH)=40.00g·mol-1,M(NaHCO3)=84.01 g·mol-1,M(Na2CO3)=106.0g·mol-1]
题目解答
答案
解:此题是用双指示剂法测定混合碱各组分的含量。
V1= 30.00mL V2= 5.00 mLV1>V2故混合碱试样由NaOH和Na2CO3组成(4分)
ω(Na2CO3)= 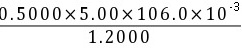 = 22.1%(3分)
= 22.1%(3分)
ω(NaOH)=  = 41.68%(3分)
= 41.68%(3分)
解析
步骤 1:确定混合碱的组成
根据题目描述,使用酚酞作为指示剂时,消耗了30.00 mL的0.5000 mol·L-1 HCl标准溶液。然后加入甲基橙指示剂,继续滴定至橙色出现,又消耗了5.00 mL的HCl。由于酚酞指示剂在碱性溶液中变色,而甲基橙指示剂在酸性溶液中变色,因此可以判断混合碱中存在两种碱性物质。根据消耗的HCl体积,可以判断混合碱由NaOH和Na2CO3组成,因为NaOH和Na2CO3的混合物在滴定过程中会先消耗NaOH,然后Na2CO3与HCl反应生成NaHCO3,再继续消耗HCl生成CO2和H2O。
步骤 2:计算Na2CO3的质量分数
根据消耗的HCl体积,可以计算出Na2CO3的物质的量。消耗的HCl体积为5.00 mL,物质的量为0.5000 mol·L-1 × 5.00 mL × 10^-3 L/mL = 2.500 × 10^-3 mol。根据Na2CO3的摩尔质量106.0 g·mol-1,可以计算出Na2CO3的质量为2.500 × 10^-3 mol × 106.0 g·mol-1 = 0.265 g。因此,Na2CO3的质量分数为0.265 g / 1.2000 g × 100% = 22.1%。
步骤 3:计算NaOH的质量分数
根据消耗的HCl体积,可以计算出NaOH的物质的量。消耗的HCl体积为30.00 mL - 5.00 mL = 25.00 mL,物质的量为0.5000 mol·L-1 × 25.00 mL × 10^-3 L/mL = 1.250 × 10^-2 mol。根据NaOH的摩尔质量40.00 g·mol-1,可以计算出NaOH的质量为1.250 × 10^-2 mol × 40.00 g·mol-1 = 0.500 g。因此,NaOH的质量分数为0.500 g / 1.2000 g × 100% = 41.67%。
根据题目描述,使用酚酞作为指示剂时,消耗了30.00 mL的0.5000 mol·L-1 HCl标准溶液。然后加入甲基橙指示剂,继续滴定至橙色出现,又消耗了5.00 mL的HCl。由于酚酞指示剂在碱性溶液中变色,而甲基橙指示剂在酸性溶液中变色,因此可以判断混合碱中存在两种碱性物质。根据消耗的HCl体积,可以判断混合碱由NaOH和Na2CO3组成,因为NaOH和Na2CO3的混合物在滴定过程中会先消耗NaOH,然后Na2CO3与HCl反应生成NaHCO3,再继续消耗HCl生成CO2和H2O。
步骤 2:计算Na2CO3的质量分数
根据消耗的HCl体积,可以计算出Na2CO3的物质的量。消耗的HCl体积为5.00 mL,物质的量为0.5000 mol·L-1 × 5.00 mL × 10^-3 L/mL = 2.500 × 10^-3 mol。根据Na2CO3的摩尔质量106.0 g·mol-1,可以计算出Na2CO3的质量为2.500 × 10^-3 mol × 106.0 g·mol-1 = 0.265 g。因此,Na2CO3的质量分数为0.265 g / 1.2000 g × 100% = 22.1%。
步骤 3:计算NaOH的质量分数
根据消耗的HCl体积,可以计算出NaOH的物质的量。消耗的HCl体积为30.00 mL - 5.00 mL = 25.00 mL,物质的量为0.5000 mol·L-1 × 25.00 mL × 10^-3 L/mL = 1.250 × 10^-2 mol。根据NaOH的摩尔质量40.00 g·mol-1,可以计算出NaOH的质量为1.250 × 10^-2 mol × 40.00 g·mol-1 = 0.500 g。因此,NaOH的质量分数为0.500 g / 1.2000 g × 100% = 41.67%。