题目
为测定CuSO 4溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题: Ⅰ.甲方案 实验原理: (O)_(4)+Ba(Cl)_(2)=BaS(O)_(4)downarrow +Cu(Cl)_(2) 实验步骤: (O)_(4)+Ba(Cl)_(2)=BaS(O)_(4)downarrow +Cu(Cl)_(2) (1)判断 (O)_(4)+Ba(Cl)_(2)=BaS(O)_(4)downarrow +Cu(Cl)_(2)沉淀完全的操作为____________。 (2)步骤②判断沉淀是否洗净所选用的试剂为_____________。 (3)步骤③灼烧时盛装样品的仪器名称为__________。 (4)固体质量为wg,则c(CuSO 4)=________mol/L。 (5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO 4)_________(填“偏高”、“偏低”或“无影响”)。 Ⅱ.乙方案 实验原理: (O)_(4)+Ba(Cl)_(2)=BaS(O)_(4)downarrow +Cu(Cl)_(2), (O)_(4)+Ba(Cl)_(2)=BaS(O)_(4)downarrow +Cu(Cl)_(2) (O)_(4)+Ba(Cl)_(2)=BaS(O)_(4)downarrow +Cu(Cl)_(2) 实验步骤: ①按如图安装装置(夹持仪器略去) ② (O)_(4)+Ba(Cl)_(2)=BaS(O)_(4)downarrow +Cu(Cl)_(2)…… ③在仪器A、B、C、D、E…中加入图示的试剂 ④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。 ⑤将CuSO 4溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生 ⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录 ⑦处理数据 (6)步骤②为___________。 (7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。 a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响 (8)Zn粉质量为ag,若测得H 2体积为bmL,已知实验条件下 (O)_(4)+Ba(Cl)_(2)=BaS(O)_(4)downarrow +Cu(Cl)_(2),则c(CuSO 4)______mol/L(列出计算表达式)。 (9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO 4)________(填“偏高”、“偏低”或“无影响”)。
为测定CuSO
4溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
Ⅰ.甲方案 实验原理: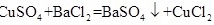
实验步骤:
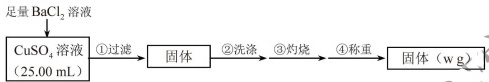
(1)判断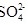 沉淀完全的操作为____________。
沉淀完全的操作为____________。
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________。
(3)步骤③灼烧时盛装样品的仪器名称为__________。
(4)固体质量为wg,则c(CuSO 4)=________mol/L。
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO 4)_________(填“偏高”、“偏低”或“无影响”)。
Ⅱ.乙方案
实验原理: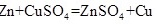 ,
,
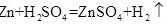
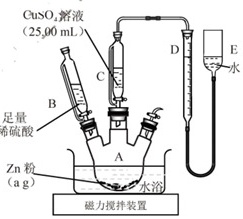
实验步骤:
①按如图安装装置(夹持仪器略去)
② ……
……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO 4溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________。
(7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(8)Zn粉质量为ag,若测得H 2体积为bmL,已知实验条件下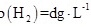 ,则c(CuSO
4)______mol/L(列出计算表达式)。
,则c(CuSO
4)______mol/L(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO 4)________(填“偏高”、“偏低”或“无影响”)。
Ⅰ.甲方案 实验原理:
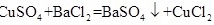
实验步骤:

(1)判断
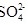 沉淀完全的操作为____________。
沉淀完全的操作为____________。
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________。
(3)步骤③灼烧时盛装样品的仪器名称为__________。
(4)固体质量为wg,则c(CuSO 4)=________mol/L。
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO 4)_________(填“偏高”、“偏低”或“无影响”)。
Ⅱ.乙方案
实验原理:
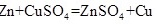 ,
,
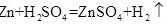

实验步骤:
①按如图安装装置(夹持仪器略去)
②
 ……
……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO 4溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________。
(7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(8)Zn粉质量为ag,若测得H 2体积为bmL,已知实验条件下
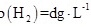 ,则c(CuSO
4)______mol/L(列出计算表达式)。
,则c(CuSO
4)______mol/L(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO 4)________(填“偏高”、“偏低”或“无影响”)。
题目解答
答案
向上层清液中继续滴加BaCl2溶液,无白色沉淀生成,则沉淀完全 AgNO3溶液等 坩埚 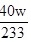 偏低 检查装置气密性 b
偏低 检查装置气密性 b 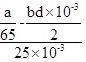 偏高
偏高
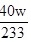 偏低 检查装置气密性 b
偏低 检查装置气密性 b 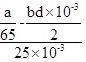 偏高
偏高解析
步骤 1:判断 ${S{O}_{4}}^{2-}$沉淀完全的操作
在沉淀反应中,判断沉淀是否完全,可以通过向沉淀后的上层清液中继续滴加沉淀剂,观察是否有新的沉淀生成。如果无沉淀生成,则说明沉淀完全。
步骤 2:判断沉淀是否洗净所选用的试剂
在沉淀反应中,为了确保沉淀完全洗净,可以使用一种能够与沉淀剂反应生成明显现象的试剂。例如,使用AgNO_3溶液,如果沉淀洗净,则滴加AgNO_3溶液后无白色沉淀生成。
步骤 3:灼烧时盛装样品的仪器名称
灼烧时,需要使用一种能够耐高温的仪器来盛装样品。常用的仪器是坩埚。
步骤 4:计算c(CuSO _4)
根据反应方程式 $CuS{O}_{4}+Ba{Cl}_{2}=BaS{O}_{4}\downarrow +Cu{Cl}_{2}$,可以知道1 mol CuSO_4生成1 mol BaSO_4。因此,根据BaSO_4的质量可以计算出CuSO_4的物质的量,进而计算出其浓度。
步骤 5:分析步骤①从烧杯中转移沉淀时未洗涤烧杯的影响
如果步骤①从烧杯中转移沉淀时未洗涤烧杯,那么烧杯中残留的CuSO_4溶液会使得测定的BaSO_4质量偏小,从而导致计算出的CuSO_4浓度偏低。
步骤 6:步骤②为检查装置气密性
在进行气体体积测量实验前,需要检查装置的气密性,以确保实验过程中气体不会泄漏。
步骤 7:分析步骤⑥需保证体系恢复到室温的原因
在气体体积测量实验中,气体的体积受温度影响较大。因此,需要保证体系恢复到室温,以确保测量的气体体积准确。
步骤 8:计算c(CuSO _4)
根据反应方程式 $Zn+CuS{O}_{4}=ZnS{O}_{4}+Cu$,可以知道1 mol Zn反应生成1 mol Cu。根据Zn的质量和生成的H_2体积,可以计算出CuSO_4的浓度。
步骤 9:分析步骤⑥E管液面高于D管的影响
如果步骤⑥E管液面高于D管,未调液面即读数,则会导致测量的气体体积偏大,从而使得计算出的CuSO_4浓度偏高。
在沉淀反应中,判断沉淀是否完全,可以通过向沉淀后的上层清液中继续滴加沉淀剂,观察是否有新的沉淀生成。如果无沉淀生成,则说明沉淀完全。
步骤 2:判断沉淀是否洗净所选用的试剂
在沉淀反应中,为了确保沉淀完全洗净,可以使用一种能够与沉淀剂反应生成明显现象的试剂。例如,使用AgNO_3溶液,如果沉淀洗净,则滴加AgNO_3溶液后无白色沉淀生成。
步骤 3:灼烧时盛装样品的仪器名称
灼烧时,需要使用一种能够耐高温的仪器来盛装样品。常用的仪器是坩埚。
步骤 4:计算c(CuSO _4)
根据反应方程式 $CuS{O}_{4}+Ba{Cl}_{2}=BaS{O}_{4}\downarrow +Cu{Cl}_{2}$,可以知道1 mol CuSO_4生成1 mol BaSO_4。因此,根据BaSO_4的质量可以计算出CuSO_4的物质的量,进而计算出其浓度。
步骤 5:分析步骤①从烧杯中转移沉淀时未洗涤烧杯的影响
如果步骤①从烧杯中转移沉淀时未洗涤烧杯,那么烧杯中残留的CuSO_4溶液会使得测定的BaSO_4质量偏小,从而导致计算出的CuSO_4浓度偏低。
步骤 6:步骤②为检查装置气密性
在进行气体体积测量实验前,需要检查装置的气密性,以确保实验过程中气体不会泄漏。
步骤 7:分析步骤⑥需保证体系恢复到室温的原因
在气体体积测量实验中,气体的体积受温度影响较大。因此,需要保证体系恢复到室温,以确保测量的气体体积准确。
步骤 8:计算c(CuSO _4)
根据反应方程式 $Zn+CuS{O}_{4}=ZnS{O}_{4}+Cu$,可以知道1 mol Zn反应生成1 mol Cu。根据Zn的质量和生成的H_2体积,可以计算出CuSO_4的浓度。
步骤 9:分析步骤⑥E管液面高于D管的影响
如果步骤⑥E管液面高于D管,未调液面即读数,则会导致测量的气体体积偏大,从而使得计算出的CuSO_4浓度偏高。