液相:3 L→ B、_、L→S2+B →E| times 100% -|||-_{1)(q)_(b)=dfrac (b{S)_(2)}({S)_(1)(S)_(2)}times dfrac (1c)(Cb)times 100% -|||-_(2)(% )_(2)=dfrac (h{S)_(1)}({S)_(1)(S)_(2)}times dfrac (1C)(Ch)times 100% -|||-液相 (% )_(0)=dfrac ({l)_(1)}({{l)_(1)}(I)_(1)}times 100% -|||-% =dfrac (b{S)_(1)}(C{S)_(1)}times dfrac ({P)_(1)}(b{P)_(1)}100% -|||-_(1)(q)_(1)=dfrac (bC)(C{S)_(1)}times dfrac ({P)_(1)}(b{P)_(1)}100% -|||-液相 (% )_(0)=dfrac (g2)(g{rho )_(2)}times 100% -|||-目相: dfrac (A+{S)_(1)+(S)_(2)arrow L}(F=0) (S2消失) dfrac (A+{S)_(1)arrow (I)_(Delta )}(F=1)A (S1消失)-A → L → A 消失-|||-液相:P2 -- P2 . c → 2 组成的熔体的冷却结晶过程(5)熔体 1 结晶结束时各相百分含量在第三次结晶过程开始前将其急冷却,各相的百分含量(6)在 P2 点对应的温度开始出现液相,在该温度下出现的最大液相量为:在 2 点对应的温度下完全熔融。组成 2 加热过程:液相:3 L→ B、_、L→S2+B →E| times 100% -|||-_{1)(q)_(b)=dfrac (b{S)_(2)}({S)_(1)(S)_(2)}times dfrac (1c)(Cb)times 100% -|||-_(2)(% )_(2)=dfrac (h{S)_(1)}({S)_(1)(S)_(2)}times dfrac (1C)(Ch)times 100% -|||-液相 (% )_(0)=dfrac ({l)_(1)}({{l)_(1)}(I)_(1)}times 100% -|||-% =dfrac (b{S)_(1)}(C{S)_(1)}times dfrac ({P)_(1)}(b{P)_(1)}100% -|||-_(1)(q)_(1)=dfrac (bC)(C{S)_(1)}times dfrac ({P)_(1)}(b{P)_(1)}100% -|||-液相 (% )_(0)=dfrac (g2)(g{rho )_(2)}times 100% -|||-目相: dfrac (A+{S)_(1)+(S)_(2)arrow L}(F=0) (S2消失) dfrac (A+{S)_(1)arrow (I)_(Delta )}(F=1)A (S1消失)-A → L → A 消失-|||-液相:P2 -- P2 . c → 2图 6-17 图 6-186-30 根据图 6-18 回答下列问题:( 1)说明化合物 S 的熔融性质,并分析相图中各界线上温度变化的方向以及界线和无变量点的性质;( 2)写出组成点为 1、2、3 及 4 各熔体的冷却结晶过程;( 3)分别将组成为 5 和组成为 6 的物系,在平衡的条件下加热到完全熔融,说明其固液相组成的变化途径。
 组成的熔体的冷却结晶过程
组成的熔体的冷却结晶过程
(5)熔体 1 结晶结束时各相百分含量
在第三次结晶过程开始前将其急冷却,各相的百分含量
(6)在 P2 点对应的温度开始出现液相,在该温度下出现的最大液相量为:
在 2 点对应的温度下完全熔融。
组成 2 加热过程:
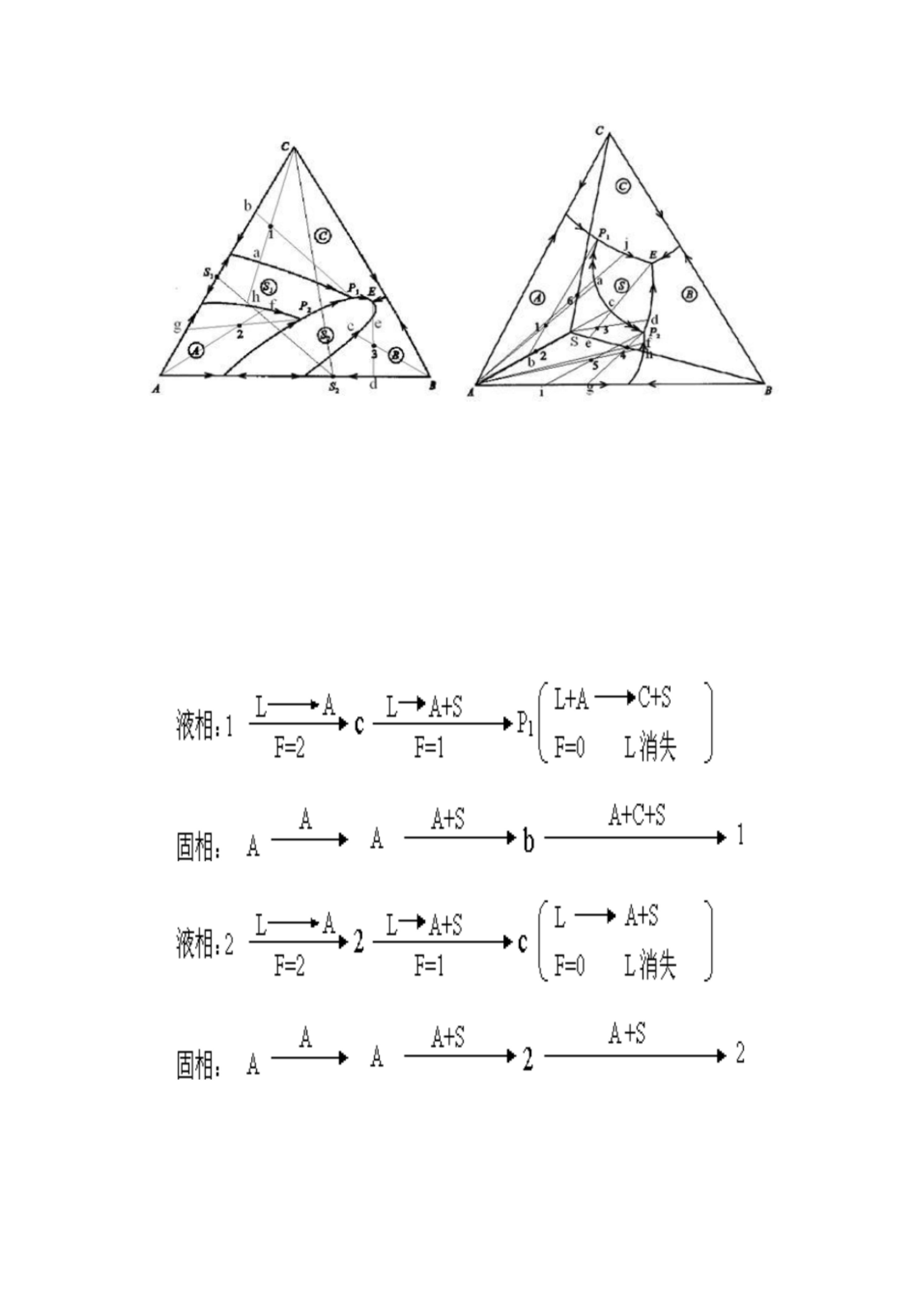 图 6-17 图 6-18
图 6-17 图 6-18
6-30 根据图 6-18 回答下列问题:( 1)说明化合物 S 的熔融性质,并分析相图中各界线上
温度变化的方向以及界线和无变量点的性质;( 2)写出组成点为 1、2、3 及 4 各熔体的冷
却结晶过程;( 3)分别将组成为 5 和组成为 6 的物系,在平衡的条件下加热到完全熔融,
说明其固液相组成的变化途径。
题目解答
答案
解:(1)化合物 S 为不一致熔融三元化合物; P1E、P2E 均为共熔界线, P1P2 为转熔界线;无
变量点 E 为低共熔点, P1、P2 均为单转熔点。
(2)组成点为 1 的熔体的冷却结晶过程:
组成点为 2 的熔体的冷却结晶过程:
组成点为 3 的熔体的冷却结晶过程:
 组成点为 4 的熔体的冷却结晶过程:
组成点为 4 的熔体的冷却结晶过程:
(3)组成为 5 物系的熔融过程:
组成为 6 物系的熔融过程:
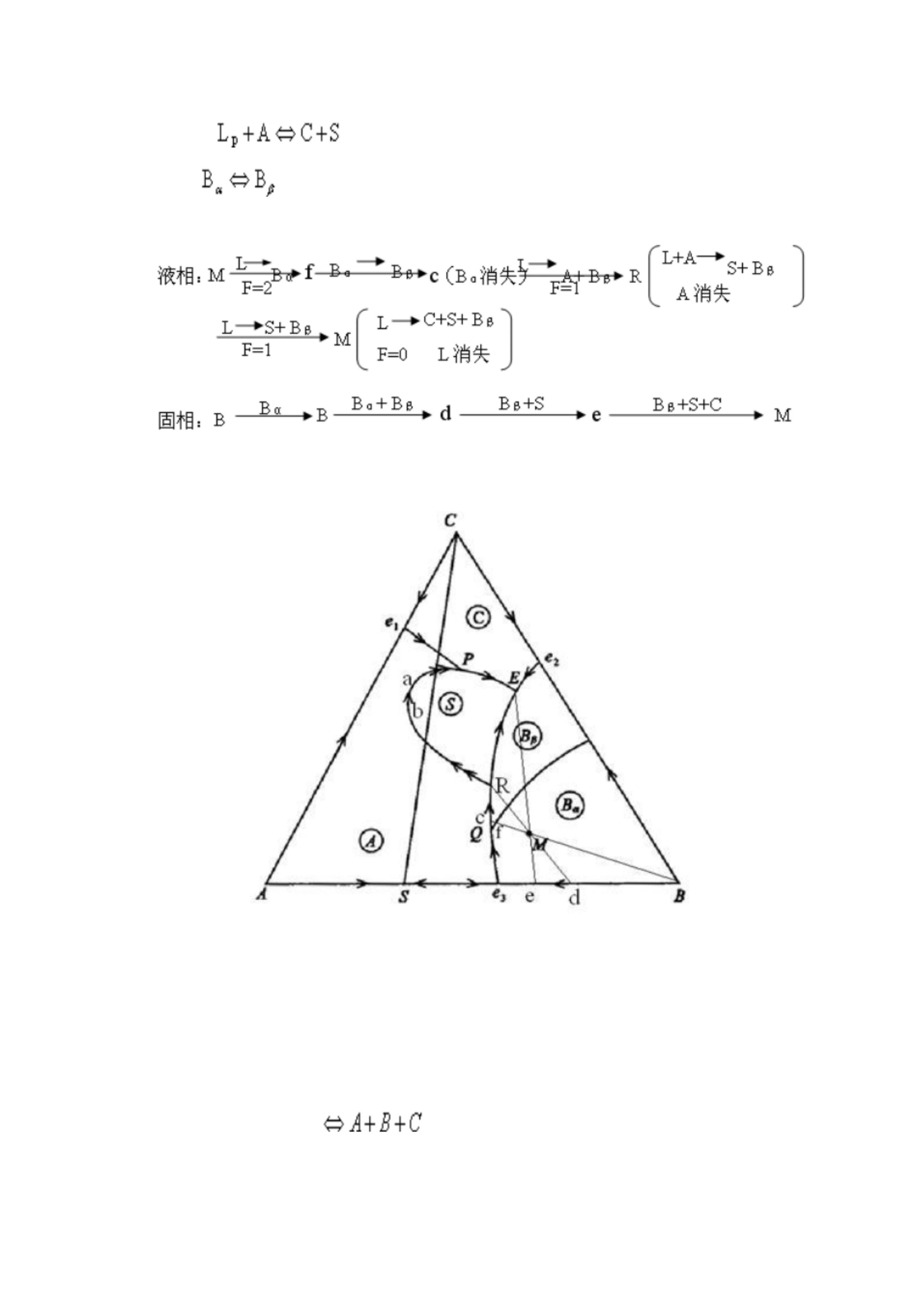
6-31 根据图 6-19 回答下列问题: (1)用箭头标出各界线的温度下降方向并说明界线性质;
(2)指出各无变量点 E、P、R、Q的性质,并写出其相平衡关系;( 3)写出熔体 M的结晶
过程,说明液相离开 R点的原因;( 4)画出 AB、BC二元系统相图。
解:( 1)界线 Ee2、e1P、ab、PE、RE、QR、e3Q均为共熔界线,界线 aP、bR为转熔界线。
(2)E 低共熔点
 P单转熔点
P单转熔点
Q过渡点
(3)熔体 M的结晶过程:
熔体 M在副△BCS内,其结晶结束点应在 E 点,所以液相离开 R点。
图 6-19
6-32 比较各种三元无变量点(低共熔点,单转熔点,双转熔点,过渡点和多晶转变点)的
特点,写出它们的平衡关系。
解:低共熔点指是一种无变量点, 系统冷却时几种晶相同时从熔液中析出, 或加热时同时融
化。相平衡关系为 L(E)
 若无变量点处于交叉位置的是单共熔分别点,在共轭位置的是双转熔点。相转变关系为
若无变量点处于交叉位置的是单共熔分别点,在共轭位置的是双转熔点。相转变关系为
,
过渡点就是转熔性质和共熔性质转变的点, 无对应三角形, 相平衡的三晶相组成在一条直线
上。
多晶转变点两种或者三种晶型发生晶型转变的温度点。
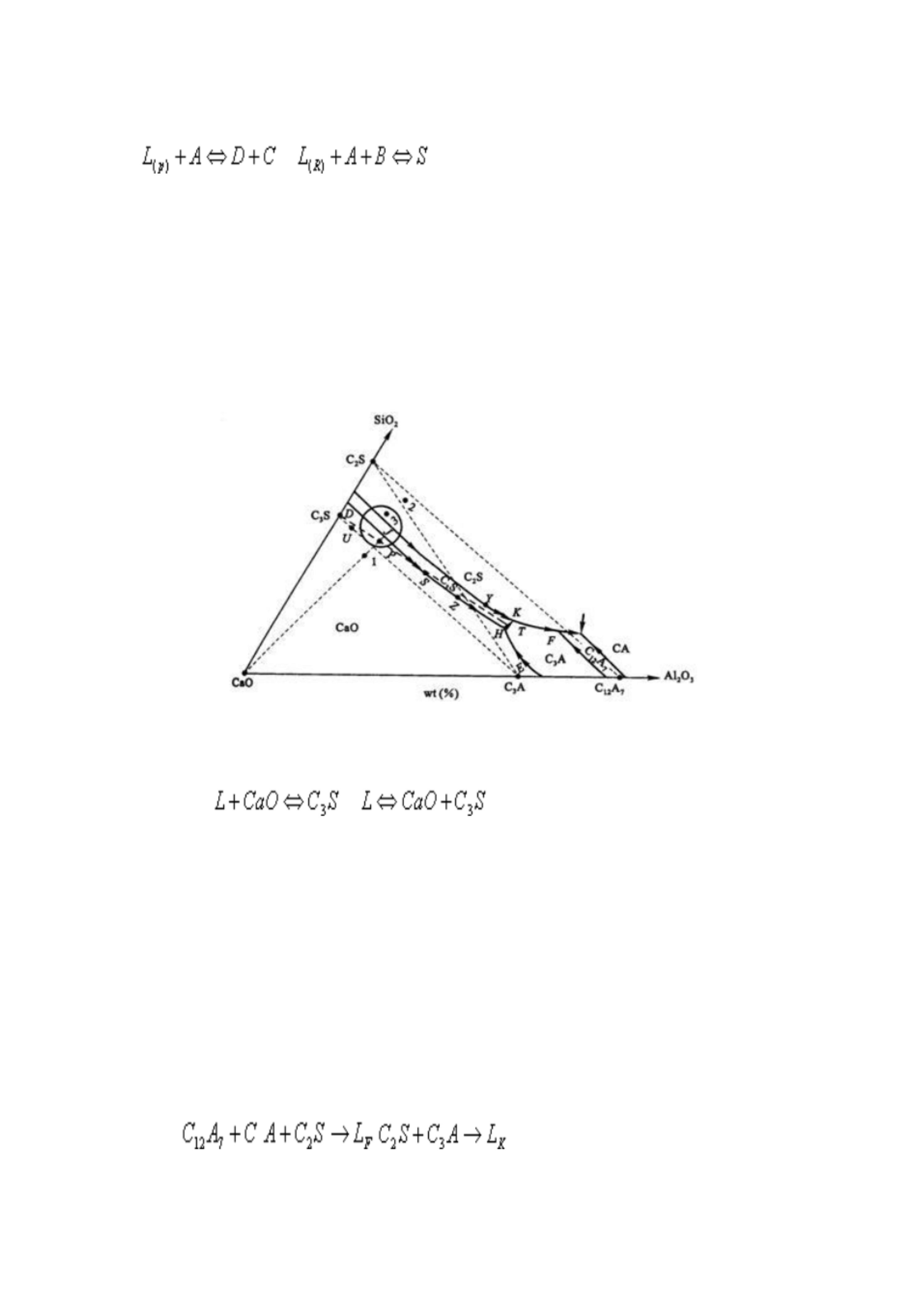
6-38 如图 6-25 为 CaO-Al 2O3-SiO2 系统的富钙部分相图,若原始液相组成位于硅酸盐水泥
的配料圈内,并恰好在 CaO和 C3S 初相区的边界曲线上。 (1)分析此液相组成的结晶过程;
(2)在缓慢冷却到无变量点 K 的温度 1455℃时急剧冷却到室温, 则最终获得哪些相, 各相
含量多少?
图 6-25 CaO-Al 2O3-SiO 2 系统高钙区部分相图
解:( 1) ,
(2)溶体平衡冷却得到产物是 C2S,C3S 和 C3A,其固相组成点为 P点, 各晶相可根据 P 点在
△C2S—C3S—C3A中的位置按双线法求得, C2S=14.6%,C3S=63.9%,C3A=21.5%。实际生产过程
中有可能会产生玻璃相。
6-39 见图 6-25 ,已知 H点的温度 1470℃,K 点温度 1455℃,F 点温度 1355℃。今取配料成
分恰为无变量点 H的组成,在充分平衡条件下,问:( l )加热该配料混合物,什么温度开
始出现液相?( 2)要使物料全部熔融,至少要加热到多高温度?( 3)写出该配合料的加
热过程相平衡表达式。
解:( 1)1335℃
(2)1455℃
(3)
 6-40 如图 6-25 ,配料 P的液相在无变量点 K发生独立析晶,最终在低共熔点 F 结束结晶。
6-40 如图 6-25 ,配料 P的液相在无变量点 K发生独立析晶,最终在低共熔点 F 结束结晶。
问此时所获得的 C3S、C2S、C3A和 C4AF四种晶相的含量各为多少?如果在 F 点仍未达到充分
平衡,残留液相能否离开 F 点向其它无变量点继续转移?为什么?
解:配料 P 的液相在无变量点 K 发生独立析晶,最终在低共熔点 F 结束结晶,所获得 C3S 为
63.9%,C2S 为 14.6%,C3A和 C4AF为 21.5%。
独立析晶过程也不一定会进行到底, 由于冷却速度较快, 还可能使熟料中残留玻璃相, 这样
的话残留玻璃相有可能离开 F 点向其它无变量点继续转移。
6-43 参看 CaO-A12O3-SiO2 系统相图(图 6-27 ),回答下列问题:( 1)组成为 66%CaO、
26%SiO2、8%A12O3的水泥配料将于什么温度开始出现液相?这时生成的最大液相量是多少;
(2)为了得到较高的 C3S 含量, (1)中组成的水泥烧成后急冷好.还是缓冷让其充分结晶
好?(3)欲得到 (l )中组成的水泥, 若只用高岭土和石灰石 (A12O3 · 2SiO2· 2H2O和 CaCO3)
配料,能否得到该水泥的组成点?为什么?若不能,需要加入何种原料?并计算出所需各
种原料的百分含量。
图 6-27CaO-Al 2O3-SiO2 系统相图
解:( 1)k 点开始出现液相,温度为 1455℃, 连接 3k 交 CaO-C3S 线于 6 点,
L%= ,线段长度可直接量取。
(2)急冷好, k 点将进行转熔过程
这样 C3S 量会减少,急冷使转熔过程来不及进行,从而提高 C3S含量
(3)AS2 与 CaCO3 配料,不能得到 3 点矿物组成