题目
写出下列电池的半电池反应及电池反应,计算其电池电动势。该电池是电解池还是原-|||-电池?-|||-|ZnS(O)_(4)(0.1molcdot (L)^-1 ) (O)_(3)(0.01molcdot (L)^-1)|Ag

题目解答
答案
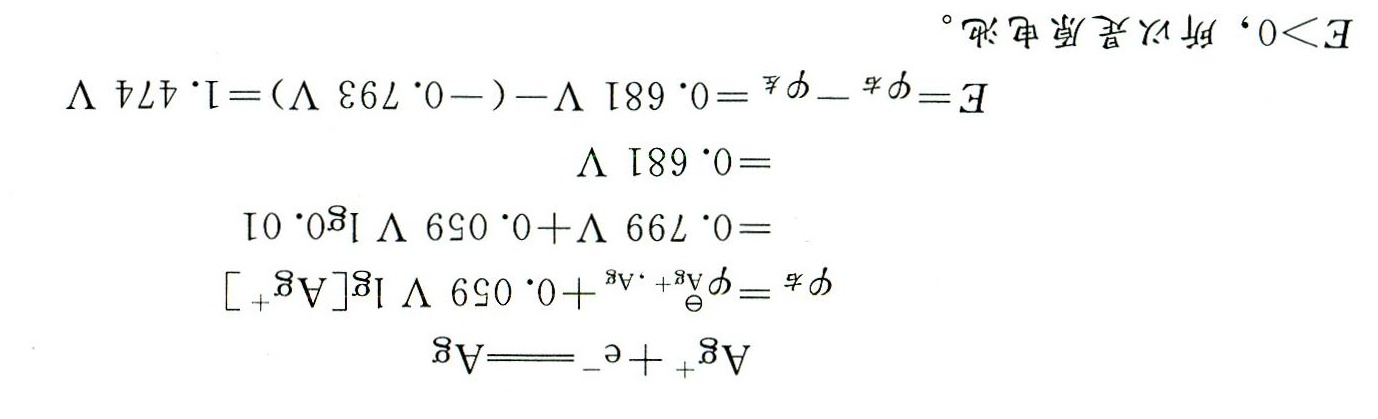
解析
步骤 1:确定半电池反应
对于锌半电池,反应为:$Zn \rightarrow Zn^{2+} + 2e^{-}$,其中$Zn^{2+}$的浓度为$0.1mol\cdot L^{-1}$。
对于银半电池,反应为:$Ag^{+} + e^{-} \rightarrow Ag$,其中$Ag^{+}$的浓度为$0.01mol\cdot L^{-1}$。
步骤 2:计算半电池电势
对于锌半电池,标准电势$\varphi_{Zn^{2+}/Zn}^{\theta} = -0.763V$,根据能斯特方程,实际电势为:
$\varphi_{Zn^{2+}/Zn} = \varphi_{Zn^{2+}/Zn}^{\theta} + \frac{0.059}{2} \log \frac{1}{[Zn^{2+}]} = -0.763V + \frac{0.059}{2} \log \frac{1}{0.1} = -0.763V + 0.0295V = -0.7335V$。
对于银半电池,标准电势$\varphi_{Ag^{+}/Ag}^{\theta} = 0.799V$,根据能斯特方程,实际电势为:
$\varphi_{Ag^{+}/Ag} = \varphi_{Ag^{+}/Ag}^{\theta} + 0.059 \log [Ag^{+}] = 0.799V + 0.059 \log 0.01 = 0.799V - 0.118V = 0.681V$。
步骤 3:计算电池电动势
电池电动势$E_{cell} = \varphi_{cathode} - \varphi_{anode} = 0.681V - (-0.7335V) = 1.4145V$。
由于$E_{cell} > 0$,所以该电池是原电池。
对于锌半电池,反应为:$Zn \rightarrow Zn^{2+} + 2e^{-}$,其中$Zn^{2+}$的浓度为$0.1mol\cdot L^{-1}$。
对于银半电池,反应为:$Ag^{+} + e^{-} \rightarrow Ag$,其中$Ag^{+}$的浓度为$0.01mol\cdot L^{-1}$。
步骤 2:计算半电池电势
对于锌半电池,标准电势$\varphi_{Zn^{2+}/Zn}^{\theta} = -0.763V$,根据能斯特方程,实际电势为:
$\varphi_{Zn^{2+}/Zn} = \varphi_{Zn^{2+}/Zn}^{\theta} + \frac{0.059}{2} \log \frac{1}{[Zn^{2+}]} = -0.763V + \frac{0.059}{2} \log \frac{1}{0.1} = -0.763V + 0.0295V = -0.7335V$。
对于银半电池,标准电势$\varphi_{Ag^{+}/Ag}^{\theta} = 0.799V$,根据能斯特方程,实际电势为:
$\varphi_{Ag^{+}/Ag} = \varphi_{Ag^{+}/Ag}^{\theta} + 0.059 \log [Ag^{+}] = 0.799V + 0.059 \log 0.01 = 0.799V - 0.118V = 0.681V$。
步骤 3:计算电池电动势
电池电动势$E_{cell} = \varphi_{cathode} - \varphi_{anode} = 0.681V - (-0.7335V) = 1.4145V$。
由于$E_{cell} > 0$,所以该电池是原电池。