电解精炼铜时,粗铜作阳极,纯铜作阴极,含Cu2+的盐溶液作电解质溶液,反应后,比铜活泼的金属以阳离子形式存在于溶液中,比铜不活泼的金属形成阳极泥。电解池及其工作原理1.电解反应实例(1)电解H2O:2H2O2H2↑+O2↑。(2)电解NaCl溶液:2NaCl+2H2O2NaOH+H2↑+Cl2↑。2.电解池(1)电解:使电流通过电解质溶液(或熔融的电解质)而在阴、阳两极引起氧化还原反应的过程。(2)电解池:将电能转化为化学能的装置。(3)电解原理①实验探究以石墨作电极电解CuCl2溶液实验装置实验现象阴极:有红色固体析出阳极:产生黄绿色气体,湿润的淀粉碘化钾试纸变蓝反应方程式阴极:Cu2++2e-===Cu阳极:2Cl--2e-===Cl2↑总反应:CuCl2Cu+Cl2↑②电解原理图示(4)电解池构成条件1.电解食盐水得到的产物是什么?反应中能量是如何转化的?提示:电解食盐水制得NaOH、Cl2和H2。反应中能量的转化形式是电能转化为化学能。2.用石墨作电极电解CuCl2溶液,通电后溶液中的离子如何移动?其中阳极和阴极发生反应的类型是什么?提示:通电后,阴离子(如Cl-)向阳极移动,阳离子(如Cu2+)向阴极移动。电解时,阳极发生氧化反应,阴极发生还原反应。3.以石墨为电极电解CuCl2溶液时,为什么会生成Cu和Cl2?提示:溶液中存在Cu2+、H+、Cl-和OH-四种离子,离子在电极上能否发生氧化还原反应,主要取决于离子得失电子的能力。因得电子能力Cu2+>H+,失电子能力Cl->OH-,故在阴极上有Cu生成,在阳极上有Cl2生成。1.电解产物的判断——“先看电极,再看顺序”(1)阳极若为活性电极(除Au、Pt外的其他金属),则优先于溶液中的任何阴离子失电子;阳极若为惰性电极,则失电子能力强的阴离子首先失电子。常见阴离子的放电顺序为S2->I->Br->Cl->OH-。(2)不管阴极的电极材料如何,都只起传导电子的作用,所以在阴极上,一定是阳离子得电子。阳离子得电子顺序可依据金属活动性顺序确定,一般放电顺序:Ag+>Fe3+>Cu2+>H+。2.原电池与电解池电极的判断1.用短线将下列电极与电极反应(或离子移动方向)连接起来。 解析:原电池的负极与电解池的阳极均发生氧化反应;原电池的正极与电解池的阴极均发生还原反应;在原电池中,阳离子向正极移动,阴离子向负极移动;在电解池中,阳离子向阴极移动,阴离子向阳极移动。实验3、4现象:锌片周围无气泡产生,铜片周围有气泡产生;电流计指针发生偏转。实验结论:锌、铜用导线连接后插入稀硫酸溶液中,导线中有电流产生。2.原电池(1)概念:将化学能转变为电能的装置。(2)工作原理(以锌-铜-稀H2SO4原电池为例):(3)构成条件a.有活泼性不同的两个电极b.电极插入电解质溶液中c.电极间构成闭合回路d.能自发地发生氧化还原反应(4)原电池的电极反应负极→流出电子→发生氧化反应,正极→流入电子→发生还原反应。
电解精炼铜时,粗铜作阳极,纯铜作阴极,含Cu2+的盐溶液作电解质溶液,反应后,比铜活泼的金属以阳离子形式存在于溶液中,比铜不活泼的金属形成阳极泥。
电解池及其工作原理
1.电解反应实例
(1)电解H2O:2H2O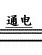 2H2↑+O2↑。
2H2↑+O2↑。
(2)电解NaCl溶液:2NaCl+2H2O 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
2.电解池
(1)电解:使电流通过电解质溶液(或熔融的电解质)而在阴、阳两极引起氧化还原反应的过程。
(2)电解池:将电能转化为化学能的装置。
(3)电解原理
①实验探究
以石墨作电极电解CuCl2溶液
实验装置
实验现象
阴极:有红色固体析出
阳极:产生黄绿色气体,湿润的淀粉碘化钾试纸变蓝
反应方程式
阴极:Cu2++2e-===Cu
阳极:2Cl--2e-===Cl2↑
总反应:CuCl2Cu+Cl2↑
②电解原理图示
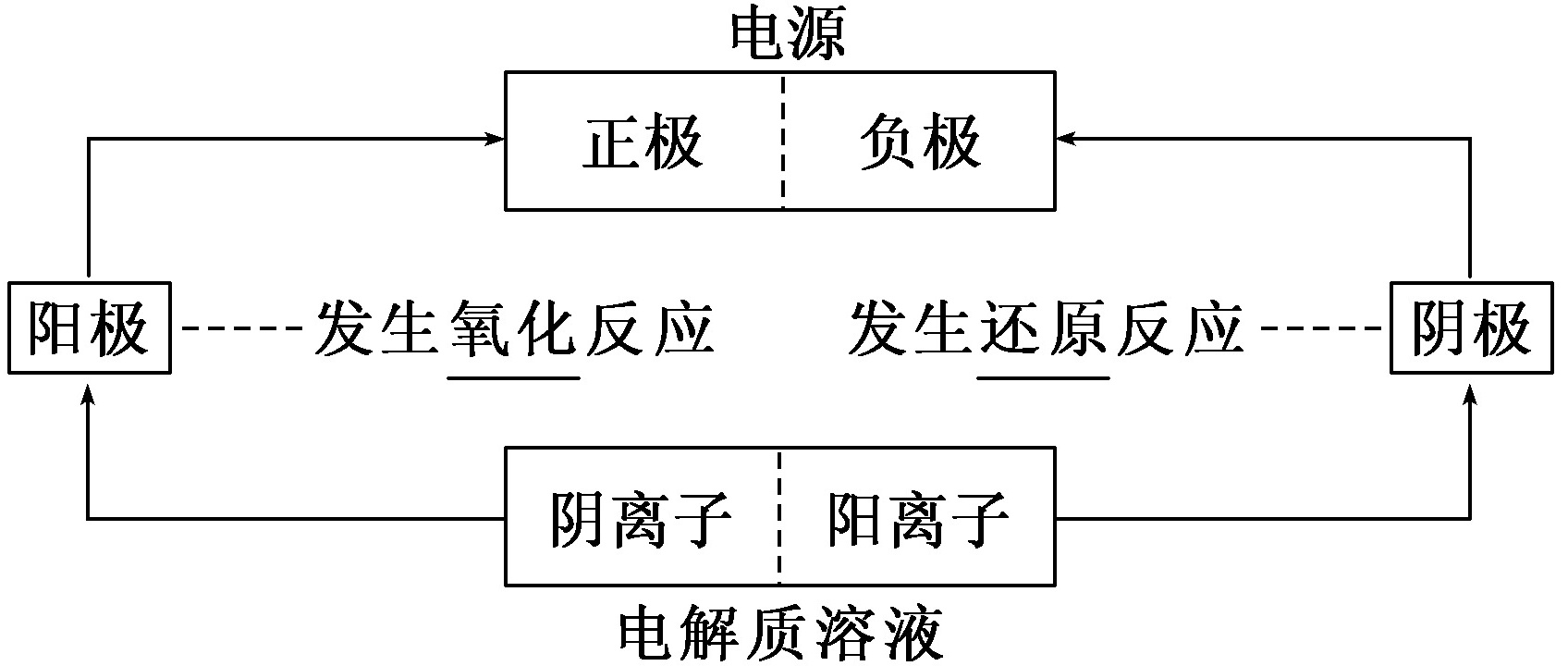
(4)电解池构成条件

1.电解食盐水得到的产物是什么?反应中能量是如何转化的?
提示:电解食盐水制得NaOH、Cl2和H2。反应中能量的转化形式是电能转化为化学能。
2.用石墨作电极电解CuCl2溶液,通电后溶液中的离子如何移动?其中阳极和阴极发生反应的类型是什么?
提示:通电后,阴离子(如Cl-)向阳极移动,阳离子(如Cu2+)向阴极移动。电解时,阳极发生氧化反应,阴极发生还原反应。
3.以石墨为电极电解CuCl2溶液时,为什么会生成Cu和Cl2?
提示:溶液中存在Cu2+、H+、Cl-和OH-四种离子,离子在电极上能否发生氧化还原反应,主要取决于离子得失电子的能力。因得电子能力Cu2+>H+,失电子能力Cl->OH-,故在阴极上有Cu生成,在阳极上有Cl2生成。

1.电解产物的判断——“先看电极,再看顺序”
(1)阳极若为活性电极(除Au、Pt外的其他金属),则优先于溶液中的任何阴离子失电子;阳极若为惰性电极,则失电子能力强的阴离子首先失电子。常见阴离子的放电顺序为S2->I->Br->Cl->OH-。
(2)不管阴极的电极材料如何,都只起传导电子的作用,所以在阴极上,一定是阳离子得电子。阳离子得电子顺序可依据金属活动性顺序确定,一般放电顺序:Ag+>Fe3+>Cu2+>H+。
2.原电池与电解池电极的判断
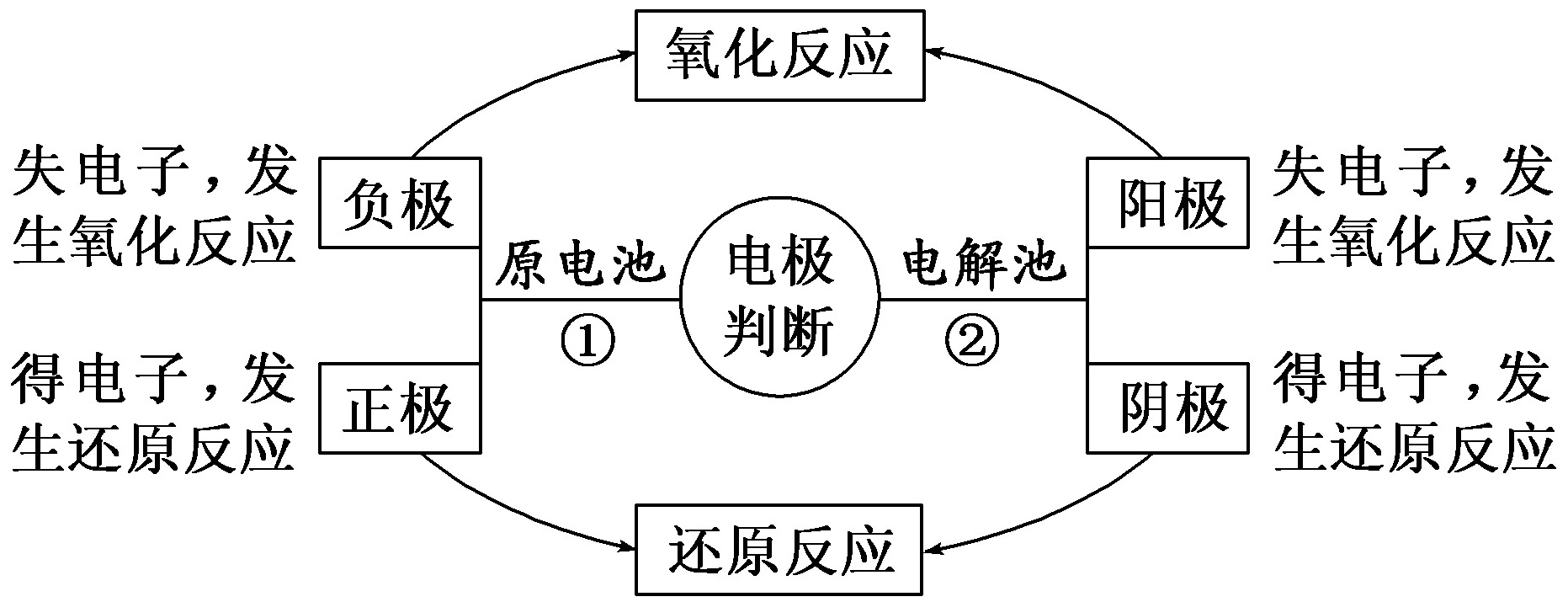

1.用短线将下列电极与电极反应(或离子移动方向)连接起来。








解析:原电池的负极与电解池的阳极均发生氧化反应;原电池的正极与电解池的阴极均发生还原反应;在原电池中,阳离子向正极移动,阴离子向负极移动;在电解池中,阳离子向阴极移动,阴离子向阳极移动。
实验3、4现象:锌片周围无气泡产生,铜片周围有气泡产生;电流计指针发生偏转。
实验结论:锌、铜用导线连接后插入稀硫酸溶液中,导线中有电流产生。
2.原电池
(1)概念:将化学能转变为电能的装置。
(2)工作原理(以锌-铜-稀H2SO4原电池为例):
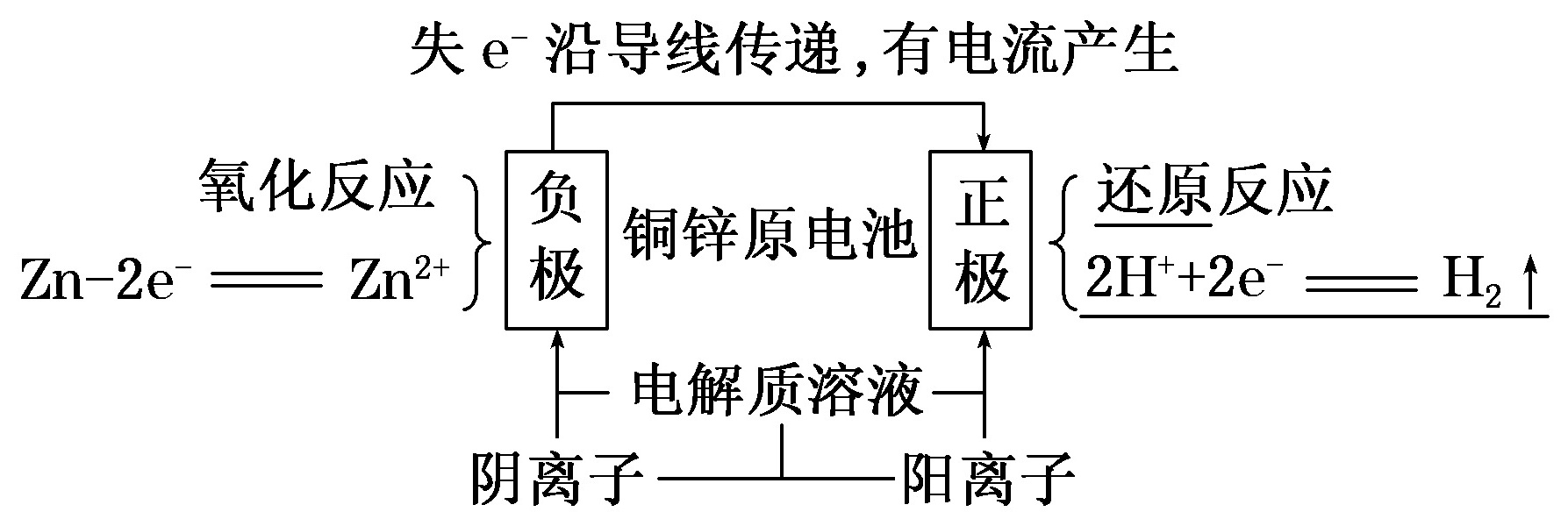
(3)构成条件
a.有活泼性不同的两个电极
b.电极插入电解质溶液中
c.电极间构成闭合回路
d.能自发地发生氧化还原反应
(4)原电池的电极反应
负极→流出电子→发生氧化反应,
正极→流入电子→发生还原反应。
题目解答
答案
答案:(1)—A、D (2)—B、C (3)—B、C (4)—A、D
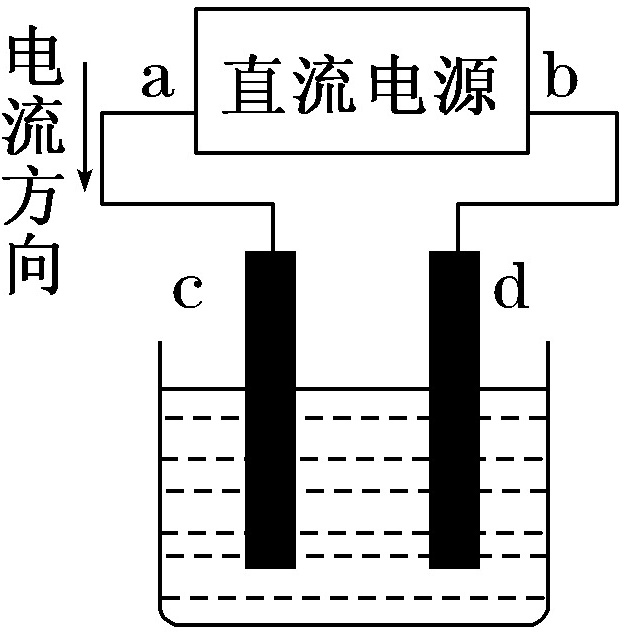 2.如图所示是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关判断正确的是( )
2.如图所示是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关判断正确的是( )
A.a为负极、b为正极
B.a为阳极、b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
解析:选C 电流从电源的正极流出,因此a为电源正极,b为负极,则c为阳极,d为阴极;电解CuCl2溶液电极反应为阳极(c电极):2Cl-2、-===Cl2↑,阴极(d电极):Cu2++2e-===Cu,故C项正确。

电解原理的应用
1.电镀
(1)概念:应用电解原理在某些金属表面镀上一薄层其他金属或合金的方法。
(2)构成

2.制备活泼金属(写出化学方程式)
(1)制取钠:2NaCl(熔融)  2Na+Cl2↑。
2Na+Cl2↑。
(2)制取镁:MgCl2(熔融)  Mg+Cl2↑。
Mg+Cl2↑。
(3)制取铝:2Al2O3(熔融)  4Al+3O2↑。
4Al+3O2↑。
3.铜的电解精炼
(1)图示
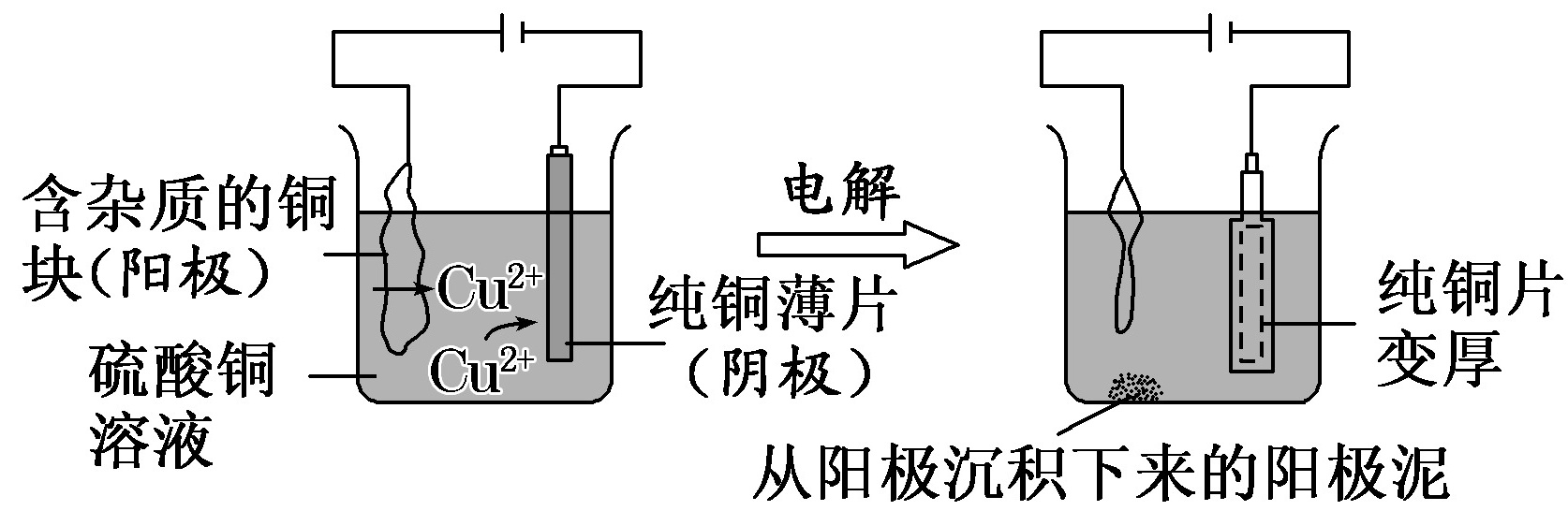
(2)电极反应
阳极:Zn2、-===Zn2+、Cu2、-===Cu2+等。
阴极:Cu2++2e-===Cu。
(3)反应特点
①比铜活泼的金属:失去电子,以阳离子的形式留在电解液中。
②活动性比铜弱的金属:以金属单质的形式沉积在电解槽底部,形成阳极泥。
③电解过程中,CuSO4溶液的浓度逐渐减小,需及时补充。