题目
9.现有0.270 kg质量分数为10%的CuCl2溶液。计算-|||-该溶液中:-|||-(1)CuCl2的物质的量;-|||-(2) ^2+ 和 Cl^- 的物质的量。

题目解答
答案
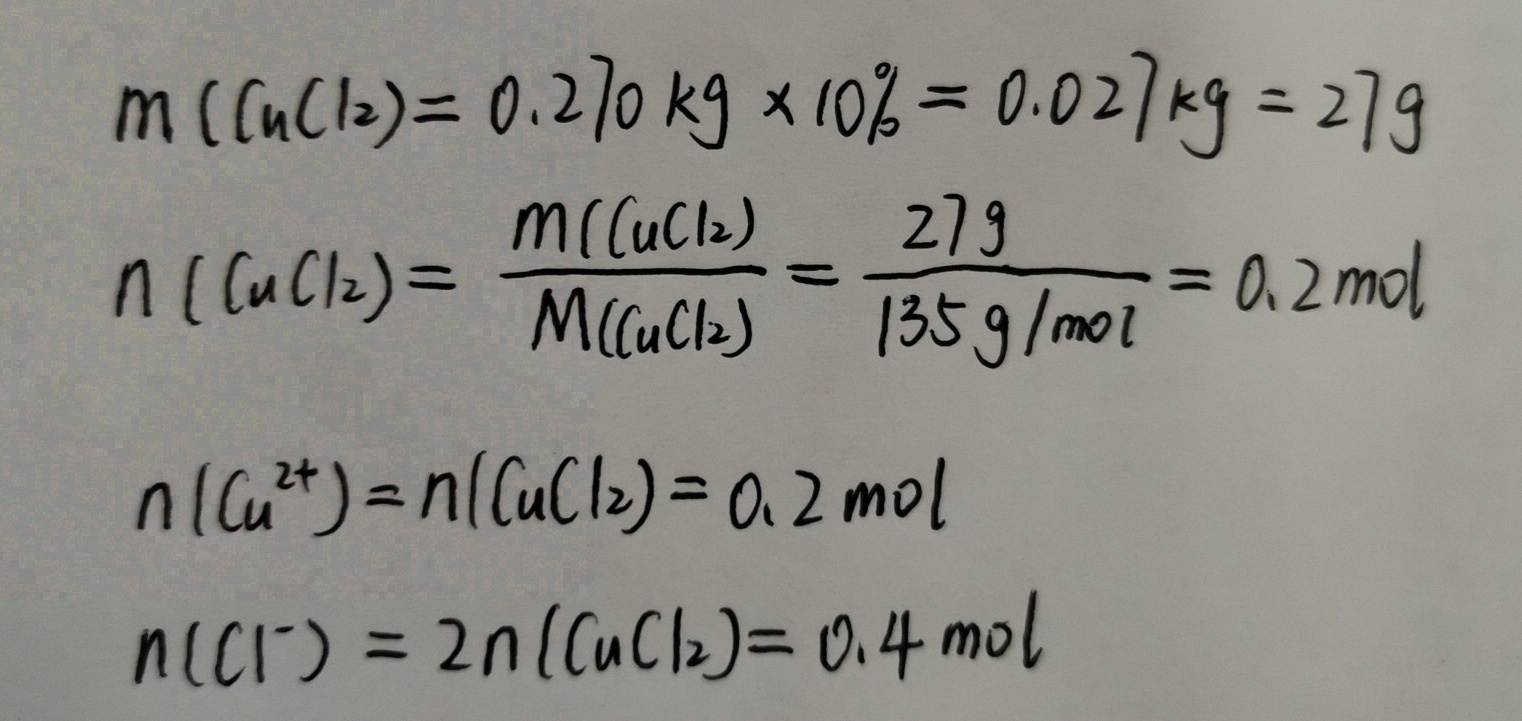
解析
步骤 1:计算CuCl2的质量
质量分数为10%,表示每100g溶液中含有10g的CuCl2。因此,0.270 kg(即270g)溶液中CuCl2的质量为:
\[ m(CuCl_2) = 270g \times 10\% = 27g \]
步骤 2:计算CuCl2的物质的量
CuCl2的摩尔质量为:
\[ M(CuCl_2) = 63.55g/mol + 2 \times 35.45g/mol = 134.45g/mol \]
因此,CuCl2的物质的量为:
\[ n(CuCl_2) = \frac{m(CuCl_2)}{M(CuCl_2)} = \frac{27g}{134.45g/mol} = 0.201mol \]
步骤 3:计算${Cu}^{2+}$和${Cl}^{-}$的物质的量
根据化学式CuCl2,每1mol的CuCl2会解离出1mol的${Cu}^{2+}$和2mol的${Cl}^{-}$。因此,${Cu}^{2+}$和${Cl}^{-}$的物质的量分别为:
\[ n(Cu^{2+}) = n(CuCl_2) = 0.201mol \]
\[ n(Cl^{-}) = 2 \times n(CuCl_2) = 2 \times 0.201mol = 0.402mol \]
质量分数为10%,表示每100g溶液中含有10g的CuCl2。因此,0.270 kg(即270g)溶液中CuCl2的质量为:
\[ m(CuCl_2) = 270g \times 10\% = 27g \]
步骤 2:计算CuCl2的物质的量
CuCl2的摩尔质量为:
\[ M(CuCl_2) = 63.55g/mol + 2 \times 35.45g/mol = 134.45g/mol \]
因此,CuCl2的物质的量为:
\[ n(CuCl_2) = \frac{m(CuCl_2)}{M(CuCl_2)} = \frac{27g}{134.45g/mol} = 0.201mol \]
步骤 3:计算${Cu}^{2+}$和${Cl}^{-}$的物质的量
根据化学式CuCl2,每1mol的CuCl2会解离出1mol的${Cu}^{2+}$和2mol的${Cl}^{-}$。因此,${Cu}^{2+}$和${Cl}^{-}$的物质的量分别为:
\[ n(Cu^{2+}) = n(CuCl_2) = 0.201mol \]
\[ n(Cl^{-}) = 2 \times n(CuCl_2) = 2 \times 0.201mol = 0.402mol \]