题目
19.(14分)金属材料对人类的生产生活起着重要的作用。请回答下列有关问题:(1)合金具有许多特殊的性能,合金的硬度一般比各成分的金属的硬度 。(2)如图1所示的实验,取一块废旧的铁丝网剪成几小片,用稀盐酸除去铁锈后的银白色的铁丝,放入锥形瓶中。向锥形瓶中加入3﹣4mL浓食盐水,塞紧带导管的单孔塞,导管的另一端伸入滴有红墨水的水中。①加入浓食盐水的作用是 。②一段时间后,观察到的现象是a.银白色的铁丝生锈变黄色,b. ;产生b现象的原因是 。③写出一条防止铁制品生锈的方法 。(3)铜制品在空气中会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3]。某化学兴趣小组欲通过实验探究“铜生锈是否需要空气中的水?”如图2所示实验中(试管内的“”均为铜片),只需完成实验 即可达到探究目的(填序号)。(4)化学兴趣小组用如图3所示装置完成木炭还原氧化铜的实验,并对生成的红色固体成分进行探究。①木炭与氧化铜发生置换反应生成使澄清石灰水变浑浊的气体。该反应的化学方程式是 。②木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用。这样处理的目的是 。③酒精灯火焰处加有铁丝网罩,其作用是 。④用上如图3所示装置完成木炭还原氧化铜的实验,试管冷却后,观察到黑色固体全部变为红色,对生成的红色固体进行探究。【查阅资料】木炭与氧化铜反应可能生成氧化亚铜(Cu2O);氧化亚铜是红色固体,能与硫酸反应:Cu2O+H2SO4═Cu+CuSO4+H2O 实验步骤 实验现象 实验结论 a.取1.8g红色固体于试管中,滴加足量 ,充分反应。 固体部分溶解; 所得固体是铜和氧化亚铜的混合物 b.将①反应后的物质过滤;将所得滤渣洗涤、干燥、称量 所得固体质量> (5)由于试管中有空气,实验时应注意:a.混合物需进行预热,除了使试管受热均匀外,目的是 。b.不能把石灰水浑浊作为木炭跟CuO反应的充分证据。因为试管中还可能发生反应: (写化学方程式)。
19.(14分)金属材料对人类的生产生活起着重要的作用。请回答下列有关问题: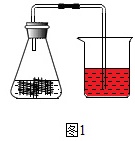


(1)合金具有许多特殊的性能,合金的硬度一般比各成分的金属的硬度 。
(2)如图1所示的实验,取一块废旧的铁丝网剪成几小片,用稀盐酸除去铁锈后的银白色的铁丝,放入锥形瓶中。向锥形瓶中加入3﹣4mL浓食盐水,塞紧带导管的单孔塞,导管的另一端伸入滴有红墨水的水中。
①加入浓食盐水的作用是 。
②一段时间后,观察到的现象是a.银白色的铁丝生锈变黄色,b. ;产生b现象的原因是 。
③写出一条防止铁制品生锈的方法 。
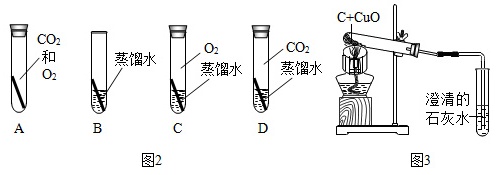
(3)铜制品在空气中会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3]。某化学兴趣小组欲通过实验探究“铜生锈是否需要空气中的水?”如图2所示实验中(试管内的“ ”均为铜片),只需完成实验 即可达到探究目的(填序号)。
”均为铜片),只需完成实验 即可达到探究目的(填序号)。
 ”均为铜片),只需完成实验 即可达到探究目的(填序号)。
”均为铜片),只需完成实验 即可达到探究目的(填序号)。(4)化学兴趣小组用如图3所示装置完成木炭还原氧化铜的实验,并对生成的红色固体成分进行探究。
①木炭与氧化铜发生置换反应生成使澄清石灰水变浑浊的气体。该反应的化学方程式是 。
②木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用。这样处理的目的是 。
③酒精灯火焰处加有铁丝网罩,其作用是 。
④用上如图3所示装置完成木炭还原氧化铜的实验,试管冷却后,观察到黑色固体全部变为红色,对生成的红色固体进行探究。
【查阅资料】木炭与氧化铜反应可能生成氧化亚铜(Cu2O);氧化亚铜是红色固体,能与硫酸反应:Cu2O+H2SO4═Cu+CuSO4+H2O
实验步骤 | 实验现象 | 实验结论 |
a.取1.8g红色固体于试管中,滴加足量 ,充分反应。 | 固体部分溶解; | 所得固体是铜和氧化亚铜的混合物 |
b.将①反应后的物质过滤;将所得滤渣洗涤、干燥、称量 | 所得固体质量> |
(5)由于试管中有空气,实验时应注意:
a.混合物需进行预热,除了使试管受热均匀外,目的是 。
b.不能把石灰水浑浊作为木炭跟CuO反应的充分证据。因为试管中还可能发生反应: (写化学方程式)。
题目解答
答案
【分析】(1)根据合金的性质来分析;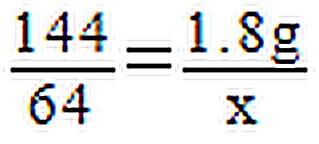
(2)根据铁锈蚀的条件、原理、装置内的压强变化以及防锈措施来分析;
(3)根据实验探究的目的以及实验设计来分析;
(4)根据化学反应的原理、使反应充分的措施、实验数据与实验结论来分析;
(5)根据加热试管的注意事项、碳的化学性质来分析。
【解答】解:(1)一般合金的硬度大于其组成中纯金属的硬度,故填:大;
(2)①加入浓食盐水的作用是加速铁的锈蚀;故填:加速铁的锈蚀;
②由于铁锈蚀消耗了锥形瓶内的氧气,锥形瓶内的压强小于外界大气压,所以一段时间后,观察到部分红墨水进入锥形瓶中;故填:部分红墨水进入锥形瓶中;铁丝生锈消耗了锥形瓶内氧气,使瓶内气压低于外界气压;
③隔绝铁与氧气、水蒸气的接触可以防止铁锈蚀,因此可采用刷漆、电镀、涂油等防锈措施;故填:刷漆(或电镀、涂油等其他合理答案均可);
(3)A实验中的铜片没有与水接触,没有锈蚀;B实验中的铜片与氧气、二氧化碳和水同时接触,发生了锈蚀;C实验中的铜片没有与二氧化碳接触,没有锈蚀;D实验中的铜片没有与氧气接触,没有锈蚀。对比实验A和实验B可知铜生锈是需要空气中的水;故填:A、B;
(4)①在高温的条件下,木炭与氧化铜发生置换反应生成铜和二氧化碳,化学方程式为:2CuO+C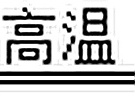 2Cu+CO2↑;故填:2CuO+C
2Cu+CO2↑;故填:2CuO+C 2Cu+CO2↑;
2Cu+CO2↑;
 2Cu+CO2↑;故填:2CuO+C
2Cu+CO2↑;故填:2CuO+C 2Cu+CO2↑;
2Cu+CO2↑;②木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用。这样处理的目的是增大木炭与氧化铜的接触面积,使反应充分;故填:增大木炭与氧化铜的接触面积,使反应充分;
③酒精灯火焰处加有铁丝网罩,其作用是使火焰集中,提高温度;故填:使火焰集中,提高温度;
④a.取1.8g红色固体于试管中,滴加足量稀硫酸,充分反应,溶液由无色变蓝色,说明反应生成了硫酸铜,而铜不能和稀硫酸反应,则证明所得固体是铜和氧化亚铜的混合物;
b.设1.8g红色固体全部是氧化亚铜,和足量稀硫酸反应生成铜的质量为x,
Cu2O+H2SO4═Cu+CuSO4+H2O,
144 64
1.8g x
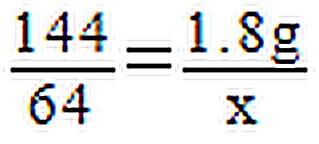
x=0.8g
过滤,将滤渣洗涤、干燥、称量,如果固体质量等于0.8g,则红色固体全部是氧化亚铜,如果固体质量大于0.8g,则红色固体是氧化亚铜和铜的混合物;
故填:a.稀硫酸;溶液由无色变为蓝色;
b.0.8g;
⑤a.混合物需进行预热,除了使试管受热均匀外,目的是减少试管内剩余空气的量,降低氧气对实验的影响;故填:减少试管内剩余空气的量,降低氧气对实验的影响;
b.因为在点燃的条件下,碳和氧气反应生成二氧化碳,所以并不能把石灰水浑浊作为木炭跟CuO反应的充分证据,化学方程式为C+O2 CO2;故填:C+O2
CO2;故填:C+O2 CO2。
CO2。
 CO2;故填:C+O2
CO2;故填:C+O2 CO2。
CO2。【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。