某废旧电池材料的主要成分为钴酸锂(LiCoO2),还含有一定量的铁、铝、铜等元素的化合物,其回收工艺如图所示,最终可得到Co2O3和锂盐。_(2)S(O)_(4)+(H)_(2)(O)_(2) NaCl(O)_(3)+(Na)_(2)C(O)_(3) 试剂X (NH4)2C2O4-|||-旧电池 还原酸浸 除铁、铝 除铜 沉钴 煅烧 Co2O3-|||-材料-|||-滤液a-|||-试剂b 沉锂 锂盐已知:CoC2O4⋅2H2O微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的C2O2−4离子生成Co(C2O4)2(n−1)−n而溶解。(l)“还原酸浸”过程中,LiCoO2发生反应的离子方程式为:___,该过程温度通常控制在40℃以下的原因是:___。(2)“除铝铁”过程的两种试剂的作用分别是___,___。(3)“除铜”所用试剂X为H2S,试写出该反应的离子方程式:___。并计算室温下该反应的平衡常数K=___,已知:25℃时Kap(CuS)=8.5×10−45,已知H2S在水中的的电离常数:K1=1.3×10−7,K2=7.l×10−15(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如下图所示:①随n(C2O2−4):N(Co2+)比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因___。②沉淀反应时间为10 min,温度在50℃以上时,随温度升高而钴的沉淀率下降的可能原因是___。_(2)S(O)_(4)+(H)_(2)(O)_(2) NaCl(O)_(3)+(Na)_(2)C(O)_(3) 试剂X (NH4)2C2O4-|||-旧电池 还原酸浸 除铁、铝 除铜 沉钴 煅烧 Co2O3-|||-材料-|||-滤液a-|||-试剂b 沉锂 锂盐(5)已知“沉锂”过程中,滤液a中的c(Li+)约为10−1mol⋅L−1,部分锂盐的溶解度数据如下表所示。 温度 Li2SO4 Li2CO30℃ 36.1g 1.33g100℃ 24.0g 0.72g结合数据分析,沉锂过程所用的试剂b是___(写化学式),相应的操作方法:向滤液a中加入略过量的试剂b,搅拌,___,___,洗涤干燥。检验沉淀洗净的方法是___。
某废旧电池材料的主要成分为钴酸锂(LiCoO2),还含有一定量的铁、铝、铜等元素的化合物,其回收工艺如图所示,最终可得到Co2O3和锂盐。
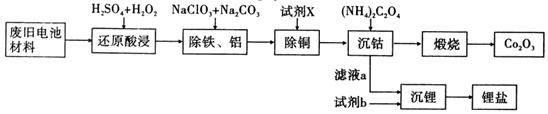
已知:CoC2O4⋅2H2O微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的C2O2−4离子生成Co(C2O4)2(n−1)−n而溶解。
(l)“还原酸浸”过程中,LiCoO2发生反应的离子方程式为:___,该过程温度通常控制在40℃以下的原因是:___。
(2)“除铝铁”过程的两种试剂的作用分别是___,___。
(3)“除铜”所用试剂X为H2S,试写出该反应的离子方程式:___。并计算室温下该反应的平衡常数K=___,已知:25℃时Kap(CuS)=8.5×10−45,已知H2S在水中的的电离常数:K1=1.3×10−7,K2=7.l×10−15
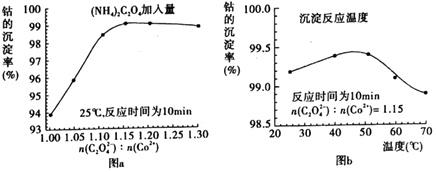
(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如下图所示:
①随n(C2O2−4):N(Co2+)比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因___。
②沉淀反应时间为10 min,温度在50℃以上时,随温度升高而钴的沉淀率下降的可能原因是___。
(5)已知“沉锂”过程中,滤液a中的c(Li+)约为10−1mol⋅L−1,部分锂盐的溶解度数据如下表所示。
| 温度 | Li2SO4 | Li2CO3 |
| 0℃ | 36.1g | 1.33g |
| 100℃ | 24.0g | 0.72g |
题目解答
答案
(1)加入过氧化氢,将Co3+还原为Co2+,反应的离子方程式为2 LiCoO2+H2O2+6H+=2Li++2Co2++O2↑+4 H2O,该过程温度通常控制在40℃以下,可避免过氧化氢分解,
故答案为:2 LiCoO2+H2O2+6H+=2Li++2Co2++O2↑+4 H2O;避免过氧化氢分解;
(2)向滤液1中加入NaClO3,NaClO3将Fe2+氧化为Fe3+,加入碳酸钠调节溶液pH,使溶液中Fe3+、Al3+沉淀,
故答案为:将Fe2+氧化为Fe3+;调节溶液pH,使溶液中Fe3+、Al3+沉淀;
(3)反应的离子方程式为Cu2++H2S=CuS↓+2H+,Kdfracc2(H+)c(Cu2+)×c(H2S)=c2(H+)c(Cu2+)×c(H2S)×c(HS−)×c(S2−)c(HS−)×c(S2−)=K1×K2Ksp=1.3×10−7×7.1×10−158.5×10−45=1.1×1023
故答案为:Cu2++H2S=CuS↓+2H+;1.1×1023;
(4)①溶液中存在化学平衡:C2O2−4(aq)+Co2+(aq)+2H2O(l)⇌CoC2O4⋅2H2O(s),随n(C2O2−4):n(Co2+)比值的增加,c(C2O2−4)增大,化学平衡正向进行有利于晶体析出,当达到n(C2O2−4):n(Co2+)=1.15以后,随草酸根离子增多,会发生副反应CoC2O4⋅2H2O+(n−1)C2O2−4=Co(C2O2−4)2(n−1)−n,使晶体部分溶解,
故答案为:随草酸根离子增多,发生CoC2O4⋅2H2O+(n−1)C2O2−4=Co(C2O2−4)2(n−1)−n,使晶体部分溶解;
②沉淀反应时间为10min,温度在40∼50℃以下时,随温度升高而钴的沉淀率升高的可能原因是它的溶解度随温度升高而逐渐增大,
故答案为:它的溶解度随温度升高而逐渐增大;
(5)由Li2SO4、Li2CO3的溶解度可知,试剂b可以是Na2CO3,且温度越高物质的溶解度越小,应加热浓缩析出Li2CO3,再趁热过滤,分离出Li2CO3,洗涤沉淀的方法是取最后一次洗涤液,加入稀盐酸酸化,再价氯化钡溶液,如无沉淀,则已洗净,
故答案为:Na2CO3;加热浓缩、趁热过滤;取最后一次洗涤液,加入稀盐酸酸化,再价氯化钡溶液,如无沉淀,则已洗净。