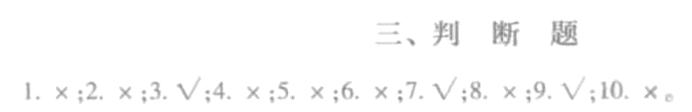题目
三、判断题-|||-1.O2为顺磁性物质,所以 ({O)_(2)}^2- 也为顺磁性物质。 ()-|||-2.在同系物HCl,HBr,HI中,因Cl、Br、I的电负性依次下降,故分子的极性依次减小,分-|||-子间的作用力也依次减小。 ()-|||-3.dn原子轨道与p,原子轨道对称性匹配。 ()-|||-4.凡是中心原子采用sp^3杂化轨道成键的分子,其分子的空间构型必定是四面体。 ()-|||-5.分子轨道中有单电子的物质,因电子自旋产生磁矩,有对抗外磁场的作用,故称它们-|||-为抗磁性物质。 ()-|||-6.与 ({O)_(2)}^+ 键长比O2短相同, _(2) 的键长也比N2短。(-|||-7. ^2+ 的极化能力大于 ^2+ 。()-|||-8.对双原子分子来说,分子的极性是由键的极性决定,已知:碳元素与氧元素的电负性-|||-相差较大,所以CO分子的偶极矩较大。 ()-|||-9.沸点高低顺序为: _(2)Ogt (H)_(2)Slt H,Selt (H)_(2)uparrow e ,说明水的沸点反常,这是因为在水分子-|||-间形成氢键。 ()-|||-10.MgO与NaF都是典型的离子化合物,晶体构型亦相同,故两者的熔点相近。 ()

题目解答
答案