保留指数定性色谱定量分析方法:色谱峰面积的测定方法:①峰高乘半峰宽法 ②峰高乘峰低宽度法 ③峰高乘平均峰宽法 ④峰高乘保留时间法 ⑤自动积分仪法常用的几种定量方法:(1)归一化法:归一化法简便、准确;进样量的准确性和操作条件的变动对测定结果影响不大;仅适用于试样中所有组分全出峰的情况。(2)外标法也称为标准曲线法,外标法不使用校正因子,准确性较高;操作条件变化对结果准确性影响较大。对进样量的准确性控制要求较高,适用于大批量试样的快速分析。(3)内标法:内标物要满足以下要求:(1)试样中不含有该物质;(2)与被测组分性质比较接近;(3)不与试样发生化学反应;(4)出峰位置应位于被测组分附近,且无组分峰影响。内标法特点:(1) 内标法的准确性较高,操作条件和进样量的稍许变动对定量结果的影响不大。 (2) 每个试样的分析,都要进行两次称量,不适合大批量试样的快速分析。气相色谱法的局限性:在缺乏标准样品的情况下定性比较困难;沸点太高或热不稳定的物质都难于应用气相色谱法进行分析。高效液相色谱法特点:高压、高效、高速, 高沸点、热不稳定有机及生化试样的高效分离分析方法。(1) 高压输液泵(2) 梯度淋洗装置(3) 进样装置:流路中为高压力工作状态,通常使用耐高压的六通阀进样装置(4) 高效分离柱(5) 高效液相色谱检测器:紫外光度检测器最常用在高效液相色谱中, 速率方程中的分子扩散项B/U较小,可以忽略不计,而只有两项,即:H = A + C u故液相色谱H-u曲线与气相色谱的形状不同影响分离的主要因素有流动相的流量、性质和极性。柱子内径一般为 1 ~ 6 mm,柱长一般为,形状为直形柱。光谱分析法导论光学分析法是基于测量物质所发射或吸收的电磁波的波长和强度的分析方法。原子光谱(发射、吸收、荧光),分子光谱;线光谱,带光谱把原子中所可能存在的光谱项---能级及能级跃迁用平面图解的形式表示出来, 称能级图。自然变宽;热(Doppler)变宽;压力变宽自吸;自蚀原子发射光谱分析方法原理:原子的核外电子一般处在基态运动,当获取足够的能量后,就会从基态跃迁到激发态,处于激发态不稳定,迅速回到基态时,就要释放出多余的能量,若此能量以光的形式出显,既得到发射光谱。光源的类型:电弧:直流电弧、交流电弧;火花;电感耦合等离子体焰炬ICP;直流电弧:稳定性差,只能作定性分析交流电弧: 稳定性好,可作定量分析;缺点:蒸发温度低,灵敏度差ICP光源的特点:1.具有好的检出限。溶液光谱分析一般元素检出限都很低。2.ICP稳定性好,精密度高,相对标准偏差约1%。3.基体效应小。4.光谱背景小。5准确度高,相对误差为1%,干扰少6自吸效应小灵敏线:信号强的谱线共振线:电子由高能态跃迁至基态所发射的谱线.原子吸收与原子荧光光谱法原子吸收:是基于物质所产生的原子蒸气对特定谱线的吸收作用来进行定量分析的方法。基态→第一激发态,又回到基态,发射出光谱线,称________。原子吸收线的半宽度:一般在~;发射线半宽度:一般在~锐线光源:空心阴极灯,即发射线半宽度远小于吸收线半宽度光源.对光源的要求:辐射强度大,稳定性高,锐线性,背景小等。(1) 火焰原子化器构造:三部分:喷雾器,雾化器,燃烧器。雾化器--使试液雾化;燃烧器--预混合型燃烧器,将雾化的试液与燃气混合火焰原子化器特点: 优:简单,火焰稳定,重现性好,精密度高,应用范围广。缺:原子化效率低只能液体进样。石墨炉原子化器:优点:绝对灵敏度高,检出 达g 原子核化效率高。缺点:基体效应,背景大,化学干扰多,重现性比火焰差。分析方法:(1).工作曲线法, 最佳吸光度,工作曲线弯曲原因。⑵. 标准加入法,能消除基体干扰,不能消背景干扰。使用时,注意要扣除背景干扰。原子荧光光谱法是通过测量原子在辐射能激发下所发射的荧光强度进行定量分析的发射光谱分析法。但所用仪器与原子吸收光谱法相近。产生:气态自由原子吸收特征辐射后跃迁到较高能级,然后又跃迁回到基态或较低能级,同时发射出与原激发辐射波长相同或不同的辐射即原子荧光。光源可用空心阴极灯,检测系统可用光电检测(光电倍增管),与原子吸收区别:(1) 光源与检测系统不在一条直线上 (2) 光源需使用高强度HCL (3)分光系统可不用光栅,甚至可用非色散型滤光片,或用日盲管PMT(320nm以上不响应)紫外:紫外光谱的形成:分子在入射光的作用下发生了价电子的跃迁,吸收了特定波长的光波形成。arrow (0)^*gt narrow (0)^*gt pi arrow (pi )^*gt narrow pi ×各种跃迁所所需能量(ΔE)的大小次序为:常见术语:生色团:分子中产生紫外吸收带的主要官能团助色团:本身在紫外区和可见区不显示吸收的原子或基团,当连接一个生色团后,则使生色团的吸收带向红移并使吸收强度增加,一般为带有p电子的原子或原子团红移:向长波移动;蓝移:向短波移动增色效应:使吸收带的吸收强度增加的效应;减色效应:使吸收带的吸收强度降低的效应溶剂的选择:1溶剂必须溶解被测物;2.选非极性溶剂(对有机物)3.考虑截止波长光源 钨灯(卤钨灯) 320~2500 nm;氢灯(氘灯) 165~350 nm吸收池:可见区——玻璃;紫外区——石英红外吸收光谱法分子中的原子与化学键处于不断的运动中。除了原子外层价电子跃迁以外,还有分子中原子的振动和分子本身的转动。通常所测得的光谱实际上是振动-转动光谱,简称振转光谱,即红外光谱。分子中基团的振动和转动能级跃迁产生:振-转光谱红外光谱测定的优点:任何气态、液态、固态样品都可以进行红外光谱的测定,这是核磁、质谱、紫外等仪器所不及的。红外光谱图:纵坐标为吸收强度,横坐标为波数1/λ,单位:cm-1应用:有机化合物的结构解析。红外光谱产生的条件 (1) 辐射应具有能满足物质产生振动跃迁所需的能量; (2) 辐射与物质间有相互偶合作用。对称分子:没有电偶极矩的变化,辐射不能引起共振,无红外活性。如:N2、O2、Cl2 等。非对称分子:有电偶极矩的变化,有红外活性。两类基本振动形式:伸缩振动,变形(弯曲)振动影响峰位变化的因素:1.内部因素【1)电子效应2)空间效应:环张力,空间位阻】2.氢键效应制样方法:气体——气体池;液体:①液膜法——难挥发液体②溶液法——液体池;固体:①研糊法(液体石腊法)②KBr压片法③薄膜法红外光谱的特征性:与一定结构单元相联系的、在一定范围内出现的化学键振动频率——基团特征频率(特征峰);基团所处化学环境不同,特征峰出现位置变化常见的有机化合物基团频率出现的范围:4000~670 cm-1(1) 4000~2500 cm-1X—H伸缩振动区(X=O,N,C,S);(2) 2400~2000 cm-1三键,累积双键伸缩振动区;(3) 1900~1200 cm-1双键伸缩振动区;(4) 1200~670 cm-1X—Y伸缩,X—H变形振动区分子的不饱和度:是指分子结构中达到饱和所缺一价元素的“对”数。如:乙烯变成饱和烷烃需要两个氢原子,不饱和度为1。计算: 若分子中仅含一,二,三,四价元素(H,O,N,C),则可按下式进行不饱和度的计算:Ω=(2 + 2n4+n3-n1)/ 2n4n3n1分别为分子中四价,三价,一价元素数目。核磁共振波谱法原子核的自旋:(1)I=0 的原子核 O(16);C(12);S(22)等,无自旋,没有磁矩,不产生共振吸收。 (2)I=1 或I>1的原子核I=1:2H,14N;I=3/2:11B,35Cl,79Br,81Br;I=5/2:17O,127I (3)I=1/2的原子核1H,13C,19F,31P原子核可看作核电荷均匀分布的球体,并自旋,有磁矩产生,是核磁共振研究的主要对象,C,H也是有机化合物的主要组成元素。当置于外加磁场H0中时,相对于外磁场,可以有(2I+1)种取向氢核(I=1/2),两种取向:(1)与外磁场平行,能量低,磁量子数m=+1/2;(2)与外磁场相反,能量高,磁量子数m=-1/2;共振条件:(1) 核有自旋(磁性核)(2) 外磁场, 能级裂分;(3) 照射频率与外磁场的比值ν0/H0=γ/(2π)由有机化合物的核磁共振图,可获得质子所处化学环境信息,进一步确定化合物结构。在有机化合物中,各种氢核周围的电子云密度不同(结构中不同位置)共振频率有差异,即引起共振吸收峰的位移,这种现象称为化学位移。核磁共振波谱仪:永久磁铁;射频振荡器;射频信号接受器;样品管化学位移的表示方法:相对标准:四甲基硅烷 Si(CH3)4(TMS)(内标) 位移常数δTMS=0为什么用TMS作为基准(1) 12个氢处于完全相同的化学环境,只产生一个尖峰; (2) 屏蔽强烈,位移最大。与有机化合物中的质子峰不重迭; (3) 化学惰性;易溶于有机溶剂;沸点低,易回收。质谱法进样系统(1.气体扩散2.直接进样3.气相色谱);离子源;质量分析器;检测器离子在磁场中的轨道半径R取决于m/e、H0、V,改变加速电压V, 可以使不同m/e的离子进入检测器。离子的分离与检测—— 质量分析器离子峰的主要类型:分子离子峰;碎片离子峰;重排离子峰;同位素离子峰;有机分子的裂解:σ―断裂,α―断裂,重排断裂电化学分析法电化学分析方法主要有下面几类: 1.电导分析法: 测定电阻参量
保留指数定性
色谱定量分析方法:色谱峰面积的测定方法:①峰高乘半峰宽法 ②峰高乘峰低宽度法 ③峰高乘平均峰宽法 ④峰高乘保留时间法 ⑤自动积分仪法
常用的几种定量方法:(1)归一化法:归一化法简便、准确;进样量的准确性和操作条件的变动对测定结果影响不大;仅适用于试样中所有组分全出峰的情况。
(2)外标法也称为标准曲线法,外标法不使用校正因子,准确性较高;操作条件变化对结果准确性影响较大。对进样量的准确性控制要求较高,适用于大批量试样的快速分析。
(3)内标法:内标物要满足以下要求:(1)试样中不含有该物质;(2)与被测组分性质比较接近;(3)不与试样发生化学反应;(4)出峰位置应位于被测组分附近,且无组分峰影响。
内标法特点:(1) 内标法的准确性较高,操作条件和进样量的稍许变动对定量结果的影响不大。 (2) 每个试样的分析,都要进行两次称量,不适合大批量试样的快速分析。
气相色谱法的局限性:
在缺乏标准样品的情况下定性比较困难;沸点太高或热不稳定的物质都难于应用气相色谱法进行分析。
高效液相色谱法
特点:高压、高效、高速, 高沸点、热不稳定有机及生化试样的高效分离分析方法。
(1) 高压输液泵(2) 梯度淋洗装置(3) 进样装置:流路中为高压力工作状态,通常使用耐高压的六通阀进样装置(4) 高效分离柱(5) 高效液相色谱检测器:紫外光度检测器最常用
在高效液相色谱中, 速率方程中的分子扩散项B/U较小,可以忽略不计,而只有两项,即:H = A + C u故液相色谱H-u曲线与气相色谱的形状不同
影响分离的主要因素有流动相的流量、性质和极性。
柱子内径一般为 1 ~ 6 mm,柱长一般为,形状为直形柱。
光谱分析法导论
光学分析法是基于测量物质所发射或吸收的电磁波的波长和强度的分析方法。
原子光谱(发射、吸收、荧光),分子光谱;线光谱,带光谱
把原子中所可能存在的光谱项---能级及能级跃迁用平面图解的形式表示出来, 称能级图。
自然变宽;热(Doppler)变宽;压力变宽
自吸;自蚀
原子发射光谱分析
方法原理:原子的核外电子一般处在基态运动,当获取足够的能量后,就会从基态跃迁到激发态,处于激发态不稳定,迅速回到基态时,就要释放出多余的能量,若此能量以光的形式出显,既得到发射光谱。
光源的类型:电弧:直流电弧、交流电弧;火花;电感耦合等离子体焰炬ICP;
直流电弧:稳定性差,只能作定性分析
交流电弧: 稳定性好,可作定量分析;缺点:蒸发温度低,灵敏度差
ICP光源的特点:1.具有好的检出限。溶液光谱分析一般元素检出限都很低。2.ICP稳定性好,精密度高,相对标准偏差约1%。3.基体效应小。4.光谱背景小。5准确度高,相对误差为1%,干扰少6自吸效应小
灵敏线:信号强的谱线
共振线:电子由高能态跃迁至基态所发射的谱线.
原子吸收与原子荧光光谱法
原子吸收:是基于物质所产生的原子蒸气对特定谱线的吸收作用来进行定量分析的方法。
基态→第一激发态,又回到基态,发射出光谱线,称________。
原子吸收线的半宽度:一般在~;发射线半宽度:一般在~
锐线光源:空心阴极灯,即发射线半宽度远小于吸收线半宽度光源.
对光源的要求:辐射强度大,稳定性高,锐线性,背景小等。
(1) 火焰原子化器构造:三部分:喷雾器,雾化器,燃烧器。
雾化器--使试液雾化;燃烧器--预混合型燃烧器,将雾化的试液与燃气混合
火焰原子化器特点: 优:简单,火焰稳定,重现性好,精密度高,应用范围广。
缺:原子化效率低只能液体进样。
石墨炉原子化器:优点:绝对灵敏度高,检出 达g 原子核化效率高。
缺点:基体效应,背景大,化学干扰多,重现性比火焰差。
分析方法:(1).工作曲线法, 最佳吸光度,工作曲线弯曲原因。
⑵. 标准加入法,能消除基体干扰,不能消背景干扰。使用时,注意要扣除背景干扰。
原子荧光光谱法是通过测量原子在辐射能激发下所发射的荧光强度进行定量分析的发射光谱分析法。但所用仪器与原子吸收光谱法相近。
产生:气态自由原子吸收特征辐射后跃迁到较高能级,然后又跃迁回到基态或较低能级,同时发射出与原激发辐射波长相同或不同的辐射即原子荧光。
光源可用空心阴极灯,检测系统可用光电检测(光电倍增管),
与原子吸收区别:(1) 光源与检测系统不在一条直线上 (2) 光源需使用高强度HCL (3)分光系统可不用光栅,甚至可用非色散型滤光片,或用日盲管PMT(320nm以上不响应)
紫外:
紫外光谱的形成:分子在入射光的作用下发生了价电子的跃迁,吸收了特定波长的光波形成。
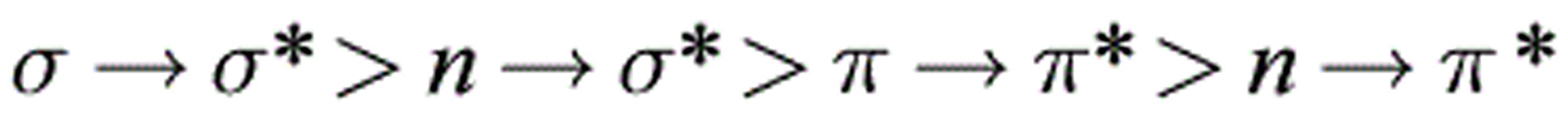 各种跃迁所所需能量(ΔE)的大小次序为:
各种跃迁所所需能量(ΔE)的大小次序为:
常见术语:
生色团:分子中产生紫外吸收带的主要官能团
助色团:本身在紫外区和可见区不显示吸收的原子或基团,当连接一个生色团后,则使生色团的吸收带向红移并使吸收强度增加,一般为带有p电子的原子或原子团
红移:向长波移动;蓝移:向短波移动
增色效应:使吸收带的吸收强度增加的效应;减色效应:使吸收带的吸收强度降低的效应
溶剂的选择:1溶剂必须溶解被测物;2.选非极性溶剂(对有机物)3.考虑截止波长
光源 钨灯(卤钨灯) 320~2500 nm;氢灯(氘灯) 165~350 nm
吸收池:可见区——玻璃;紫外区——石英
红外吸收光谱法
分子中的原子与化学键处于不断的运动中。除了原子外层价电子跃迁以外,还有分子中原子的振动和分子本身的转动。通常所测得的光谱实际上是振动-转动光谱,简称振转光谱,即红外光谱。
分子中基团的振动和转动能级跃迁产生:振-转光谱
红外光谱测定的优点:任何气态、液态、固态样品都可以进行红外光谱的测定,这是核磁、质谱、紫外等仪器所不及的。
红外光谱图:纵坐标为吸收强度,横坐标为波数1/λ,单位:cm-1
应用:有机化合物的结构解析。
红外光谱产生的条件 (1) 辐射应具有能满足物质产生振动跃迁所需的能量; (2) 辐射与物质间有相互偶合作用。
对称分子:没有电偶极矩的变化,辐射不能引起共振,无红外活性。如:N2、O2、Cl2 等。
非对称分子:有电偶极矩的变化,有红外活性。
两类基本振动形式:伸缩振动,变形(弯曲)振动
影响峰位变化的因素:1.内部因素【1)电子效应2)空间效应:环张力,空间位阻】2.氢键效应
制样方法:气体——气体池;液体:①液膜法——难挥发液体②溶液法——液体池;固体:①研糊法(液体石腊法)②KBr压片法③薄膜法
红外光谱的特征性:与一定结构单元相联系的、在一定范围内出现的化学键振动频率——基团特征频率(特征峰);基团所处化学环境不同,特征峰出现位置变化
常见的有机化合物基团频率出现的范围:4000~670 cm-1
(1) 4000~2500 cm-1X—H伸缩振动区(X=O,N,C,S);(2) 2400~2000 cm-1三键,累积双键伸缩振动区;(3) 1900~1200 cm-1双键伸缩振动区;(4) 1200~670 cm-1X—Y伸缩,X—H变形振动区
分子的不饱和度:是指分子结构中达到饱和所缺一价元素的“对”数。如:乙烯变成饱和烷烃需要两个氢原子,不饱和度为1。
计算: 若分子中仅含一,二,三,四价元素(H,O,N,C),则可按下式进行不饱和度的计算:Ω=(2 + 2n4+n3-n1)/ 2n4n3n1分别为分子中四价,三价,一价元素数目。
核磁共振波谱法
原子核的自旋:(1)I=0 的原子核 O(16);C(12);S(22)等,无自旋,没有磁矩,不产生共振吸收。 (2)I=1 或I>1的原子核I=1:2H,14N;I=3/2:11B,35Cl,79Br,81Br;I=5/2:17O,127I (3)I=1/2的原子核1H,13C,19F,31P
原子核可看作核电荷均匀分布的球体,并自旋,有磁矩产生,是核磁共振研究的主要对象,C,H也是有机化合物的主要组成元素。
当置于外加磁场H0中时,相对于外磁场,可以有(2I+1)种取向
氢核(I=1/2),两种取向:(1)与外磁场平行,能量低,磁量子数m=+1/2;(2)与外磁场相反,能量高,磁量子数m=-1/2;
共振条件:(1) 核有自旋(磁性核)(2) 外磁场, 能级裂分;(3) 照射频率与外磁场的比值ν0/H0=γ/(2π)
由有机化合物的核磁共振图,可获得质子所处化学环境信息,进一步确定化合物结构。
在有机化合物中,各种氢核周围的电子云密度不同(结构中不同位置)共振频率有差异,即引起共振吸收峰的位移,这种现象称为化学位移。
核磁共振波谱仪:永久磁铁;射频振荡器;射频信号接受器;样品管
化学位移的表示方法:相对标准:四甲基硅烷 Si(CH3)4(TMS)(内标) 位移常数δTMS=0
为什么用TMS作为基准(1) 12个氢处于完全相同的化学环境,只产生一个尖峰; (2) 屏蔽强烈,位移最大。与有机化合物中的质子峰不重迭; (3) 化学惰性;易溶于有机溶剂;沸点低,易回收。
质谱法
进样系统(1.气体扩散2.直接进样3.气相色谱);离子源;质量分析器;检测器
离子在磁场中的轨道半径R取决于m/e、H0、V,改变加速电压V, 可以使不同m/e的离子进入检测器。
离子的分离与检测—— 质量分析器
离子峰的主要类型:分子离子峰;碎片离子峰;重排离子峰;同位素离子峰;
有机分子的裂解:σ―断裂,α―断裂,重排断裂
电化学分析法
电化学分析方法主要有下面几类: 1.电导分析法: 测定电阻参量
题目解答
答案
共振发射线