题目
在电解质NaCl、NaOH、HCl、H2SO4、HAc溶液中无限稀释摩尔电导率不能用外推法到的是
在电解质NaCl、NaOH、HCl、H2SO4、HAc溶液中无限稀释摩尔电导率不能用外推法
到的是
题目解答
答案
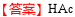
解析
步骤 1:理解无限稀释摩尔电导率的概念
无限稀释摩尔电导率是指电解质溶液在无限稀释时的摩尔电导率。在无限稀释条件下,电解质分子几乎完全解离,溶液中的离子浓度极低,离子间的相互作用可以忽略不计,此时的摩尔电导率可以视为离子的本征电导率。
步骤 2:理解外推法的适用条件
外推法是通过测量不同浓度的电解质溶液的摩尔电导率,然后根据这些数据进行线性外推,以得到无限稀释摩尔电导率。这种方法适用于完全解离的强电解质,因为它们在稀释过程中摩尔电导率的变化是线性的。
步骤 3:分析各电解质的解离情况
- NaCl、NaOH、HCl、H2SO4都是强电解质,在水中完全解离,因此它们的无限稀释摩尔电导率可以用外推法得到。
- HAc是弱电解质,在水中部分解离,其摩尔电导率随浓度的变化不是线性的,因此不能用外推法得到其无限稀释摩尔电导率。
无限稀释摩尔电导率是指电解质溶液在无限稀释时的摩尔电导率。在无限稀释条件下,电解质分子几乎完全解离,溶液中的离子浓度极低,离子间的相互作用可以忽略不计,此时的摩尔电导率可以视为离子的本征电导率。
步骤 2:理解外推法的适用条件
外推法是通过测量不同浓度的电解质溶液的摩尔电导率,然后根据这些数据进行线性外推,以得到无限稀释摩尔电导率。这种方法适用于完全解离的强电解质,因为它们在稀释过程中摩尔电导率的变化是线性的。
步骤 3:分析各电解质的解离情况
- NaCl、NaOH、HCl、H2SO4都是强电解质,在水中完全解离,因此它们的无限稀释摩尔电导率可以用外推法得到。
- HAc是弱电解质,在水中部分解离,其摩尔电导率随浓度的变化不是线性的,因此不能用外推法得到其无限稀释摩尔电导率。