非金属及其化合物1.下列说法不正确的是A.[Cu(NH3)4]SO4可通过CuSO4溶液与过量氨水作用得到B.铁锈的主要成分可表示为Fe2O3·nH2OC.钙单质可以从TiCl4中置换出TiD.可用H2还原MgO制备单质Mg【答案】D【解析】A.硫酸铜溶液与氨水反应,当氨水过量时发生反应生成[Cu(NH3)4]SO4,A选项正确;B.在钢铁发生吸氧腐蚀时生成氢氧化亚铁,总反应为:2Fe+O2+2H2O═2Fe(OH)2,Fe(OH)2被氧化为Fe(OH)3:4Fe(OH)2+O2+2H2O=Fe(OH)3,Fe(OH)3分解即得铁锈:2Fe(OH)3=Fe2O3•nH2O+(3-n)H2O,故所得铁锈的主要成分为Fe2O3•nH2O,,B选项正确;C.钙还原性较强,钙单质可以从TiCl4中置换出Ti,C选项正确;D.镁属于较活泼金属,不能利用氢气还原氧化镁制备镁,而是常用电解熔融MgCl2的方法,D选项错误;答案选D。2.下列叙述正确的是( )A.Fe在氯气中燃烧生成FeCl2B.将AlCl3溶液逐滴滴入到NaOH溶液,先产生白色沉淀,最后沉淀消失C.电解氯化铝溶液制取金属单质铝D.常温下,铝制品用浓硫酸或浓硝酸处理过,可耐腐蚀【答案】D【解析】A.Fe在氯气中燃烧生成FeCl3,故A错误;B.将AlCl3溶液逐滴滴入到NaOH溶液,先生成偏铝酸钠,后生成氢氧化铝,涉及反应为AlCl3+4NaOH=NaAlO2+2H2O+3NaCl、AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl,现象为:先不产生沉淀,后沉淀逐渐增多至不变,故B错误;C.电解熔融状态的氧化铝制取金属单质铝,电解氯化铝溶液生成氢氧化铝、氢气和氯气,故C错误;D.铝可与浓硫酸、浓硝酸在常温下发生钝化反应。常温下,铝制品用浓硫酸或浓硝酸处理过,表面形成一层致密的氧化膜,可耐腐蚀,故D正确;故选D。【点睛】本题综合考查元素化合物知识,侧重于学生的分析能力和实验能力的考查,学习中注意相关基础知识的积累,难点B,将NaOH溶液逐滴滴入到AlCl3溶液,先产生白色沉淀,最后沉淀消失,注意滴加次序不同,产生的现象不同。3.下列说法正确的是( )A.铁制器具表面涂油,可防止其锈蚀B.使氯水褪色,证明具有漂白性C.在空气中蒸干溶液可获得固体D.浓盐酸敞口放置浓度会降低,说明其具有吸水性【答案】A【解析】A.铁制器具表面涂油,可使其与空气隔绝,A项正确;B.使氯水褪色是具有强的还原性,B项错误;C.溶液在蒸干过程中与空气接触,被氧化会有生成,C项错误;D.浓盐酸长期暴露于空气中浓度降低,是因为其具有挥发性,D项错误;答案选A。4.下列有关实验的现象和结论都正确,且二者具有因果关系的是( )【答案】B【解析】A.Na2O2久置后会生成Na2CO3,Na2CO3与盐酸反应生成无色无味的CO2,A错误;B.向偏铝酸钠溶液中通入二氧化碳,生成白色的氢氧化铝,氢氧化铝为两性氢氧化物可溶于强酸或者强碱,但不溶于弱酸弱碱,B正确;C.Cu在常温下不与浓硫酸反应,C错误;D.若溶液X中若含,滴加稀硝酸时被氧化为,再滴加BaCl2溶液时,也有白色沉淀生成,D错误;故选B。5.如图是产生和收集气体的实验装置,该装置适合于( ) A.用浓硝酸与Cu反应制取NO2B.用浓盐酸和MnO2反应制取Cl2C.用H2O2溶液和MnO2反应制取O2D.用NH4Cl和Ca(OH)2反应制取NH3【答案】C【解析】A.铜与浓硝酸反应生成二氧化氮,实验为固体和液体常温下反应生成气体实验,且二氧化氮难溶于水,不能用排水法收集,需用向上排空气法收集,故A错误;B.用浓盐酸和二氧化锰反应制取氯气需要加热,发生装置错误,氯气可与水反应,不可用排水法收集,需用排饱和食盐水收集,故B错误;C.用H2O2溶液和MnO2反应制取O2属于固液常温型,氧气难溶于水,可用排水法收集,故C正确;D.氯化铵和氢氧化钙是固体,反应需要加热,所以反应应该在试管中进行,且试管口略向下倾斜,发生装置错误;氨气极易溶于水,不可用排水法收集,故D错误;答案选C。6.下列说法中正确的是A.Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色B.Na2O2与CO2反应生成0.1molO2时转移电子0.4molC.向饱和烧碱溶液中加入2gNa2O2充分反应完时,溶液中c(Na+)不变D.将Na2O2投入CuCl2溶液中有蓝色沉淀及气泡产生【答案】D【解析】A.Na2O2遇到湿润的紫色石蕊试纸后,可以和水之间反应生成氢氧化钠和氧气,石蕊试纸变蓝,但是过氧化钠具有漂白性,最终试纸变白色,故A错误;B.过氧化钠与水反应为歧化反应,过氧化钠既是氧化剂又是还原剂,生成1mol氧气转移2mol电子,则生成0.1 mol氧气转移电子0.2mol,故B错误;C.Na2O2与水反应时放出大量热,反应后溶液温度升高,导致氢氧化钠溶液的溶解度增大,所以溶液中钠离子浓度增大,故C错误;D.Na2O2投入到CuCl2溶液中,反应生成氢氧化铜沉淀和氧气,所以有蓝色沉淀及气泡产生,故D正确。答案选D。【点睛】明确过氧化钠的性质为解答关键,注意熟练掌握常见元素及其化合物性质。7.下列说法不正确的是( )A.FeSO4常用于制取净水剂,原因是溶于水时形成具有净水作用的氢氧化亚铁胶体B.纳米铁粉和FeS都可以去除水体中的Cu2+、Hg2+等离子,其原理不相同C.SO2具有还原性,可用KMnO4溶液测定食品中SO2残留量D.利用碳酸钠溶液可消除燃煤烟气中的SO2【答案】A【解析】A.FeSO4常用于制取净水剂,原因是溶于水时亚铁离子不稳定,被氧化为三价铁离子,三价铁离子发生水解生成形成具有净水作用的氢氧化铁胶体,故A错误;B.纳米铁粉具有还原性,可将水中的Cu2+、Hg2+等重金属离子还原为金属单质而除去,FeS可将水体中的Cu2+、Hg2+等重金属离子转化为更难溶的CuS、HgS而除去,其原理不相同,故B正确;C.二氧化硫具有还原性,硫元素化合价+4价升高为+6价,能被酸性高锰酸钾溶液氧化为硫酸,锰元素化合价+7价降低为+2价,由电子守恒和原子守恒得到离子方程式为:5SO2+2MnO4−+2H2O=5SO42−+2Mn2++4H+,可用已知浓度的KMnO4溶液测定食品中SO2残留量,故C正确;D.二氧化硫为酸性氧化物,亚硫酸的酸性大于碳酸,能与碳酸钠溶液反应,可利用碳酸钠溶液吸收燃煤烟气中的SO2,故D正确;答案选A。8.在试管中进行下列实验,现象与实验操作不匹配的是( )选项操作现象结论A向久置的Na2O2粉末中滴加过量盐酸有无色无味气体生成Na2O2没有变质B向NaAlO2溶液中通入足量CO2有白色沉淀生成Al(OH)3不溶于弱酸C室温下,将Cu置于浓硫酸中无现象在浓硫酸中Cu表面形成致密氧化膜阻止进一步反应D向溶液X中先滴加稀硝酸,再滴加BaCl2溶液有白色沉淀生成溶液X中含有Ag+或【答案】B【解析】A.向硫酸铜水溶液中逐滴加入氨水,先生成氢氧化铜沉淀,后与氨水反应生成四氨合铜络离子,则先产生蓝色沉淀,然后溶解,最后得到深蓝色透明溶液,故A正确;B.向碘水中加入CCl4,振荡、静置,由于四氯化碳的密度比水大,下层呈紫红色,故B错误;C.向FeCl3溶液中加入2滴KSCN溶液,发生Fe3++3SCN-=Fe(SCN)3,呈现血红色,故C正确;D.碳酸的酸性比硼酸强,则饱和硼酸溶液中加入Na2CO3溶液,不会产生CO2,因而无现象,故D正确;答案为B。9.下列物质的转化在给定条件下能实现的是( )A.Fe2O3(s)Fe(s)FeCl2(aq)B.Mg(OH)2MgCl2(aq)MgC.Cu2(OH)2CO3CuOCu(OH)2D.NaCl(aq)NaHCO3(s)Na2CO3(s)【答案】A【解析】A.Al和Fe2O3在高温下发生铝热反应生成Fe,Fe和稀盐酸反应生成FeCl2,故A正确;B.用惰性电极电解MgCl2溶液生成Mg(OH)2、H2和Cl2,无Mg生成,故B错误;C.CuO不能溶于水生成Cu(OH)2,故C错误;D.弱酸不能制强酸,则NaCl溶液中通入CO2气体不能发生反应生成NaHCO3,故D错误;故答案为A。10.下列有关物质性质与用途具有对应关系的是A.Al2O3是两性氧化物,可用作耐高温材料B.氯化铁溶液呈酸性,可用于蚀刻铜电路板C.晶体硅熔点高、硬度大,可用于制作半导体材料D.Fe粉具有还原性,可用作食品袋中的抗氧化剂【答案】D【解析】A.氧化铝具有较高熔点,可以用于耐高温材料,与其两性氧化物性质无关,故A错误;B.氯化铁与Cu反应生成氯化亚铁和氯化铜,反应中氯化铁表现氧化性,与溶液的酸性无关,故B错误;C.晶体硅是良好的半导体,用于制作半导体材料,与晶体硅的熔点和硬度无关,故C错误;D.Fe粉具有还原性,易和空气中的氧气反应,可用作食品袋中的抗氧化剂,故D正确;故答案为D。11.下列有关物质性质的叙述不正确的是A.Na2O2与CO2反应生成O2B.铁片投入到冷的浓硫酸中,发生钝化C.NH4Cl溶液中滴加酚酞溶液,溶液变红D.AlCl3溶液中加入足量氨水,生成Al(OH)3【答案】C【解析】A.Na2O2与CO2反应生成O2和碳酸钠,选项A正确;B.铁片投入到冷的浓硫酸中,发生钝化,选项B正确;C.NH4Cl为强酸弱碱盐,水解使溶液呈酸性,滴加酚酞溶液,溶液呈无色,选项C实验操作实验现象A向硫酸铜水溶液中逐滴加入氨水先产生蓝色沉淀,然后溶解,最后得到深蓝色透明溶液B向碘水中加入CCl4,振荡、静置溶液分层,上层为紫红色C向FeCl3溶液中加入2滴KSCN溶液溶液由黄色变为血红色D向饱和硼酸溶液中加入Na2CO3溶液无明显现象
非金属及其化合物
1.下列说法不正确的是
A.[Cu(NH3)4]SO4可通过CuSO4溶液与过量氨水作用得到
B.铁锈的主要成分可表示为Fe2O3·nH2O
C.钙单质可以从TiCl4中置换出Ti
D.可用H2还原MgO制备单质Mg
【答案】D
【解析】A.硫酸铜溶液与氨水反应,当氨水过量时发生反应生成[Cu(NH3)4]SO4,A选项正确;
B.在钢铁发生吸氧腐蚀时生成氢氧化亚铁,总反应为:2Fe+O2+2H2O═2Fe(OH)2,Fe(OH)2被氧化为Fe(OH)3:4Fe(OH)2+O2+2H2O=Fe(OH)3,Fe(OH)3分解即得铁锈:2Fe(OH)3=Fe2O3•nH2O+(3-n)H2O,故所得铁锈的主要成分为Fe2O3•nH2O,,B选项正确;
C.钙还原性较强,钙单质可以从TiCl4中置换出Ti,C选项正确;
D.镁属于较活泼金属,不能利用氢气还原氧化镁制备镁,而是常用电解熔融MgCl2的方法,D选项错误;
答案选D。
2.下列叙述正确的是( )
A.Fe在氯气中燃烧生成FeCl2
B.将AlCl3溶液逐滴滴入到NaOH溶液,先产生白色沉淀,最后沉淀消失
C.电解氯化铝溶液制取金属单质铝
D.常温下,铝制品用浓硫酸或浓硝酸处理过,可耐腐蚀
【答案】D
【解析】A.Fe在氯气中燃烧生成FeCl3,故A错误;
B.将AlCl3溶液逐滴滴入到NaOH溶液,先生成偏铝酸钠,后生成氢氧化铝,涉及反应为AlCl3+4NaOH=NaAlO2+2H2O+3NaCl、AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl,现象为:先不产生沉淀,后沉淀逐渐增多至不变,故B错误;
C.电解熔融状态的氧化铝制取金属单质铝,电解氯化铝溶液生成氢氧化铝、氢气和氯气,故C错误;
D.铝可与浓硫酸、浓硝酸在常温下发生钝化反应。常温下,铝制品用浓硫酸或浓硝酸处理过,表面形成一层致密的氧化膜,可耐腐蚀,故D正确;
故选D。
【点睛】
本题综合考查元素化合物知识,侧重于学生的分析能力和实验能力的考查,学习中注意相关基础知识的积累,难点B,将NaOH溶液逐滴滴入到AlCl3溶液,先产生白色沉淀,最后沉淀消失,注意滴加次序不同,产生的现象不同。
3.下列说法正确的是( )
A.铁制器具表面涂油,可防止其锈蚀
B.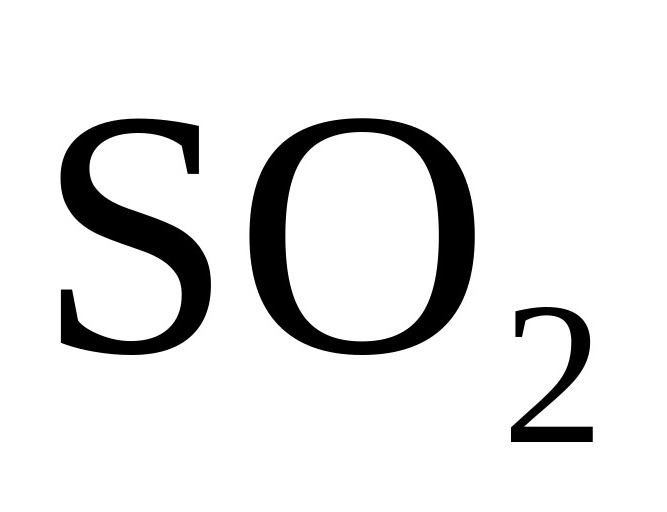 使氯水褪色,证明
使氯水褪色,证明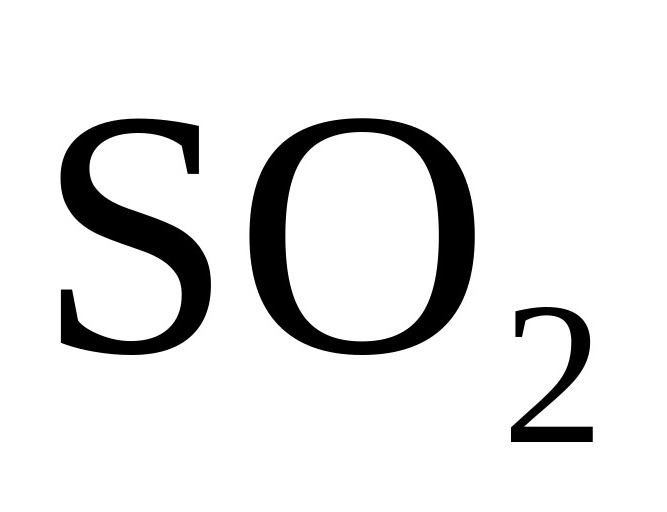 具有漂白性
具有漂白性
C.在空气中蒸干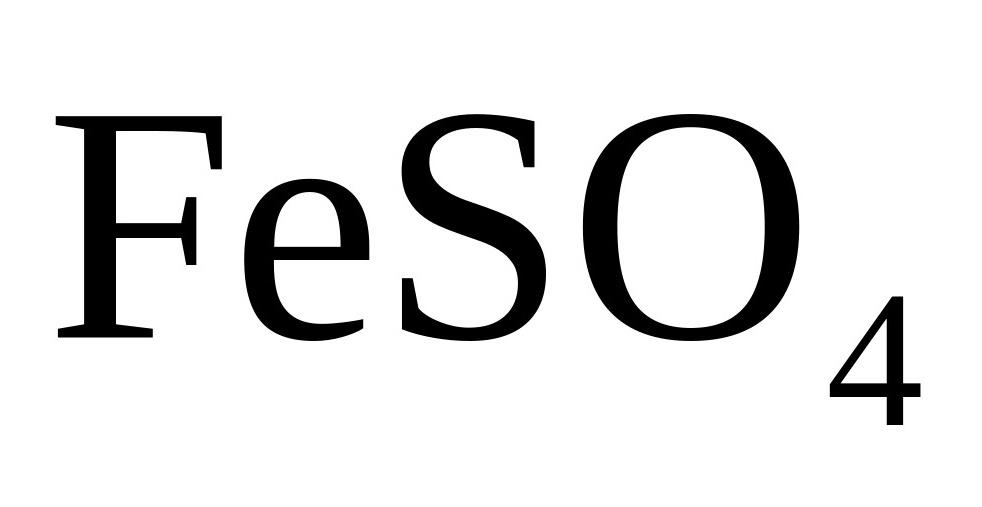 溶液可获得
溶液可获得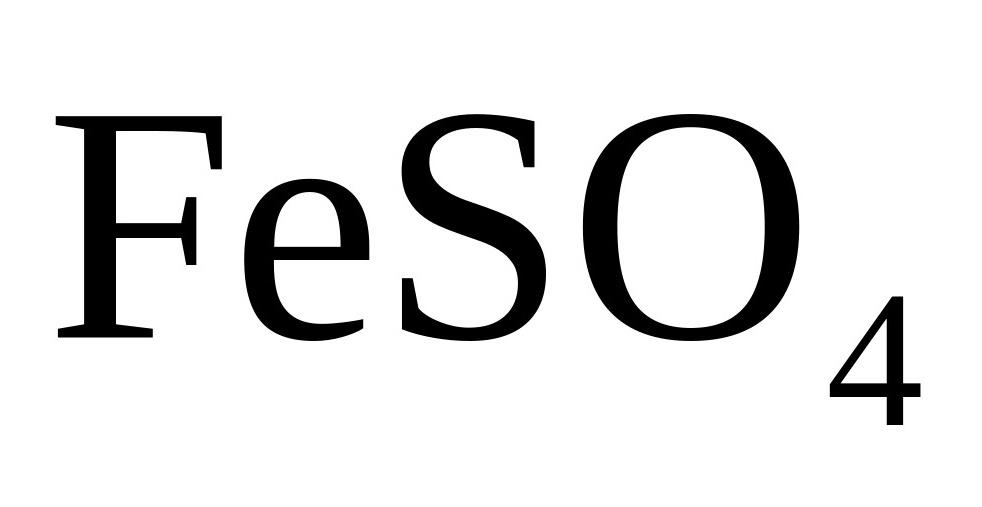 固体
固体
D.浓盐酸敞口放置浓度会降低,说明其具有吸水性
【答案】A
【解析】A.铁制器具表面涂油,可使其与空气隔绝,A项正确;
B.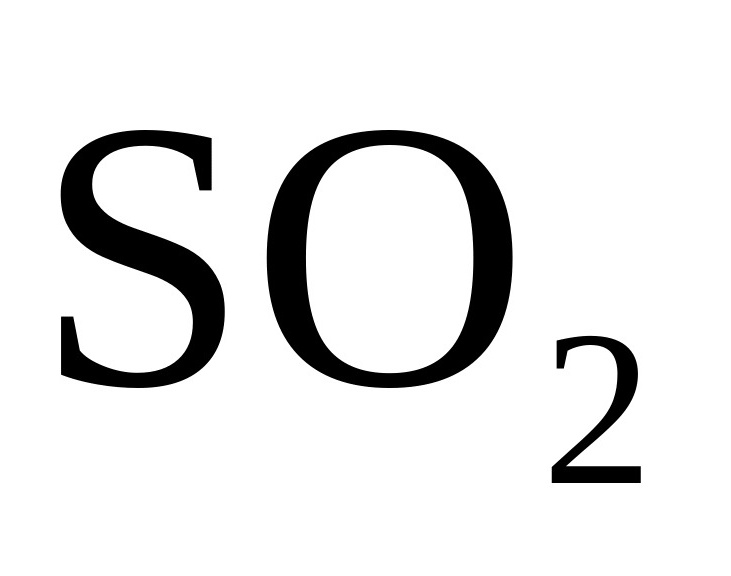 使氯水褪色是
使氯水褪色是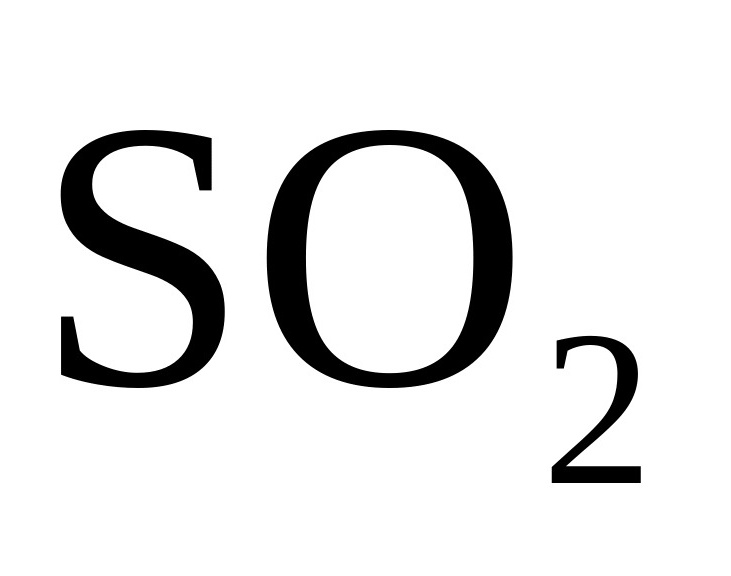 具有强的还原性,B项错误;
具有强的还原性,B项错误;
C.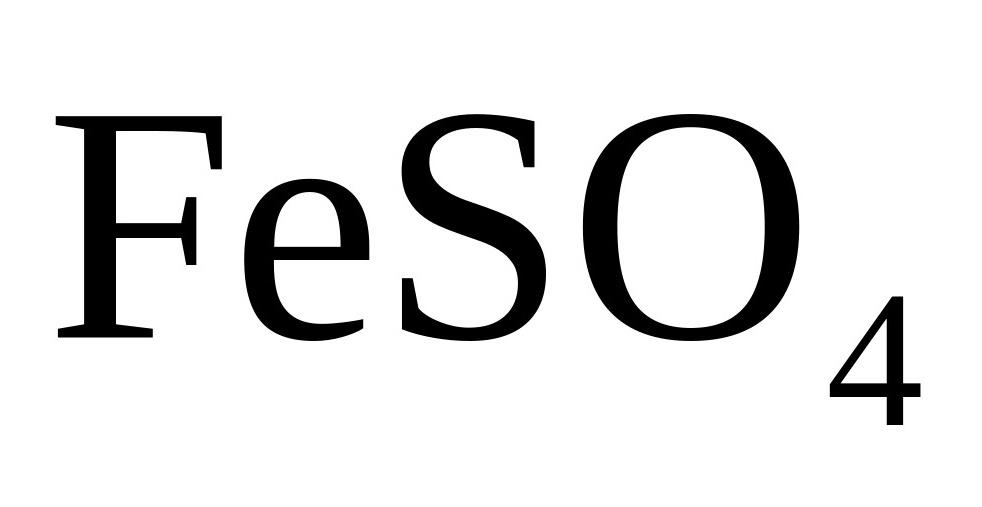 溶液在蒸干过程中与空气接触,被
溶液在蒸干过程中与空气接触,被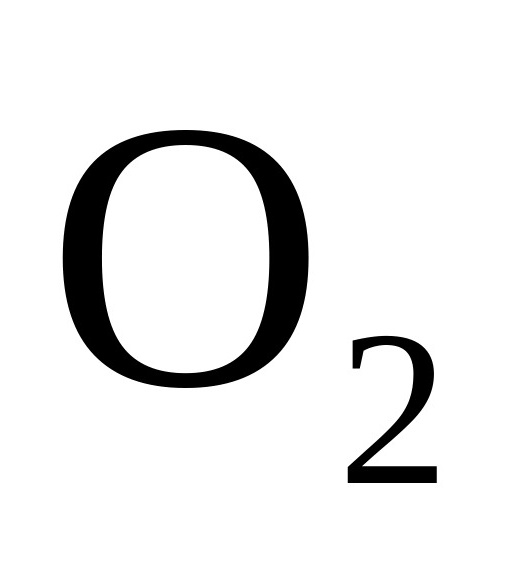 氧化会有
氧化会有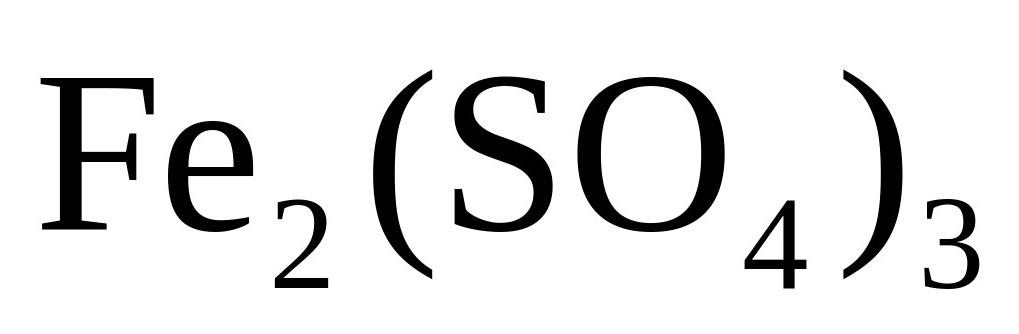 生成,C项错误;
生成,C项错误;
D.浓盐酸长期暴露于空气中浓度降低,是因为其具有挥发性,D项错误;
答案选A。
4.下列有关实验的现象和结论都正确,且二者具有因果关系的是( )
【答案】B
【解析】A.Na2O2久置后会生成Na2CO3,Na2CO3与盐酸反应生成无色无味的CO2,A错误;
B.向偏铝酸钠溶液中通入二氧化碳,生成白色的氢氧化铝,氢氧化铝为两性氢氧化物可溶于强酸或者强碱,但不溶于弱酸弱碱,B正确;
C.Cu在常温下不与浓硫酸反应,C错误;
D.若溶液X中若含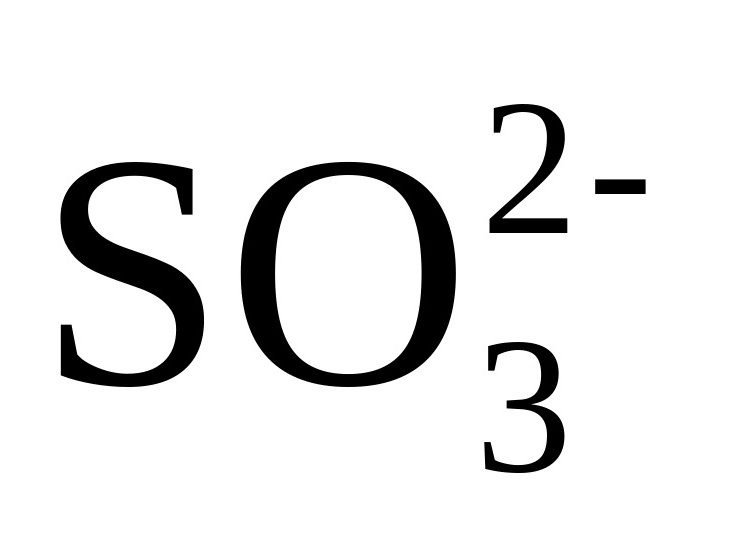 ,滴加稀硝酸时被氧化为
,滴加稀硝酸时被氧化为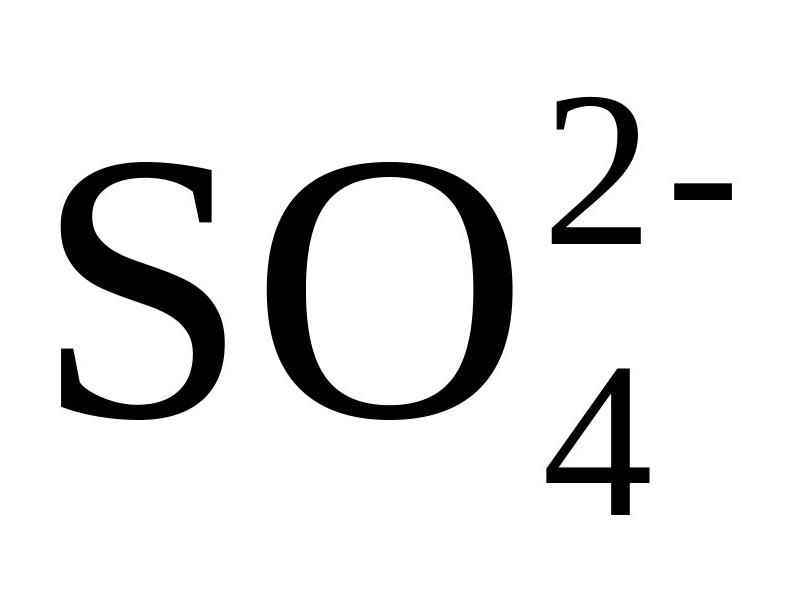 ,再滴加BaCl2溶液时,也有白色沉淀生成,D错误;
,再滴加BaCl2溶液时,也有白色沉淀生成,D错误;
故选B。
5.如图是产生和收集气体的实验装置,该装置适合于( )
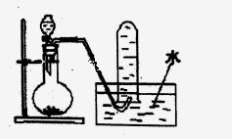
A.用浓硝酸与Cu反应制取NO2
B.用浓盐酸和MnO2反应制取Cl2
C.用H2O2溶液和MnO2反应制取O2
D.用NH4Cl和Ca(OH)2反应制取NH3
【答案】C
【解析】A.铜与浓硝酸反应生成二氧化氮,实验为固体和液体常温下反应生成气体实验,且二氧化氮难溶于水,不能用排水法收集,需用向上排空气法收集,故A错误;
B.用浓盐酸和二氧化锰反应制取氯气需要加热,发生装置错误,氯气可与水反应,不可用排水法收集,需用排饱和食盐水收集,故B错误;
C.用H2O2溶液和MnO2反应制取O2属于固液常温型,氧气难溶于水,可用排水法收集,故C正确;
D.氯化铵和氢氧化钙是固体,反应需要加热,所以反应应该在试管中进行,且试管口略向下倾斜,发生装置错误;氨气极易溶于水,不可用排水法收集,故D错误;
答案选C。
6.下列说法中正确的是
A.Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B.Na2O2与CO2反应生成0.1molO2时转移电子0.4mol
C.向饱和烧碱溶液中加入2gNa2O2充分反应完时,溶液中c(Na+)不变
D.将Na2O2投入CuCl2溶液中有蓝色沉淀及气泡产生
【答案】D
【解析】A.Na2O2遇到湿润的紫色石蕊试纸后,可以和水之间反应生成氢氧化钠和氧气,石蕊试纸变蓝,但是过氧化钠具有漂白性,最终试纸变白色,故A错误;
B.过氧化钠与水反应为歧化反应,过氧化钠既是氧化剂又是还原剂,生成1mol氧气转移2mol电子,则生成0.1 mol氧气转移电子0.2mol,故B错误;
C.Na2O2与水反应时放出大量热,反应后溶液温度升高,导致氢氧化钠溶液的溶解度增大,所以溶液中钠离子浓度增大,故C错误;
D.Na2O2投入到CuCl2溶液中,反应生成氢氧化铜沉淀和氧气,所以有蓝色沉淀及气泡产生,故D正确。
答案选D。
【点睛】
明确过氧化钠的性质为解答关键,注意熟练掌握常见元素及其化合物性质。
7.下列说法不正确的是( )
A.FeSO4常用于制取净水剂,原因是溶于水时形成具有净水作用的氢氧化亚铁胶体
B.纳米铁粉和FeS都可以去除水体中的Cu2+、Hg2+等离子,其原理不相同
C.SO2具有还原性,可用KMnO4溶液测定食品中SO2残留量
D.利用碳酸钠溶液可消除燃煤烟气中的SO2
【答案】A
【解析】A.FeSO4常用于制取净水剂,原因是溶于水时亚铁离子不稳定,被氧化为三价铁离子,三价铁离子发生水解生成形成具有净水作用的氢氧化铁胶体,故A错误;
B.纳米铁粉具有还原性,可将水中的Cu2+、Hg2+等重金属离子还原为金属单质而除去,FeS可将水体中的Cu2+、Hg2+等重金属离子转化为更难溶的CuS、HgS而除去,其原理不相同,故B正确;
C.二氧化硫具有还原性,硫元素化合价+4价升高为+6价,能被酸性高锰酸钾溶液氧化为硫酸,锰元素化合价+7价降低为+2价,由电子守恒和原子守恒得到离子方程式为:5SO2+2MnO4−+2H2O=5SO42−+2Mn2++4H+,可用已知浓度的KMnO4溶液测定食品中SO2残留量,故C正确;
D.二氧化硫为酸性氧化物,亚硫酸的酸性大于碳酸,能与碳酸钠溶液反应,可利用碳酸钠溶液吸收燃煤烟气中的SO2,故D正确;
答案选A。
8.在试管中进行下列实验,现象与实验操作不匹配的是( )
选项 | 操作 | 现象 | 结论 |
A | 向久置的Na2O2粉末中滴加过量盐酸 | 有无色无味气体生成 | Na2O2没有变质 |
B | 向NaAlO2溶液中通入足量CO2 | 有白色沉淀生成 | Al(OH)3不溶于弱酸 |
C | 室温下,将Cu置于浓硫酸中 | 无现象 | 在浓硫酸中Cu表面形成致密氧化膜阻止进一步反应 |
D | 向溶液X中先滴加稀硝酸,再滴加BaCl2溶液 | 有白色沉淀生成 | 溶液X中含有Ag+或 |
【答案】B
【解析】A.向硫酸铜水溶液中逐滴加入氨水,先生成氢氧化铜沉淀,后与氨水反应生成四氨合铜络离子,则先产生蓝色沉淀,然后溶解,最后得到深蓝色透明溶液,故A正确;
B.向碘水中加入CCl4,振荡、静置,由于四氯化碳的密度比水大,下层呈紫红色,故B错误;
C.向FeCl3溶液中加入2滴KSCN溶液,发生Fe3++3SCN-=Fe(SCN)3,呈现血红色,故C正确;
D.碳酸的酸性比硼酸强,则饱和硼酸溶液中加入Na2CO3溶液,不会产生CO2,因而无现象,故D正确;
答案为B。
9.下列物质的转化在给定条件下能实现的是( )
A.Fe2O3(s) Fe(s)
Fe(s)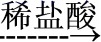 FeCl2(aq)
FeCl2(aq)
B.Mg(OH)2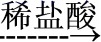 MgCl2(aq)
MgCl2(aq) Mg
Mg
C.Cu2(OH)2CO3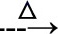 CuO
CuO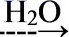 Cu(OH)2
Cu(OH)2
D.NaCl(aq)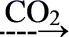 NaHCO3(s)
NaHCO3(s)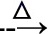 Na2CO3(s)
Na2CO3(s)
【答案】A
【解析】A.Al和Fe2O3在高温下发生铝热反应生成Fe,Fe和稀盐酸反应生成FeCl2,故A正确;
B.用惰性电极电解MgCl2溶液生成Mg(OH)2、H2和Cl2,无Mg生成,故B错误;
C.CuO不能溶于水生成Cu(OH)2,故C错误;
D.弱酸不能制强酸,则NaCl溶液中通入CO2气体不能发生反应生成NaHCO3,故D错误;
故答案为A。
10.下列有关物质性质与用途具有对应关系的是
A.Al2O3是两性氧化物,可用作耐高温材料
B.氯化铁溶液呈酸性,可用于蚀刻铜电路板
C.晶体硅熔点高、硬度大,可用于制作半导体材料
D.Fe粉具有还原性,可用作食品袋中的抗氧化剂
【答案】D
【解析】A.氧化铝具有较高熔点,可以用于耐高温材料,与其两性氧化物性质无关,故A错误;
B.氯化铁与Cu反应生成氯化亚铁和氯化铜,反应中氯化铁表现氧化性,与溶液的酸性无关,故B错误;
C.晶体硅是良好的半导体,用于制作半导体材料,与晶体硅的熔点和硬度无关,故C错误;
D.Fe粉具有还原性,易和空气中的氧气反应,可用作食品袋中的抗氧化剂,故D正确;
故答案为D。
11.下列有关物质性质的叙述不正确的是
A.Na2O2与CO2反应生成O2
B.铁片投入到冷的浓硫酸中,发生钝化
C.NH4Cl溶液中滴加酚酞溶液,溶液变红
D.AlCl3溶液中加入足量氨水,生成Al(OH)3
【答案】C
【解析】A.Na2O2与CO2反应生成O2和碳酸钠,选项A正确;
B.铁片投入到冷的浓硫酸中,发生钝化,选项B正确;
C.NH4Cl为强酸弱碱盐,水解使溶液呈酸性,滴加酚酞溶液,溶液呈无色,选项C
实验操作 | 实验现象 | |
A | 向硫酸铜水溶液中逐滴加入氨水 | 先产生蓝色沉淀,然后溶解,最后得到深蓝色透明溶液 |
B | 向碘水中加入CCl4,振荡、静置 | 溶液分层,上层为紫红色 |
C | 向FeCl3溶液中加入2滴KSCN溶液 | 溶液由黄色变为血红色 |
D | 向饱和硼酸溶液中加入Na2CO3溶液 | 无明显现象 |
题目解答
答案
【答案】C
【解析】【分析】由制备绿矾流程可知,烧渣(主要成分:Fe3O4、Fe2O3和FeO)均溶于硫酸,溶液含Fe2+、Fe3+,步骤②发生FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4,步骤③为蒸发浓缩、冷却结晶析出绿矾,绿矾与氨水、空气可发生氧化还原反应生成Fe(OH)3,以此来解答。
【详解】A.因绿矾的酸根离子为硫酸根离子,则步骤①,最好用硫酸来溶解烧渣,A说法正确;
B.步骤②发生FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4,离子反应为FeS2+14Fe3++8H2O=15Fe2++2SO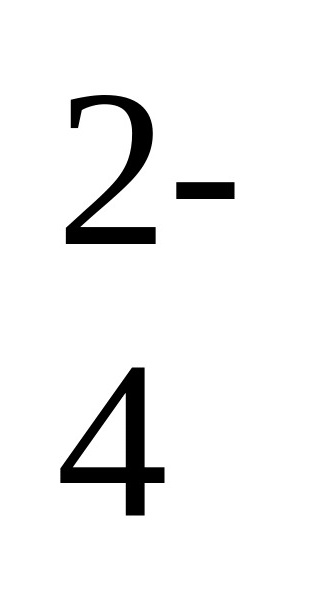 +16H+,B说法正确;
+16H+,B说法正确;
C.步骤③为蒸发浓缩、冷却结晶析出绿矾,若蒸干时绿矾受热失去结晶水,C说法错误;
D.步骤④,反应条件控制不当,绿矾与氨水、空气可发生氧化还原反应生成Fe(OH)3,D说法正确;
答案选C。
【点睛】
把握制备流程中发生的反应、混合物分离方法、实验技能等为解答本题的关键。