题目
反应 (s)+2AgCl(s)=Ca(Cl)_(2)(aq)+2Ag(s), 25℃、101.325kPa下-|||-(Delta )_(1)(H)_(m)(Cd(Cl)_(2))=-389158] cdot mo(l)^-1 (Delta )_(1)(H)_(m)(AgCl)=-126654Jcdot mo(l)^-1, 将此反应构成-|||-原电池的电动势为0.6753V,问:-|||-①上述反应的反应热为 __ ;-|||-②反应在电池中和烧杯中进行时的 Delta (H)_(m) Q各是 __ , __-|||-③使上述反应可逆进行时所做的有用功为 __ 。

题目解答
答案
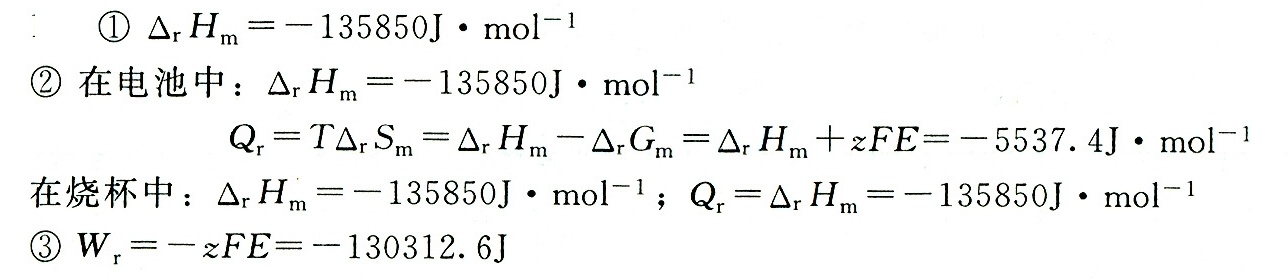
解析
步骤 1:计算反应热
反应热 ${\Delta }_{r}{H}_{m}$ 可以通过反应物和生成物的标准摩尔生成焓的差值来计算。对于反应 $Cd(s)+2AgCl(s)=\!=\!= Cd{Cl}_{2}(aq)+2Ag(s)$,反应热 ${\Delta }_{r}{H}_{m}$ 可以表示为:
${\Delta }_{r}{H}_{m} = {\Delta }_{f}{H}_{m}^{\theta}(CdCl_{2}) - 2{\Delta }_{f}{H}_{m}^{\theta}(AgCl)$
步骤 2:计算电池中和烧杯中进行时的 $\Delta {H}_{m}$ 和 Q
在电池中,反应热 ${\Delta }_{r}{H}_{m}$ 与在烧杯中进行时的反应热相同,但热量 Q 不同。在电池中,热量 Q 为 ${\Delta }_{r}{H}_{m} - T{\Delta }_{r}S_{m}$,其中 T 为温度,${\Delta }_{r}S_{m}$ 为反应的熵变。在烧杯中,热量 Q 等于反应热 ${\Delta }_{r}{H}_{m}$。
步骤 3:计算可逆进行时所做的有用功
可逆进行时所做的有用功 ${W}_{r}$ 可以通过电动势 E 和反应的电子转移数 z 来计算,公式为 ${W}_{r} = -zFE$,其中 F 为法拉第常数。
反应热 ${\Delta }_{r}{H}_{m}$ 可以通过反应物和生成物的标准摩尔生成焓的差值来计算。对于反应 $Cd(s)+2AgCl(s)=\!=\!= Cd{Cl}_{2}(aq)+2Ag(s)$,反应热 ${\Delta }_{r}{H}_{m}$ 可以表示为:
${\Delta }_{r}{H}_{m} = {\Delta }_{f}{H}_{m}^{\theta}(CdCl_{2}) - 2{\Delta }_{f}{H}_{m}^{\theta}(AgCl)$
步骤 2:计算电池中和烧杯中进行时的 $\Delta {H}_{m}$ 和 Q
在电池中,反应热 ${\Delta }_{r}{H}_{m}$ 与在烧杯中进行时的反应热相同,但热量 Q 不同。在电池中,热量 Q 为 ${\Delta }_{r}{H}_{m} - T{\Delta }_{r}S_{m}$,其中 T 为温度,${\Delta }_{r}S_{m}$ 为反应的熵变。在烧杯中,热量 Q 等于反应热 ${\Delta }_{r}{H}_{m}$。
步骤 3:计算可逆进行时所做的有用功
可逆进行时所做的有用功 ${W}_{r}$ 可以通过电动势 E 和反应的电子转移数 z 来计算,公式为 ${W}_{r} = -zFE$,其中 F 为法拉第常数。