题目
选择题:本题包括10 小题,每小题2 分,共计20 分。每小题只有一个选项符合题意。1.CO2是自然界碳循环中的重要物质。下列过程会引起大气中CO2含量上升的是A.光合作用 B.自然降雨 C.化石燃料的燃烧 D.碳酸盐的沉积 2.用化学用语表示 NH3+ HClNH4Cl中的相关微粒,其中正确的是A.中子数为8 的氮原子: B.HCl 的电子式: C.NH3的结构式: D.Cl−的结构示意图: 3.下列有关物质性质与用途具有对应关系的是A.NaHCO3受热易分解,可用于制胃酸中和剂 B.SiO2熔点高硬度大,可用于制光导纤维 C.Al2O3是两性氧化物,可用作耐高温材料 D.CaO能与水反应,可用作食品干燥剂 4.室温下,下列各组离子在指定溶液中能大量共存的是A.0. 1 mol·L−1KI 溶液:Na+、K+、ClO− 、OH− B.0. 1 mol·L−1Fe2(SO4)3溶液:Cu2+、NH4+ 、NO3−、SO42− C.0. 1 mol·L−1HCl 溶液:Ba2+、K+、CH3COO−、NO3− D.0. 1 mol·L−1NaOH溶液:Mg2+、Na+、SO42−、HCO3− 5.下列有关从海带中提取碘的实验原理和装置能达到实验目的的是A.用装置甲灼烧碎海带 B.用装置乙过滤海带灰的浸泡液 C.用装置丙制备用于氧化浸泡液中I−的Cl2 D.用装置丁吸收氧化浸泡液中I−后的Cl2尾气 6.下列有关物质性质的叙述一定不正确的是A.向FeCl2溶液中滴加NH4SCN溶液,溶液显红色 B.KAl(SO4) 2·12H2O溶于水可形成 Al(OH)3胶体 C.NH4Cl与Ca(OH)2混合加热可生成NH3 D.Cu与FeCl3溶液反应可生成CuCl2 7. 下列指定反应的离子方程式正确的是A.饱和Na2CO3溶液与CaSO4固体反应:CO32−+CaSO4 B.酸化NaIO3和NaI的混合溶液:I− +IO3−+6H+ C.KClO碱性溶液与Fe(OH)3反应:3ClO−+2Fe(OH)3 D.电解饱和食盐水:2Cl−+2H+ 8.短周期主族元素 X、Y、Z、W 原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主族。下列说法正确的是A.原子半径: B.由X、Y 组成的化合物中均不含共价键 C.Y 的最高价氧化物的水化物的碱性比Z的弱 D.X 的简单气态氢化物的热稳定性比W的强 9.在给定条件下,下列选项所示的物质间转化均能实现的是A. B. C. D. 10.下列说法正确的是A.氢氧燃料电池放电时化学能全部转化为电能 B.反应4Fe(s)+3O2(g) C.3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023 D.在酶催化淀粉水解反应中,温度越高淀粉水解速率越快 11.化合物Y 能用于高性能光学树脂的合成,可由化合物X与2 −甲基丙烯酰氯在一定条件下反应制得:下列有关化合物X、Y 的说法正确的是A.X 分子中所有原子一定在同一平面上 B.Y与Br2的加成产物分子中含有手性碳原子 C.X、Y均不能使酸性KMnO4溶液褪色 D.X→Y的反应为取代反应 12.根据下列实验操作和现象所得出的结论正确的是A. B. C. D. 13.根据下列图示所得出的结论不正确的是A.图甲是CO(g)+H2O(g) B.图乙是室温下H2O2催化分解放出氧气的反应中 C.图丙是室温下用0.1000 mol·L−1NaOH溶液滴定20.00 mL 0.1000 mol·L−1某一元酸HX的滴定曲线,说明HX是一元强酸 D.图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中 14.H2C2O4为二元弱酸,Ka1 (H2C2O4 ) =5.4×10−2,Ka2 (H2C2O4 ) =5.4×10−5,设H2C2O4溶液中c(总)=c(H2C2O4) +c(HC2O4−) +c(C2O42−)。室温下用NaOH溶液滴定25.00 mL 0.1000 mol·L−1H2C2O4溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是A.0.1000 mol·L−1 H2C2O4溶液: B.c C.pH = 7的溶液: D.c 15.一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g)2SO3(g)(正反应放热),测得反应的相关数据如下:下列说法正确的是A.v B.K C.v D.c
选择题:本题包括10 小题,每小题2 分,共计20 分。每小题只有一个选项符合题意。
1.CO2是自然界碳循环中的重要物质。下列过程会引起大气中CO2含量上升的是
A.光合作用 B.自然降雨 C.化石燃料的燃烧 D.碳酸盐的沉积
2.用化学用语表示 NH3+ HCl![]()
![]()
 NH4Cl中的相关微粒,其中正确的是
NH4Cl中的相关微粒,其中正确的是
 NH4Cl中的相关微粒,其中正确的是
NH4Cl中的相关微粒,其中正确的是A.中子数为8 的氮原子: B.HCl 的电子式: C.NH3的结构式: D.Cl−的结构示意图:
3.下列有关物质性质与用途具有对应关系的是
A.NaHCO3受热易分解,可用于制胃酸中和剂 B.SiO2熔点高硬度大,可用于制光导纤维 C.Al2O3是两性氧化物,可用作耐高温材料 D.CaO能与水反应,可用作食品干燥剂
4.室温下,下列各组离子在指定溶液中能大量共存的是
A.0. 1 mol·L−1KI 溶液:Na+、K+、ClO− 、OH− B.0. 1 mol·L−1Fe2(SO4)3溶液:Cu2+、NH4+ 、NO3−、SO42− C.0. 1 mol·L−1HCl 溶液:Ba2+、K+、CH3COO−、NO3− D.0. 1 mol·L−1NaOH溶液:Mg2+、Na+、SO42−、HCO3−
5.下列有关从海带中提取碘的实验原理和装置能达到实验目的的是![]()
![]()
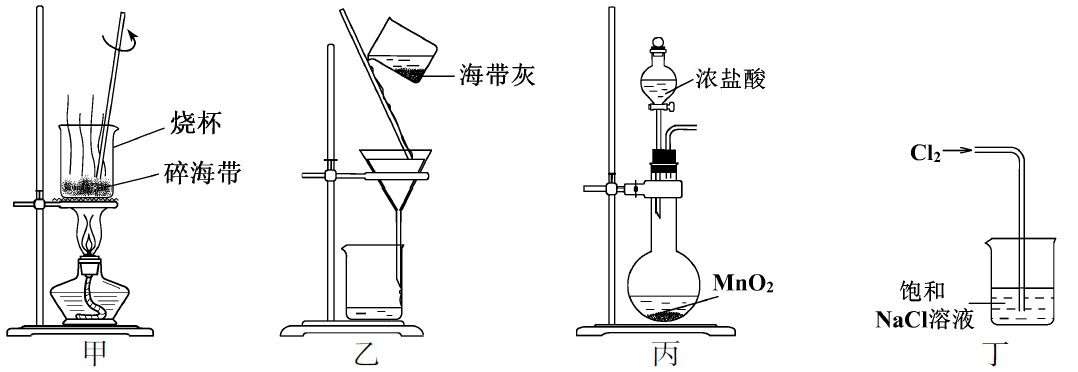

A.用装置甲灼烧碎海带 B.用装置乙过滤海带灰的浸泡液 C.用装置丙制备用于氧化浸泡液中I−的Cl2 D.用装置丁吸收氧化浸泡液中I−后的Cl2尾气
6.下列有关物质性质的叙述一定不正确的是
A.向FeCl2溶液中滴加NH4SCN溶液,溶液显红色 B.KAl(SO4) 2·12H2O溶于水可形成 Al(OH)3胶体 C.NH4Cl与Ca(OH)2混合加热可生成NH3 D.Cu与FeCl3溶液反应可生成CuCl2
7. 下列指定反应的离子方程式正确的是
A.饱和Na2CO3溶液与CaSO4固体反应:CO32−+CaSO4 B.酸化NaIO3和NaI的混合溶液:I− +IO3−+6H+ C.KClO碱性溶液与Fe(OH)3反应:3ClO−+2Fe(OH)3 D.电解饱和食盐水:2Cl−+2H+
8.短周期主族元素 X、Y、Z、W 原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主族。下列说法正确的是
A.原子半径: B.由X、Y 组成的化合物中均不含共价键 C.Y 的最高价氧化物的水化物的碱性比Z的弱 D.X 的简单气态氢化物的热稳定性比W的强
9.在给定条件下,下列选项所示的物质间转化均能实现的是![]()
![]()

![]()
![]()
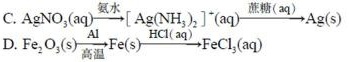

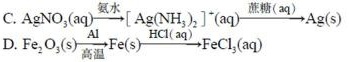
A. B. C. D.
10.下列说法正确的是
A.氢氧燃料电池放电时化学能全部转化为电能 B.反应4Fe(s)+3O2(g) C.3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023 D.在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
11.化合物Y 能用于高性能光学树脂的合成,可由化合物X与2 −甲基丙烯酰氯在一定条件下反应制得:![]()
![]()
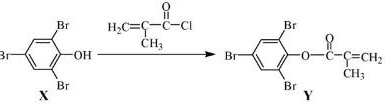

下列有关化合物X、Y 的说法正确的是
A.X 分子中所有原子一定在同一平面上 B.Y与Br2的加成产物分子中含有手性碳原子 C.X、Y均不能使酸性KMnO4溶液褪色 D.X→Y的反应为取代反应
12.根据下列实验操作和现象所得出的结论正确的是![]()
![]()
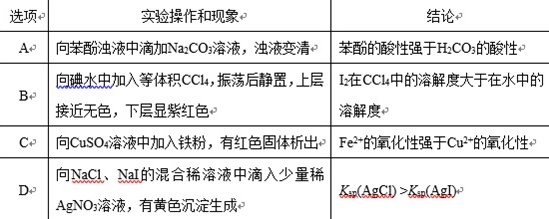

A. B. C. D.
13.根据下列图示所得出的结论不正确的是![]()
![]()
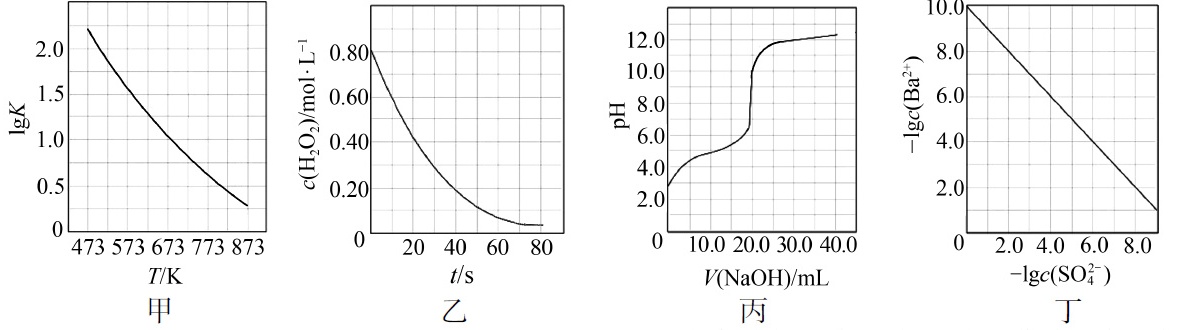

A.图甲是CO(g)+H2O(g) B.图乙是室温下H2O2催化分解放出氧气的反应中 C.图丙是室温下用0.1000 mol·L−1NaOH溶液滴定20.00 mL 0.1000 mol·L−1某一元酸HX的滴定曲线,说明HX是一元强酸 D.图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中
14.H2C2O4为二元弱酸,Ka1 (H2C2O4 ) =5.4×10−2,Ka2 (H2C2O4 ) =5.4×10−5,设H2C2O4溶液中c(总)=c(H2C2O4) +c(HC2O4−) +c(C2O42−)。室温下用NaOH溶液滴定25.00 mL 0.1000 mol·L−1H2C2O4溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是
A.0.1000 mol·L−1 H2C2O4溶液: B.c C.pH = 7的溶液: D.c
15.一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g)![]()
![]()
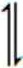 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:![]()
![]()
![]() 下列说法正确的是
下列说法正确的是![]()

 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:

A.v B.K C.v D.c
题目解答
答案
CCDBBAADACBDBCADCD