题目
液体A和B可以形成理想的液态混合物。在320 K时,将3 mol A和1 mol B混合形成液态混合物I,总蒸气压为5.33×104 Pa。再加入2 mol B 形成理想液态混合物II,总蒸气压为 6.13×104 Pa。试计算:(1)未混合前纯液体A和B的饱和蒸气压°和°。(2) 与理想液态混合物I达平衡的气相组成°。(3) 在形成理想液态混合物I的过程中,Gibbs自由能的变化值°。(4) 若在理想液态混合物II中再加入3 mol B,形成理想液态混合物Ⅲ的蒸气压。
液体A和B可以形成理想的液态混合物。在320 K时,将3 mol A和1 mol B混合形成液态混合物I,总蒸气压为5.33×104 Pa。再加入2 mol B 形成理想液态混合物II,总蒸气压为 6.13×104 Pa。试计算:
(1)未混合前纯液体A和B的饱和蒸气压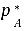 和
和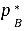 。
。
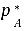 和
和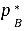 。
。(2) 与理想液态混合物I达平衡的气相组成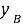 。
。
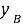 。
。(3) 在形成理想液态混合物I的过程中,Gibbs自由能的变化值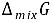 。
。
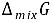 。
。(4) 若在理想液态混合物II中再加入3 mol B,形成理想液态混合物Ⅲ的蒸气压。
题目解答
答案
解:(1) 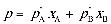
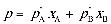
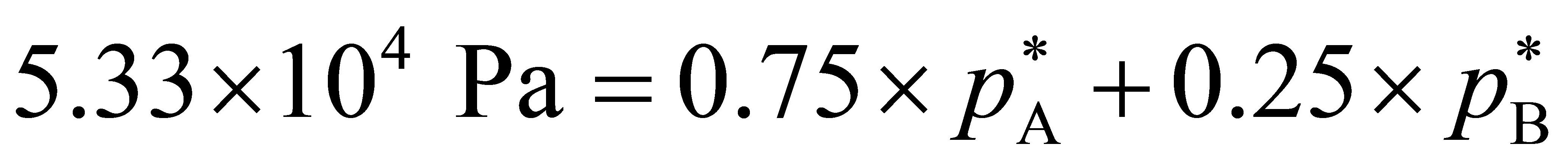 (a)
(a)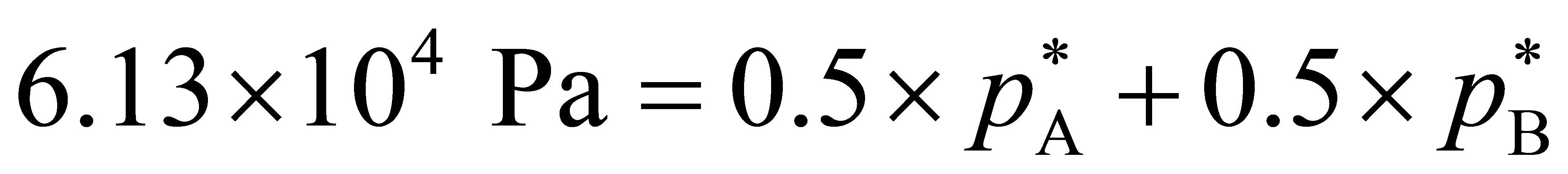 (b)
(b)将(a)式与 (b) 式联立,解得:

(2) 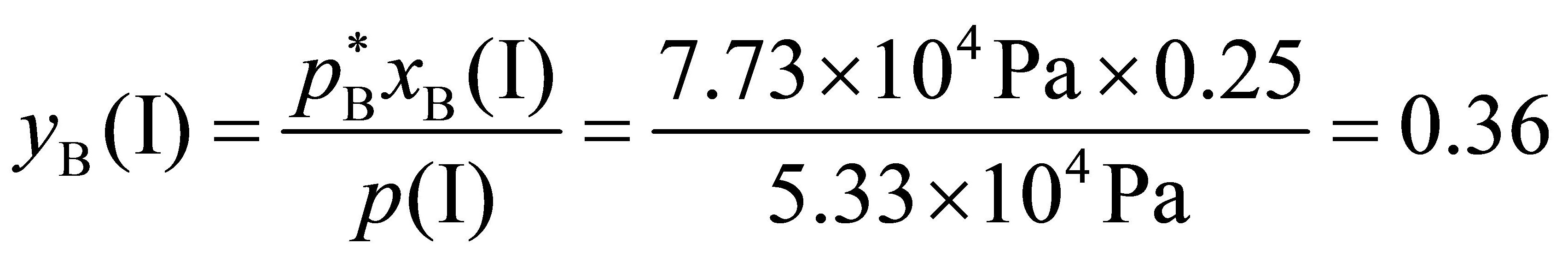
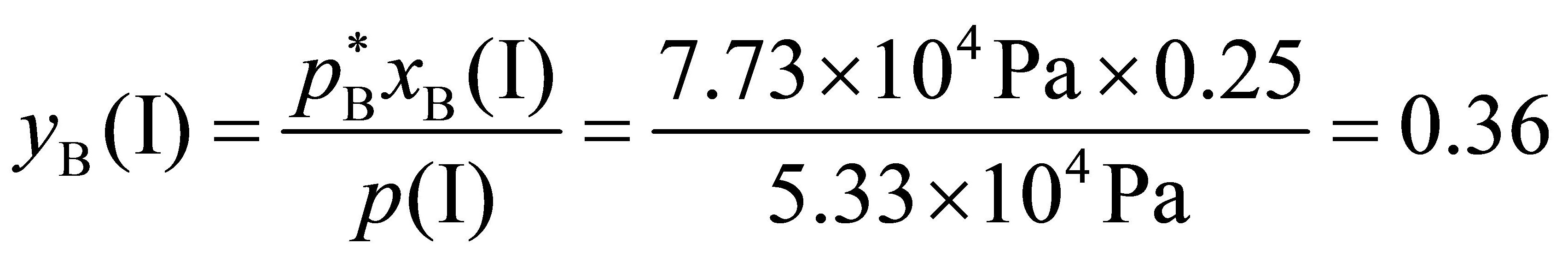
(3) 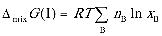
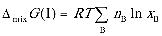
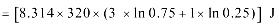
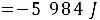
(4) 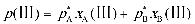
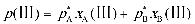
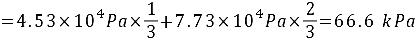
解析
步骤 1:计算纯液体A和B的饱和蒸气压
根据理想液态混合物的蒸气压公式,总蒸气压等于各组分的摩尔分数乘以各自的饱和蒸气压之和。对于混合物I和II,可以列出两个方程,联立求解纯液体A和B的饱和蒸气压。
步骤 2:计算与理想液态混合物I达平衡的气相组成yB
根据道尔顿分压定律,气相中各组分的分压等于其在液相中的摩尔分数乘以总蒸气压。由此可以计算出气相中B的摩尔分数yB。
步骤 3:计算形成理想液态混合物I的过程中Gibbs自由能的变化值$\Delta mix$
根据理想液态混合物的Gibbs自由能变化公式,可以计算出形成混合物I时的Gibbs自由能变化值。
步骤 4:计算理想液态混合物III的蒸气压
根据理想液态混合物的蒸气压公式,可以计算出加入3 mol B后形成的理想液态混合物III的蒸气压。
根据理想液态混合物的蒸气压公式,总蒸气压等于各组分的摩尔分数乘以各自的饱和蒸气压之和。对于混合物I和II,可以列出两个方程,联立求解纯液体A和B的饱和蒸气压。
步骤 2:计算与理想液态混合物I达平衡的气相组成yB
根据道尔顿分压定律,气相中各组分的分压等于其在液相中的摩尔分数乘以总蒸气压。由此可以计算出气相中B的摩尔分数yB。
步骤 3:计算形成理想液态混合物I的过程中Gibbs自由能的变化值$\Delta mix$
根据理想液态混合物的Gibbs自由能变化公式,可以计算出形成混合物I时的Gibbs自由能变化值。
步骤 4:计算理想液态混合物III的蒸气压
根据理想液态混合物的蒸气压公式,可以计算出加入3 mol B后形成的理想液态混合物III的蒸气压。