题目
295k时,纯水中((H)^+)=(10)^-7molcdot (L)^-1-|||-__,溶液呈中性,温度升高时,纯水的pH为( )A.大于7B.小于7C.等于7D.无法确定
295k时,纯水中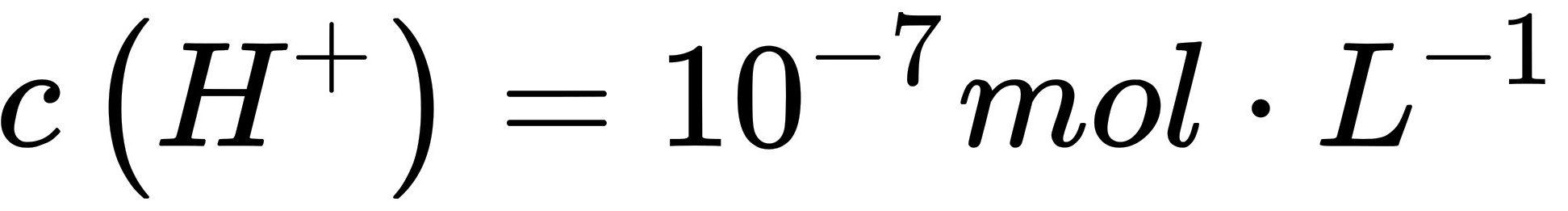 ,溶液呈中性,温度升高时,纯水的pH为( )
,溶液呈中性,温度升高时,纯水的pH为( )
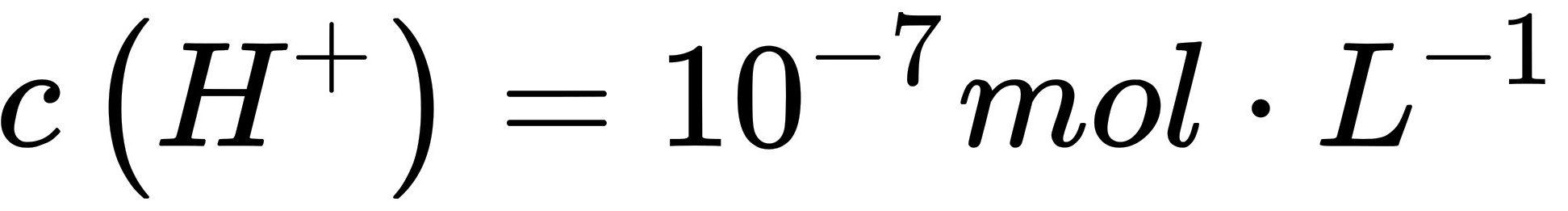 ,溶液呈中性,温度升高时,纯水的pH为( )
,溶液呈中性,温度升高时,纯水的pH为( )- A.大于7
- B.小于7
- C.等于7
- D.无法确定
题目解答
答案
B. 小于7
解析
考查要点:本题主要考查温度对水的电离平衡的影响及pH值变化的理解。
解题核心思路:
- 水的电离平衡:水的电离是吸热反应(H₂O ⇌ H⁺ + OH⁻),温度升高会促进电离平衡向右移动。
- pH的定义:pH = -log[H⁺],当温度升高时,H⁺浓度增大,导致pH减小。
- 中性溶液的性质:纯水中[H⁺] = [OH⁻],但pH是否等于7取决于温度(仅在25℃时成立)。
破题关键点:
- 温度升高时,水的电离度增大,H⁺和OH⁻浓度均增大,但溶液仍保持中性([H⁺] = [OH⁻])。
- pH值由H⁺浓度决定,因此温度升高会导致pH < 7。
温度对水的电离影响:
- 电离平衡移动:温度升高,水的电离平衡右移,H⁺和OH⁻的浓度均增大。
- 中性条件下的pH变化:
- 原题中295K时,纯水pH = 7([H⁺] = 10⁻⁷ mol/L)。
- 温度升高后,假设新的[H⁺] = [OH⁻] = 10⁻⁶.5 mol/L,则pH = -log(10⁻⁶.5) = 6.5 < 7。
- 结论:温度升高时,纯水的pH会小于7。