题目
某学习小组在实验室制备SO_(2)并探究其性质,将铜丝插入热浓硫酸中进行如图所示的探究活动(asim d均为浸有相应试液的棉花)。(1)该实验装置的优点是______(至少写两点)。(2)具支试管中发生反应的化学方程式为______。晶红 浓NaOH-|||-d-|||-a-|||-紫色 酸性 安全-|||-石蕊 KMnO4 气球(3)a处的实验现象是______,说明SO_(2)的水溶液具有______性。(4)说明SO_(2)具有还原性的实验现象是______。(5)d处发生反应的离子方程式为______。(6)关于b处品红褪色的原因,一般认为是由于SO_(2)与品红生成了不稳定的无色物质。请设计实验证明:______。
某学习小组在实验室制备$SO_{2}$并探究其性质,将铜丝插入热浓硫酸中进行如图所示的探究活动$(a\sim d$均为浸有相应试液的棉花)。
$(1)$该实验装置的优点是______$(至少写两点)$。
$(2)$具支试管中发生反应的化学方程式为______。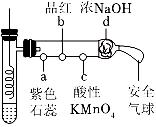
$(3)a$处的实验现象是______,说明$SO_{2}$的水溶液具有______性。
$(4)$说明$SO_{2}$具有还原性的实验现象是______。
$(5)d$处发生反应的离子方程式为______。
$(6)$关于$b$处品红褪色的原因,一般认为是由于$SO_{2}$与品红生成了不稳定的无色物质。请设计实验证明:______。
$(1)$该实验装置的优点是______$(至少写两点)$。
$(2)$具支试管中发生反应的化学方程式为______。

$(3)a$处的实验现象是______,说明$SO_{2}$的水溶液具有______性。
$(4)$说明$SO_{2}$具有还原性的实验现象是______。
$(5)d$处发生反应的离子方程式为______。
$(6)$关于$b$处品红褪色的原因,一般认为是由于$SO_{2}$与品红生成了不稳定的无色物质。请设计实验证明:______。
题目解答
答案
(1)上下移动铜丝可使铜丝伸入和离开浓硫酸液面,控制反应的开始和终止,整个反应在密闭装置进行,药品用量少,并且可防止$SO_{2}$逸出,污染空气,
故答案为:可以控制反应的开始和终止;节省药品并且环保;
$(2)Cu$与浓硫酸反应生成硫酸铜、二氧化硫和水,反应方程式为$Cu+2H_{2}SO_{4}($浓)$\frac{\underline{\;\;△\;\;}}{\;}CuSO_{4}+2H_{2}O+SO_{2}\uparrow $,
故答案为:$Cu+2H_{2}SO_{4}($浓)$\frac{\underline{\;\;△\;\;}}{\;}CuSO_{4}+2H_{2}O+SO_{2}\uparrow $;
$(3)SO_{2}$是酸性氧化物,其水溶液呈酸性,能使石蕊溶液变红色,所以$a$处的实验现象是紫色石䓌变红,
故答案为:紫色石䓌变红;酸;
$(4)SO_{2}$能还原酸性高锰酸钾而使之褪色,即$c$处红色酸性高锰酸钾褪色,可证明$SO_{2}$具有还原性,
故答案为:$c$处红色酸性高锰酸钾褪色;
$(5)SO_{2}$是酸性氧化物,能与$NaOH$溶液反应生成$Na_{2}SO_{3}$或$NaHSO_{3}$,离子方程式为$SO_{2}+2OH^{-}={SO}_{3}^{2-}+H_{2}O$或$SO_{2}+OH^{-}={HSO}_{3}^{-}$,
故答案为:$SO_{2}+2OH^{-}={SO}_{3}^{2-}+H_{2}O$或$SO_{2}+OH^{-}={HSO}_{3}^{-}$;
$(6)$一般而言,品红褪色的原因是$SO_{2}$与品红生成了不稳定的无色物质,该不稳定的无色物质在加热条件下易分解而使溶液恢复为红色,所以实验方案为品红褪色后,用燃着的酒精灯加热,品红恢复为红色,
故答案为:品红褪色后,用燃着的酒精灯加热,品红恢复为红色。
故答案为:可以控制反应的开始和终止;节省药品并且环保;
$(2)Cu$与浓硫酸反应生成硫酸铜、二氧化硫和水,反应方程式为$Cu+2H_{2}SO_{4}($浓)$\frac{\underline{\;\;△\;\;}}{\;}CuSO_{4}+2H_{2}O+SO_{2}\uparrow $,
故答案为:$Cu+2H_{2}SO_{4}($浓)$\frac{\underline{\;\;△\;\;}}{\;}CuSO_{4}+2H_{2}O+SO_{2}\uparrow $;
$(3)SO_{2}$是酸性氧化物,其水溶液呈酸性,能使石蕊溶液变红色,所以$a$处的实验现象是紫色石䓌变红,
故答案为:紫色石䓌变红;酸;
$(4)SO_{2}$能还原酸性高锰酸钾而使之褪色,即$c$处红色酸性高锰酸钾褪色,可证明$SO_{2}$具有还原性,
故答案为:$c$处红色酸性高锰酸钾褪色;
$(5)SO_{2}$是酸性氧化物,能与$NaOH$溶液反应生成$Na_{2}SO_{3}$或$NaHSO_{3}$,离子方程式为$SO_{2}+2OH^{-}={SO}_{3}^{2-}+H_{2}O$或$SO_{2}+OH^{-}={HSO}_{3}^{-}$,
故答案为:$SO_{2}+2OH^{-}={SO}_{3}^{2-}+H_{2}O$或$SO_{2}+OH^{-}={HSO}_{3}^{-}$;
$(6)$一般而言,品红褪色的原因是$SO_{2}$与品红生成了不稳定的无色物质,该不稳定的无色物质在加热条件下易分解而使溶液恢复为红色,所以实验方案为品红褪色后,用燃着的酒精灯加热,品红恢复为红色,
故答案为:品红褪色后,用燃着的酒精灯加热,品红恢复为红色。
解析
- 实验装置优点:需结合装置特点分析,如反应控制、环保、药品节约等。
- 反应方程式:明确浓硫酸与铜在加热条件下的反应类型及产物。
- SO₂酸性:通过石蕊试纸变色判断SO₂水溶液的酸性。
- SO₂还原性:需识别强氧化剂(如酸性高锰酸钾)与SO₂反应的现象。
- 离子方程式:SO₂与强碱反应的产物需考虑溶液酸碱性。
- 实验设计:通过加热褪色后的品红溶液验证是否可逆。
第(1)题
反应控制
装置通过上下移动铜丝实现反应的启停,避免过量反应。
节约环保
密闭设计减少药品用量,防止SO₂逸出污染空气。
第(2)题
反应条件
浓硫酸与铜需在加热(△)条件下反应。
产物分析
生成CuSO₄、SO₂和H₂O,方程式需配平并标注气体符号。
第(3)题
现象分析
SO₂溶于水生成H₂SO₃,溶液显酸性,使紫色石蕊变红。
性质判断
酸性对应酸性氧化物的通性。
第(4)题
反应原理
酸性条件下,KMnO₄将SO₂氧化为SO₄²⁻,自身被还原为Mn²⁺。
关键现象
c处红色褪去直接证明SO₂的还原性。
第(5)题
反应类型
SO₂与强碱反应生成亚硫酸盐或酸式盐,需分步书写离子方程式。
第(6)题
实验设计逻辑
若褪色是可逆反应,加热后品红应恢复红色。需通过加热处理验证。