题目
[题目]-|||-在化学分析中,为了测定某试样中FeS O4·7H2O的质量分-|||-数,一般采用在酸性条件下用高锰酸钾标准溶液滴定的方-|||-法,反应原理为: (Fe)^2++8(H)^++Mn(O)_(4)^-=!=!= 5(Fe)^3++Mn-|||-+4(H)_(2)(O)_(0) 高锰酸钾标准溶液可用性质稳定、相对分子-|||-质量较大的基准物质草酸钠 _(r)((Na)_(2)(C)_(2)(O)_(4))=134.01 进行标-|||-定,反应原理为: (C)_(2)({O)_(4)}^2-+2Na(O)_(4)+16(H)^+=10CO-|||-+2(Mn)^2++8(H)_(2)(O)_(0)-|||-实验步骤如下:-|||-步骤一:先粗配浓度约为 https:/img.zuoyebang.cc/zyb_eae335a7f46dd674727d8edb50199b8c.jpg.5times (10)^-2molcdot (L)^-1 的高锰酸钾溶液-|||-500mL。-|||-步骤二:称取Na 2C2O4固体mg放入锥形瓶中,用蒸馏水-|||-溶解并加稀硫酸酸化,加热至 backsim (80)^circ C, 用(1)所配高锰酸-|||-钾溶液进行滴定,从而可标定高锰酸钾溶液的浓度。经测-|||-定, (km({O)_(4)})=0.0160molcdot (L)^-1-|||-步骤三:称取FeS O4·7H2O试样1.073g,放入锥形瓶中,-|||-加入适量的水溶解,-|||-步骤四:用标准高锰酸钾溶液滴定步骤三所配样品溶液,-|||-达到终点时消耗标准溶液48.00mL。-|||-试回答下列问题:-|||-(1)步骤一中要用到的玻璃仪器是烧杯、 __-|||-__ __-|||-(2)步骤二中需要对m的大致值进行预估,你预估的依据-|||-是 __-|||-__-|||-(3)本实验中操作滴定管的以下图示,正确的是 __-|||-(填编号)。-|||-A 3 c-|||-(4)步骤二的滴定是在一定温度下进行的,操作过程中发现-|||-前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶-|||-段褪色又变慢。试根据影响化学反应速率的条件分析,溶-|||-液褪色明显变快的原因可能是 __-|||-(5)请在下面空白处设计步骤四中的数据记录和数据处理表-|||-格(不必填数据)。-|||-(6)国家标准规定Fe SO4·7H2O的含量(w):一级品100.5%-|||-geqslant u 99.50% ;二级品 .5% geqslant u 199.00% ;三级品-|||-.0% geqslant ugeqslant 98.00% 试判断该试样符合国家 __ 级-|||-品标准。-|||-(7)测定试样中FeS O4·7H2O的含量时,有时测定值会超过-|||-100%,其原因可能是 __-|||-__-|||-__

题目解答
答案
解析
步骤 1:步骤一中要用到的玻璃仪器
步骤一中粗配高锰酸钾溶液,需要使用烧杯和玻璃棒进行溶解和搅拌,量筒用于量取溶液体积,容量瓶用于定容。
步骤 2:步骤二中需要对m的大致值进行预估
步骤二中,需要根据反应的定量关系、滴定管的规格(最大容量)及高锰酸钾溶液的粗浓度来确定草酸钠的质量。一般比计算值低一些。
步骤 3:本实验中操作滴定管的正确图示
滴定管操作时,左手控制活塞,右手摇动锥形瓶,眼睛观察锥形瓶内溶液颜色变化,故A正确。
步骤 4:步骤二的滴定过程中溶液褪色明显变快的原因
反应过程中生成的 ${Mn}^{2+}$ 为催化剂,使反应速率变大。
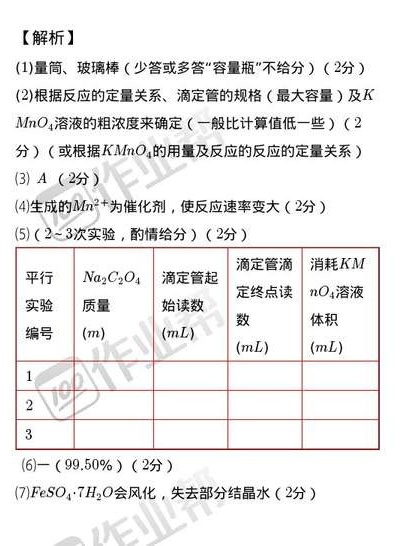
步骤 5:设计步骤四中的数据记录和数据处理表格
设计表格时,需要记录滴定管的起始读数、终点读数、消耗高锰酸钾溶液的体积、平行实验的次数等。
步骤 6:判断该试样符合国家哪级品标准
根据步骤四中消耗高锰酸钾溶液的体积,计算出FeSO4·7H2O的含量,然后与国家标准进行比较,判断该试样符合国家哪级品标准。
步骤 7:测定试样中FeSO4·7H2O的含量时,有时测定值会超过100%的原因
测定试样中FeSO4·7H2O的含量时,有时测定值会超过100%,其原因可能是FeSO4·7H2O会风化,失去部分结晶水。
步骤一中粗配高锰酸钾溶液,需要使用烧杯和玻璃棒进行溶解和搅拌,量筒用于量取溶液体积,容量瓶用于定容。
步骤 2:步骤二中需要对m的大致值进行预估
步骤二中,需要根据反应的定量关系、滴定管的规格(最大容量)及高锰酸钾溶液的粗浓度来确定草酸钠的质量。一般比计算值低一些。
步骤 3:本实验中操作滴定管的正确图示
滴定管操作时,左手控制活塞,右手摇动锥形瓶,眼睛观察锥形瓶内溶液颜色变化,故A正确。
步骤 4:步骤二的滴定过程中溶液褪色明显变快的原因
反应过程中生成的 ${Mn}^{2+}$ 为催化剂,使反应速率变大。
步骤 5:设计步骤四中的数据记录和数据处理表格
设计表格时,需要记录滴定管的起始读数、终点读数、消耗高锰酸钾溶液的体积、平行实验的次数等。
步骤 6:判断该试样符合国家哪级品标准
根据步骤四中消耗高锰酸钾溶液的体积,计算出FeSO4·7H2O的含量,然后与国家标准进行比较,判断该试样符合国家哪级品标准。
步骤 7:测定试样中FeSO4·7H2O的含量时,有时测定值会超过100%的原因
测定试样中FeSO4·7H2O的含量时,有时测定值会超过100%,其原因可能是FeSO4·7H2O会风化,失去部分结晶水。