题目
10 分 (0824)计算 1mol He(理想气体) 在下列状态变化过程中的ΔH和ΔG。He (101325 kPa,473 K) He (101325 kPa,673 K)已知:Cp, m [He(g)] = (5/2)R ,473K 时 S [He(g)] = 135.1 J·K-1·mol-1 。
10 分 (0824)
计算 1mol He(理想气体) 在下列状态变化过程中的ΔH和ΔG。
He (101325 kPa,473 K) He (101325 kPa,673 K)
已知:Cp, m [He(g)] = (5/2)R ,473K 时 S [He(g)] = 135.1 J·K-1·mol-1 。
题目解答
答案
解: ΔH=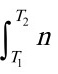 Cp,m dT =1×2.5×8.314×(673-473)=4.157 kJ (2分)
Cp,m dT =1×2.5×8.314×(673-473)=4.157 kJ (2分)
ΔS =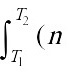 Cp,m /T)dT = nCp,m ln(T2/T1)
Cp,m /T)dT = nCp,m ln(T2/T1)
= 1×2.5×8.314×ln(673/473)=7.3 J·K-1 (4分)
S2= ΔS+S1= 142.4 J·K-1 (2分)
ΔG=ΔH-Δ(TS)=ΔH-(T2S2-T1S1 )
=4.157-(673×142.4-473×135.1) ×10-3=27.780kJ (2分)
解析
步骤 1:计算 ΔH
根据理想气体的热力学性质,对于一个理想气体,其焓变(ΔH)可以通过以下公式计算:
\[ \Delta H = n \int_{T_1}^{T_2} C_{p,m} dT \]
其中,\( n \) 是物质的量,\( C_{p,m} \) 是摩尔定压热容,\( T_1 \) 和 \( T_2 \) 分别是初始和最终温度。对于理想气体,\( C_{p,m} \) 是常数,因此积分可以简化为:
\[ \Delta H = n C_{p,m} (T_2 - T_1) \]
步骤 2:计算 ΔS
熵变(ΔS)可以通过以下公式计算:
\[ \Delta S = n \int_{T_1}^{T_2} \frac{C_{p,m}}{T} dT \]
对于理想气体,\( C_{p,m} \) 是常数,因此积分可以简化为:
\[ \Delta S = n C_{p,m} \ln \left( \frac{T_2}{T_1} \right) \]
步骤 3:计算 ΔG
吉布斯自由能变(ΔG)可以通过以下公式计算:
\[ \Delta G = \Delta H - T_2 \Delta S \]
其中,\( T_2 \) 是最终温度。由于 \( \Delta H \) 和 \( \Delta S \) 已经计算出来,可以直接代入公式计算 \( \Delta G \)。
根据理想气体的热力学性质,对于一个理想气体,其焓变(ΔH)可以通过以下公式计算:
\[ \Delta H = n \int_{T_1}^{T_2} C_{p,m} dT \]
其中,\( n \) 是物质的量,\( C_{p,m} \) 是摩尔定压热容,\( T_1 \) 和 \( T_2 \) 分别是初始和最终温度。对于理想气体,\( C_{p,m} \) 是常数,因此积分可以简化为:
\[ \Delta H = n C_{p,m} (T_2 - T_1) \]
步骤 2:计算 ΔS
熵变(ΔS)可以通过以下公式计算:
\[ \Delta S = n \int_{T_1}^{T_2} \frac{C_{p,m}}{T} dT \]
对于理想气体,\( C_{p,m} \) 是常数,因此积分可以简化为:
\[ \Delta S = n C_{p,m} \ln \left( \frac{T_2}{T_1} \right) \]
步骤 3:计算 ΔG
吉布斯自由能变(ΔG)可以通过以下公式计算:
\[ \Delta G = \Delta H - T_2 \Delta S \]
其中,\( T_2 \) 是最终温度。由于 \( \Delta H \) 和 \( \Delta S \) 已经计算出来,可以直接代入公式计算 \( \Delta G \)。