绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了rm Cr—Fe—Al—Mg的深度利用和rm Na^+内循环。工艺流程如图:气体A-|||-_(2)(g)+ 熔融NaOH H2O(1) ↓-|||-Na2CrO4溶液 → 工序③ Na2Cr2O7溶液+-|||-物质V(s)-|||-Fe(CrO2)2→ [高温连续氧化 → 工序① →□ 过滤 → 粗分离-|||-介稳态 NaOH溶液(循环)-|||-(含Al2O3,MgO) 过量气体A-|||-滤渣I-|||-无色 工序④ 物质V的溶液-|||-((OH))_(3)(s)+-|||-过量气体 +(H)_(2)O(g) → 工序② 溶液 →-|||-过滤 → 溶液 → 热解 一 MgCO3(s)→煅烧 →MgO(s)-|||-物质Ⅱ-|||-T T-|||-固体Ⅲ 混合气体IV回答下列问题:(1)高温连续氧化工序中被氧化的元素是 (填元素符号)。(2)工序①的名称为 。(3)滤渣的主要成分是 (填化学式)。(4)工序③中发生反应的离子方程式为 。(5)物质V可代替高温连续氧化工序中的 rm NaOH,此时发生的主要反应的化学方程式为 ,可代替 rm NaOH 的化学试剂还有 (填化学式)。(6)热解工序产生的混合气体最适宜返回工序 (填“①”或“②”或“③”或“④”)参与内循环。(7)工序④溶液中的铝元素恰好完全转化为沉淀的 rm pH 为 。(通常认为溶液中离子浓度小于 rm 10^-5 mathrm(molcdot L^-1) 为沉淀完全;rm A1(OH)_3+OH^-⇌Al(OH)_4^-:K=rm 10^0.63,K_mathrm W=rm 10^-14,K_(mathrm {sp)}[mathrm (A1(OH)_3)]=10-33)
绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了$$\rm Cr—Fe—Al—Mg$$的深度利用和$$\rm Na^+$$内循环。工艺流程如图:
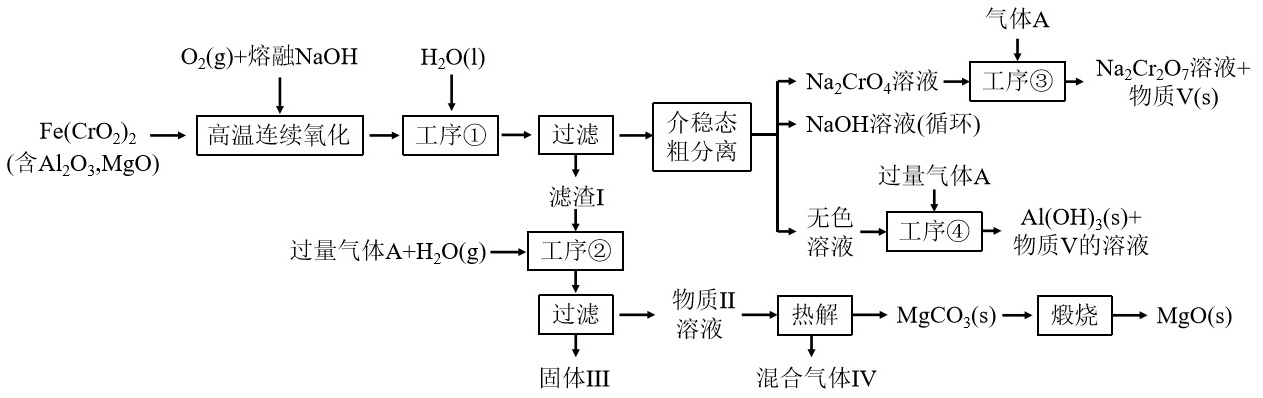
回答下列问题:
(1)高温连续氧化工序中被氧化的元素是 (填元素符号)。
(2)工序①的名称为 。
(3)滤渣的主要成分是 (填化学式)。
(4)工序③中发生反应的离子方程式为 。
(5)物质V可代替高温连续氧化工序中的 $$\rm NaOH$$,此时发生的主要反应的化学方程式为 ,可代替 $$\rm NaOH$$ 的化学试剂还有 (填化学式)。
(6)热解工序产生的混合气体最适宜返回工序 (填“①”或“②”或“③”或“④”)参与内循环。
(7)工序④溶液中的铝元素恰好完全转化为沉淀的 $$\rm pH$$ 为 。(通常认为溶液中离子浓度小于 $$\rm 10^{-5}$$ $$\mathrm{mol\cdot L^{-1}} $$为沉淀完全;$$\rm A1(OH)_3+OH^-⇌Al(OH)_4^-$$:$$K$$=$$\rm 10^{0.63}$$,$$K_\mathrm W$$=$$\rm 10^{-14}$$,$$K_{\mathrm {sp}}[\mathrm {A1(OH)_3}]$$=10-33)
题目解答
答案
(1) $$\rm Fe$$、$$\rm Cr$$ ;
(2) 溶解浸出;
(3)$$\rm MgO$$、$$\rm Fe_2O_3$$;
(4)$$\rm 2Na^+CrO_4^{2-}+2CO_2+H_2O\!=\!=\!= Na_2Cr_2O_7+2NaHCO_3\downarrow $$;
(5) $$\rm 4Fe(CrO_2)_2+7O_2+16NaHCO_3\overset{高温}{\!=\!=\!=} 8Na_2CrO_4+2Fe_2O_3+16CO_2+8H_2O$$; $$\rm Na_2CO_3$$;
(6) ②;
(7) 8.37。