题目
氢氧化钠水溶液中氢氧化钠的质量分数0.64,则其质量比为_______,摩尔分数_______。(以小数形式表达且保留两位小数)
氢氧化钠水溶液中氢氧化钠的质量分数0.64,则其质量比为_______,摩尔分数_______。(以小数形式表达且保留两位小数)
题目解答
答案
根据计算溶质质量分数的公式:
,假设溶质的质量+溶剂的质量等于 ,将氢氧化钠的质量分数和
,将氢氧化钠的质量分数和 带入计算溶质质量分数的公式可得
带入计算溶质质量分数的公式可得

,则可知溶质氢氧化钠的质量为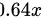 。则溶剂的质量为
。则溶剂的质量为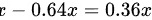 ,故其质量比为
,故其质量比为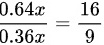 ,即
,即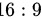 。
。
摩尔分数的计算公式为:
假设溶液的总质量为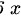 ,则溶质氢氧化钠的质量为
,则溶质氢氧化钠的质量为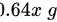 ,溶剂水的质量为
,溶剂水的质量为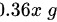 。由此可计算出溶质和溶剂物质的量分别为:
。由此可计算出溶质和溶剂物质的量分别为: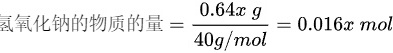
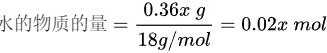
将数据代入计算物质摩尔分数的公式可得: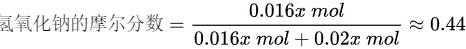
故综上所述,答案为:
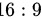 ;0.44
;0.44
解析
步骤 1:计算氢氧化钠和水的质量比
根据溶质质量分数的公式,假设溶液的总质量为x,则氢氧化钠的质量为0.64x,水的质量为0.36x。因此,氢氧化钠和水的质量比为$\dfrac{0.64x}{0.36x}=\dfrac{16}{9}$,即6:91。
步骤 2:计算氢氧化钠的摩尔分数
根据摩尔分数的计算公式,氢氧化钠的物质的量为$\dfrac{0.64x}{40}$,水的物质的量为$\dfrac{0.36x}{18}$。将这些值代入摩尔分数的公式,得到氢氧化钠的摩尔分数为$\dfrac{\dfrac{0.64x}{40}}{\dfrac{0.64x}{40}+\dfrac{0.36x}{18}}$,计算结果为0.44。
根据溶质质量分数的公式,假设溶液的总质量为x,则氢氧化钠的质量为0.64x,水的质量为0.36x。因此,氢氧化钠和水的质量比为$\dfrac{0.64x}{0.36x}=\dfrac{16}{9}$,即6:91。
步骤 2:计算氢氧化钠的摩尔分数
根据摩尔分数的计算公式,氢氧化钠的物质的量为$\dfrac{0.64x}{40}$,水的物质的量为$\dfrac{0.36x}{18}$。将这些值代入摩尔分数的公式,得到氢氧化钠的摩尔分数为$\dfrac{\dfrac{0.64x}{40}}{\dfrac{0.64x}{40}+\dfrac{0.36x}{18}}$,计算结果为0.44。