题目
5 . 铁卟啉(FeP)是细胞色素(P-450)的活性中心,具有将各种氧供体的氧原子活化并转移至底物的能力。研究人员为模拟活体内的加氧酶催化β-胡萝卜素(P)分解为维生素A(VA)的反应,以FeP为催化剂、间氯过氧化苯甲酸(CPBA)为氧化剂,研究了β-胡萝卜素的分解反应动力学。研究中FeP和CPBA的浓度可视为不变。无论是否存在催化剂FeP,该分解反应对一胡萝卜素均为一级反应。已知:若y=ax+b,则出dfrac (dy)(dt)=adfrac (dx)(dt)。式中,a,b均为与t无关的常数。实验A:在无FeP情况下,β-胡萝卜素-间氯过氧化苯甲酸反应体系(β-CPBA)的反应机理1如下(其中β*CPBA为反应中间物,CBA为间氯苯甲酸):(i)β+CPBAdfrac (dy)(dt)=adfrac (dx)(dt)β*CPBA平衡(ii)β*CPBAdfrac (dy)(dt)=adfrac (dx)(dt)VA+CBA实验B.以FeP为催化剂,β-胡萝卜素-间氯过氧化苯甲酸——啉反应体系(β-CPBA-FeP)的反应机理2如下(其中FeOP*CBA、β*FeOP*CBA、β*CPBA为反应中间物):(iii)FeP+CPBAdfrac (dy)(dt)=adfrac (dx)(dt)FeOP*CBA(快速平衡)(iv)FeOP*CBA+βdfrac (dy)(dt)=adfrac (dx)(dt)β*FeOP*CBA(快速平衡)(v)β*FeOP*CBAdfrac (dy)(dt)=adfrac (dx)(dt)VA+FeP+CBA(vi)β+CPBAdfrac (dy)(dt)=adfrac (dx)(dt)β*CPBA(快速平衡)(vi)β*CPBAdfrac (dy)(dt)=adfrac (dx)(dt)VA+CBA对该体系的实验结果进行曲线拟合,可得下表数据(dfrac (dy)(dt)=adfrac (dx)(dt)为反应的表观速率常数);T/Kk1/s-1k1/s-1dfrac (dy)(dt)=adfrac (dx)(dt)/s-1293.2301.24.869×10-37.731×10-31.350×10-42.398×10-45.865×10-49.795×10-4(1)对β-CBPA体系,根据实验测得的表观速率常数dfrac (dy)(dt)=adfrac (dx)(dt)(293.2K)=4.795×10-4s-1,dfrac (dy)(dt)=adfrac (dx)(dt)(301.2K)=8.285×10-4s-1,求反应的表观活化能dfrac (dy)(dt)=adfrac (dx)(dt)_____。(2)根据反应机理2推导dfrac (dy)(dt)=adfrac (dx)(dt)与[β]间关系的速率方程______,并给出dfrac (dy)(dt)=adfrac (dx)(dt)的表达式________。(3)已知β-CPBA-FeP体系反应的表观活化能dfrac (dy)(dt)=adfrac (dx)(dt)=47.07kJ·mol-1和机理2中(v)步的活化能Ea,1=42.43kJ·mol-1,计算(vii)步的活化能Ea,2___________。(4)分别根据以下条件,说明β-CPBA和β-CPBA-FeP中哪一个体系反应更为有利。①Ea,1与Ea,2的结果及题中所给其他数据_______。②dfrac (dy)(dt)=adfrac (dx)(dt)与dfrac (dy)(dt)=adfrac (dx)(dt)的结果及题中所给其他数据________。实验C.在金属卟啉催化氧化反应体系中加入一些含氮小分子,会加速反成。为揭示反应机理,研究了FeP与咪唑类(Im)含氮小分子的配位反应热力学。FeP+2lm⇌FePlm2(1)实验测得反应(1)的标准平衡常数dfrac (dy)(dt)=adfrac (dx)(dt)见下表。T/K293.2297.2301.2305.2dfrac (dy)(dt)=adfrac (dx)(dt)2.775×1051.012×1054.080×1041.458×104(5)请根据上表中293.2K和301.2K的平衡常数计算反应(1)的dfrac (dy)(dt)=adfrac (dx)(dt)=_____,dfrac (dy)(dt)=adfrac (dx)(dt)=_____。已知2730~400K间dfrac (dy)(dt)=adfrac (dx)(dt)=0。(6)用上表中所给数据和(5)的计算结果分別解释温度对反应(1)的影响______、________。(7)已知在一定温度下反应方向会发生变化,请计算反应的转向温度_________。
5 . 铁卟啉(FeP)是细胞色素(P-450)的活性中心,具有将各种氧供体的氧原子活化并转移至底物的能力。研究人员为模拟活体内的加氧酶催化β-胡萝卜素(P)分解为维生素A(VA)的反应,以FeP为催化剂、间氯过氧化苯甲酸(CPBA)为氧化剂,研究了β-胡萝卜素的分解反应动力学。研究中FeP和CPBA的浓度可视为不变。无论是否存在催化剂FeP,该分解反应对一胡萝卜素均为一级反应。
已知:若y=ax+b,则出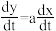 。式中,a,b均为与t无关的常数。
。式中,a,b均为与t无关的常数。
实验A:在无FeP情况下,β-胡萝卜素-间氯过氧化苯甲酸反应体系(β-CPBA)的反应机理1如下(其中β*CPBA为反应中间物,CBA为间氯苯甲酸):
(i)β+CPBA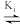 β*CPBA平衡
β*CPBA平衡
(ii)β*CPBA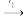 VA+CBA
VA+CBA
实验B.以FeP为催化剂,β-胡萝卜素-间氯过氧化苯甲酸——啉反应体系(β-CPBA-FeP)的反应机理2如下(其中FeOP*CBA、β*FeOP*CBA、β*CPBA为反应中间物):
(iii)FeP+CPBA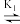 FeOP*CBA(快速平衡)
FeOP*CBA(快速平衡)
(iv)FeOP*CBA+β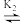 β*FeOP*CBA(快速平衡)
β*FeOP*CBA(快速平衡)
(v)β*FeOP*CBA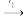 VA+FeP+CBA
VA+FeP+CBA
(vi)β+CPBA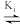 β*CPBA(快速平衡)
β*CPBA(快速平衡)
(vi)β*CPBA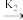 VA+CBA
VA+CBA
对该体系的实验结果进行曲线拟合,可得下表数据(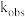 为反应的表观速率常数);
为反应的表观速率常数);
(1)对β-CBPA体系,根据实验测得的表观速率常数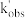 (293.2K)=4.795×10-4s-1,
(293.2K)=4.795×10-4s-1,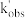 (301.2K)=8.285×10-4s-1,求反应的表观活化能
(301.2K)=8.285×10-4s-1,求反应的表观活化能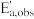
_____ 。
(2)根据反应机理2推导 与[β]间关系的速率方程
与[β]间关系的速率方程______ ,并给出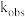 的表达式
的表达式________ 。
(3)已知β-CPBA-FeP体系反应的表观活化能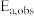 =47.07kJ·mol-1和机理2中(v)步的活化能Ea,1=42.43kJ·mol-1,计算(vii)步的活化能Ea,2
=47.07kJ·mol-1和机理2中(v)步的活化能Ea,1=42.43kJ·mol-1,计算(vii)步的活化能Ea,2___________ 。
(4)分别根据以下条件,说明β-CPBA和β-CPBA-FeP中哪一个体系反应更为有利。
①Ea,1与Ea,2的结果及题中所给其他数据_______ 。
②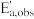 与
与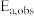 的结果及题中所给其他数据
的结果及题中所给其他数据________ 。
实验C.在金属卟啉催化氧化反应体系中加入一些含氮小分子,会加速反成。为揭示反应机理,研究了FeP与咪唑类(Im)含氮小分子的配位反应热力学。
FeP+2lm⇌FePlm2(1)
实验测得反应(1)的标准平衡常数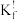 见下表。
见下表。
(5)请根据上表中293.2K和301.2K的平衡常数计算反应(1)的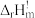 =
=_____ ,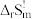 =
=_____ 。已知2730~400K间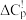 =0。
=0。
(6)用上表中所给数据和(5)的计算结果分別解释温度对反应(1)的影响______ 、________ 。
(7)已知在一定温度下反应方向会发生变化,请计算反应的转向温度_________ 。
已知:若y=ax+b,则出
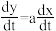 。式中,a,b均为与t无关的常数。
。式中,a,b均为与t无关的常数。实验A:在无FeP情况下,β-胡萝卜素-间氯过氧化苯甲酸反应体系(β-CPBA)的反应机理1如下(其中β*CPBA为反应中间物,CBA为间氯苯甲酸):
(i)β+CPBA
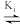 β*CPBA平衡
β*CPBA平衡(ii)β*CPBA
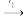 VA+CBA
VA+CBA实验B.以FeP为催化剂,β-胡萝卜素-间氯过氧化苯甲酸——啉反应体系(β-CPBA-FeP)的反应机理2如下(其中FeOP*CBA、β*FeOP*CBA、β*CPBA为反应中间物):
(iii)FeP+CPBA
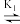 FeOP*CBA(快速平衡)
FeOP*CBA(快速平衡)(iv)FeOP*CBA+β
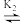 β*FeOP*CBA(快速平衡)
β*FeOP*CBA(快速平衡)(v)β*FeOP*CBA
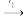 VA+FeP+CBA
VA+FeP+CBA(vi)β+CPBA
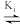 β*CPBA(快速平衡)
β*CPBA(快速平衡)(vi)β*CPBA
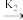 VA+CBA
VA+CBA对该体系的实验结果进行曲线拟合,可得下表数据(
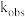 为反应的表观速率常数);
为反应的表观速率常数);| T/K | k1/s-1 | k1/s-1 | 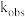 /s-1 /s-1 |
| 293.2301.2 | 4.869×10-37.731×10-3 | 1.350×10-42.398×10-4 | 5.865×10-49.795×10-4 |
(1)对β-CBPA体系,根据实验测得的表观速率常数
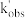 (293.2K)=4.795×10-4s-1,
(293.2K)=4.795×10-4s-1,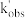 (301.2K)=8.285×10-4s-1,求反应的表观活化能
(301.2K)=8.285×10-4s-1,求反应的表观活化能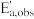
(2)根据反应机理2推导
 与[β]间关系的速率方程
与[β]间关系的速率方程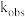 的表达式
的表达式(3)已知β-CPBA-FeP体系反应的表观活化能
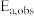 =47.07kJ·mol-1和机理2中(v)步的活化能Ea,1=42.43kJ·mol-1,计算(vii)步的活化能Ea,2
=47.07kJ·mol-1和机理2中(v)步的活化能Ea,1=42.43kJ·mol-1,计算(vii)步的活化能Ea,2(4)分别根据以下条件,说明β-CPBA和β-CPBA-FeP中哪一个体系反应更为有利。
①Ea,1与Ea,2的结果及题中所给其他数据
②
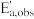 与
与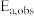 的结果及题中所给其他数据
的结果及题中所给其他数据实验C.在金属卟啉催化氧化反应体系中加入一些含氮小分子,会加速反成。为揭示反应机理,研究了FeP与咪唑类(Im)含氮小分子的配位反应热力学。
FeP+2lm⇌FePlm2(1)
实验测得反应(1)的标准平衡常数
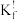 见下表。
见下表。| T/K | 293.2 | 297.2 | 301.2 | 305.2 |
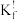 | 2.775×105 | 1.012×105 | 4.080×104 | 1.458×104 |
(5)请根据上表中293.2K和301.2K的平衡常数计算反应(1)的
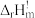 =
=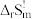 =
=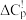 =0。
=0。(6)用上表中所给数据和(5)的计算结果分別解释温度对反应(1)的影响
(7)已知在一定温度下反应方向会发生变化,请计算反应的转向温度
题目解答
答案

解析
步骤 1:计算表观活化能Ea,obs
根据阿伦尼乌斯方程,$k_{obs} = A \exp(-\frac{E_{a,obs}}{RT})$,其中$R$是气体常数,$T$是温度,$A$是频率因子。对于两个不同温度下的速率常数,可以得到两个方程,联立求解得到$E_{a,obs}$。
步骤 2:推导速率方程和kobs的表达式
根据反应机理2,推导出速率方程$\frac{d[β]}{dt}$,并根据速率方程得到kobs的表达式。
步骤 3:计算E_a_,_2
根据表观活化能${890}^{\circ }B=$和E_a_,_1,利用表观活化能的定义计算E_a_,_2。
步骤 4:比较β-CPBA和β-CPBA-FeP体系的反应有利性
根据E_a_,_1与E_a_,_2的结果及题中所给其他数据,比较两个体系的反应有利性。
步骤 5:计算反应(1)的$\Delta H_m^{\theta}$和$\Delta S_m^{\theta}$
根据平衡常数和温度,利用热力学公式计算$\Delta H_m^{\theta}$和$\Delta S_m^{\theta}$。
步骤 6:解释温度对反应(1)的影响
根据$\Delta H_m^{\theta}$和$\Delta S_m^{\theta}$的符号,解释温度对反应(1)的影响。
步骤 7:计算反应的转向温度
根据$\Delta H_m^{\theta}$和$\Delta S_m^{\theta}$,利用热力学公式计算反应的转向温度。
根据阿伦尼乌斯方程,$k_{obs} = A \exp(-\frac{E_{a,obs}}{RT})$,其中$R$是气体常数,$T$是温度,$A$是频率因子。对于两个不同温度下的速率常数,可以得到两个方程,联立求解得到$E_{a,obs}$。
步骤 2:推导速率方程和kobs的表达式
根据反应机理2,推导出速率方程$\frac{d[β]}{dt}$,并根据速率方程得到kobs的表达式。
步骤 3:计算E_a_,_2
根据表观活化能${890}^{\circ }B=$和E_a_,_1,利用表观活化能的定义计算E_a_,_2。
步骤 4:比较β-CPBA和β-CPBA-FeP体系的反应有利性
根据E_a_,_1与E_a_,_2的结果及题中所给其他数据,比较两个体系的反应有利性。
步骤 5:计算反应(1)的$\Delta H_m^{\theta}$和$\Delta S_m^{\theta}$
根据平衡常数和温度,利用热力学公式计算$\Delta H_m^{\theta}$和$\Delta S_m^{\theta}$。
步骤 6:解释温度对反应(1)的影响
根据$\Delta H_m^{\theta}$和$\Delta S_m^{\theta}$的符号,解释温度对反应(1)的影响。
步骤 7:计算反应的转向温度
根据$\Delta H_m^{\theta}$和$\Delta S_m^{\theta}$,利用热力学公式计算反应的转向温度。