题目
【题文】某工厂的废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属Cu。请根据以下流程图,回答下列问题。加入试剂-|||-⑦ ③-|||-①-|||-工 加入试剂 ⑧ ④-|||-⑤ 操作方法-|||-⑥-|||-操作方法 FeSO4·7H2O-|||-②-|||-冷却结晶(1)填写下列标号所代表的物质(主要成分化学物质的化学式):① _______② _______③ _______④ _______⑤ _______⑦ _______(2)写出加入试剂⑤与工业废水反应的离子方程式: _______
【题文】某工厂的废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属Cu。请根据以下流程图,回答下列问题。
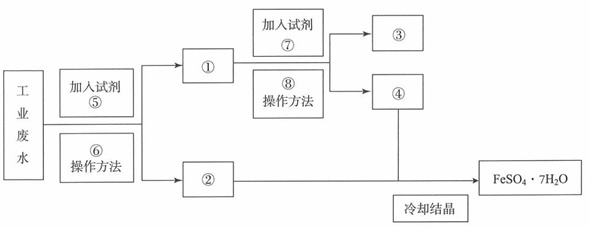
(1)填写下列标号所代表的物质(主要成分化学物质的化学式):① _______ ② _______ ③ _______ ④ _______ ⑤ _______ ⑦ _______
(2)写出加入试剂⑤与工业废水反应的离子方程式: _______

(1)填写下列标号所代表的物质(主要成分化学物质的化学式):①
(2)写出加入试剂⑤与工业废水反应的离子方程式:
题目解答
答案
【答案】Cu、Fe FeSO4 Cu FeSO4 Fe H2SO4(稀) Fe+Cu2+=Cu+Fe2+
解析
步骤 1:确定①的物质
根据流程图,加入试剂①后,通过操作方法⑥得到金属Cu,说明①是还原剂,可以将Cu^{2+}还原为Cu。常见的还原剂有Fe、Zn等,但考虑到FeSO_4的存在,Fe是更合适的还原剂。
步骤 2:确定②的物质
操作方法⑥得到金属Cu后,剩余的溶液中主要含有Fe^{2+},通过冷却结晶得到FeSO_4·7H_2O,说明②是FeSO_4。
步骤 3:确定③的物质
加入试剂③后,通过操作方法⑥得到FeSO_4·7H_2O,说明③是FeSO_4。
步骤 4:确定④的物质
操作方法⑥得到FeSO_4·7H_2O后,剩余的溶液中主要含有Fe^{2+},通过加入试剂⑤得到FeSO_4,说明④是FeSO_4。
步骤 5:确定⑤的物质
加入试剂⑤后,得到FeSO_4,说明⑤是H_2SO_4(稀)。
步骤 6:确定⑦的物质
加入试剂⑦后,通过操作方法⑥得到金属Cu,说明⑦是Fe。
步骤 7:写出加入试剂⑤与工业废水反应的离子方程式
加入试剂⑤(H_2SO_4)与工业废水中的Fe^{2+}反应,生成FeSO_4,离子方程式为:Fe+Cu^{2+}=Cu+Fe^{2+}。
根据流程图,加入试剂①后,通过操作方法⑥得到金属Cu,说明①是还原剂,可以将Cu^{2+}还原为Cu。常见的还原剂有Fe、Zn等,但考虑到FeSO_4的存在,Fe是更合适的还原剂。
步骤 2:确定②的物质
操作方法⑥得到金属Cu后,剩余的溶液中主要含有Fe^{2+},通过冷却结晶得到FeSO_4·7H_2O,说明②是FeSO_4。
步骤 3:确定③的物质
加入试剂③后,通过操作方法⑥得到FeSO_4·7H_2O,说明③是FeSO_4。
步骤 4:确定④的物质
操作方法⑥得到FeSO_4·7H_2O后,剩余的溶液中主要含有Fe^{2+},通过加入试剂⑤得到FeSO_4,说明④是FeSO_4。
步骤 5:确定⑤的物质
加入试剂⑤后,得到FeSO_4,说明⑤是H_2SO_4(稀)。
步骤 6:确定⑦的物质
加入试剂⑦后,通过操作方法⑥得到金属Cu,说明⑦是Fe。
步骤 7:写出加入试剂⑤与工业废水反应的离子方程式
加入试剂⑤(H_2SO_4)与工业废水中的Fe^{2+}反应,生成FeSO_4,离子方程式为:Fe+Cu^{2+}=Cu+Fe^{2+}。