题目
我国是一个海洋大国,海域面积十分辽阔。习主席在三亚考察时指出,一定要向海洋进军,加快建设海洋强国。加强创新协作,加快打造深海研发基地,加快发展深海科技事业,推动我国海洋科技全面发展。海水中蕴含着丰富的化学资源,我们应予以合理开发及综合利用。母液 石灰乳 g(OH)2 盐酸 MgCl2 通电 Mg-|||-① ② ③-|||-海水 NaOH 低温 NaClO-|||-粗盐 净化 NaCl NaCl 电解 Cl2 ⑦ (次氯酸钠)-|||-④ 溶液 ⑤ 饱和溶液 ⑥-|||-H2-|||-⑧ NaHCO3 加热 Na2CO3-|||-⑨-|||-图1(1)海水淡化。母液 石灰乳 g(OH)2 盐酸 MgCl2 通电 Mg-|||-① ② ③-|||-海水 NaOH 低温 NaClO-|||-粗盐 净化 NaCl NaCl 电解 Cl2 ⑦ (次氯酸钠)-|||-④ 溶液 ⑤ 饱和溶液 ⑥-|||-H2-|||-⑧ NaHCO3 加热 Na2CO3-|||-⑨-|||-图1①蒸馏法是常用的海水淡化方法,该方法是利用混合体系中各物质的 ____ 不同,将物质进行分离。②图2所示为膜分离法淡化海水,水分子可以通过淡化膜(海水中体积较大的盐的离子和其他分子不能通过)进入左侧的淡水池,从而得到淡水。下列说法中正确的是 ____ (填字母序号)。A.膜分离法的原理与滤纸过滤原理类似B.膜分离法还可以浓缩海水中的盐类物质C.该膜分离法的目的是除去海水中的不溶物(2)海水制镁。步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是 ____ 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 ____ 。(3)海水晒盐①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是 ____ (填字母序号)。A.在蒸发池中水蒸发所需能量主要为太阳能和风能B.在结晶池中主要通过降温结晶使氯化钠析出C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过 ____ 、过滤、蒸发结晶等操作。蒸发结晶操作中要用到玻璃棒,其作用是 ____ 。③通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是 ____ 。(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是 ____ 。(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH═X+NaClO+H2O,则X的化学式是 ____ 。(6)我国有9900多万公顷盐碱地,根据土壤类型和气候条件,分为滨海盐渍区、黄准海平原盐渍区、荒漠及荒漠草原盐渍区、草原盐渍区四大类型。盐碱地影响农作物正常生长,农作物产量极低,甚至寸草不生。盐碱土形成的根本原因在于水分状况不良,各种易溶性盐类在集盐地区的土壤表层逐渐积聚起来。有些地区春季地表水分蒸发强烈,地下水中的盐分随毛管水上升而聚集在土壤表层,此即“返盐“季节;有些地区到了秋季,土壤中会析出芒硝(主要成分是Na2SO4•10H2O),人们将上述现象俗称为“春泛盐,秋泛硝”。根据上述信息,试回答下列问题:①由图4可知,50℃时,两者中溶解度较大的物质是 ____ 。②将40℃等质量的NaCl和Na2SO4的饱和溶液同时降温到10℃,析出晶体较多的是 ____ 。③40℃时,将25gNa2SO4固体放入50g水中,充分溶解后,可得到Na2SO4的 ____ 溶液。(选填“饱和”或“不饱和”)④结合图4中的溶解度曲线,试解释“秋泛硝”的原理 ____ 。⑤盐碱地也是一种珍贵的土地资源,许多科技工作者正以满腔热情投入到治理盐碱地的工作中,目前已有许多可喜的实质性进展。下列方法措施中,不能改良盐碱地的是 ____ (选填序号之一)。A.向盐碱地里撒施大量熟石灰B.春秋季平整土地,适时耙地,并适量灌水洗盐C.施用有机肥料(能产生有机酸)和高效复合肥,并配合使用富含活性菌的土壤改良剂D.种植沙枣、白榆、胡杨、滨柃、枸杞等耐盐碱的植物
我国是一个海洋大国,海域面积十分辽阔。习主席在三亚考察时指出,一定要向海洋进军,加快建设海洋强国。加强创新协作,加快打造深海研发基地,加快发展深海科技事业,推动我国海洋科技全面发展。海水中蕴含着丰富的化学资源,我们应予以合理开发及综合利用。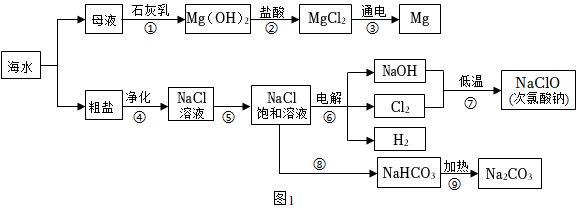
(1)海水淡化。
①蒸馏法是常用的海水淡化方法,该方法是利用混合体系中各物质的 ____ 不同,将物质进行分离。
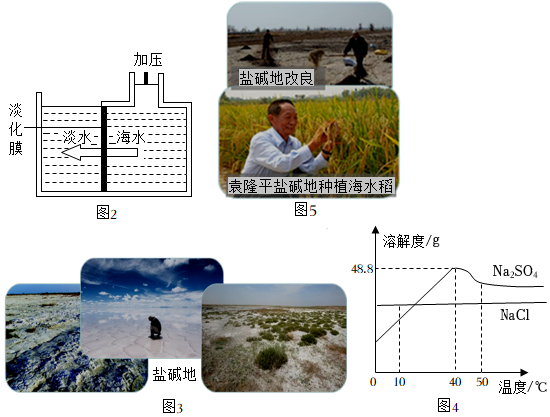
②图2所示为膜分离法淡化海水,水分子可以通过淡化膜(海水中体积较大的盐的离子和其他分子不能通过)进入左侧的淡水池,从而得到淡水。下列说法中正确的是 ____ (填字母序号)。
A.膜分离法的原理与滤纸过滤原理类似
B.膜分离法还可以浓缩海水中的盐类物质
C.该膜分离法的目的是除去海水中的不溶物
(2)海水制镁。步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是 ____ 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 ____ 。
(3)海水晒盐
①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是 ____ (填字母序号)。
A.在蒸发池中水蒸发所需能量主要为太阳能和风能
B.在结晶池中主要通过降温结晶使氯化钠析出
C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过 ____ 、过滤、
蒸发结晶等操作。蒸发结晶操作中要用到玻璃棒,其作用是 ____ 。
③通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是 ____ 。
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是 ____ 。
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH═X+NaClO+H2O,则X的化学式是 ____ 。
(6)我国有9900多万公顷盐碱地,根据土壤类型和气候条件,分为滨海盐渍区、黄准海平原盐渍区、荒漠及荒漠草原盐渍区、草原盐渍区四大类型。盐碱地影响农作物正常生长,农作物产量极低,甚至寸草不生。盐碱土形成的根本原因在于水分状况不良,各种易溶性盐类在集盐地区的土壤表层逐渐积聚起来。有些地区春季地表水分蒸发强烈,地下水中的盐分随毛管水上升而聚集在土壤表层,此即“返盐“季节;有些地区到了秋季,土壤中会析出芒硝(主要成分是Na2SO4•10H2O),人们将上述现象俗称为“春泛盐,秋泛硝”。
根据上述信息,试回答下列问题:
①由图4可知,50℃时,两者中溶解度较大的物质是 ____ 。
②将40℃等质量的NaCl和Na2SO4的饱和溶液同时降温到10℃,析出晶体较多的是 ____ 。
③40℃时,将25gNa2SO4固体放入50g水中,充分溶解后,可得到Na2SO4的 ____ 溶液。(选填“饱和”或“不饱和”)
④结合图4中的溶解度曲线,试解释“秋泛硝”的原理 ____ 。
⑤盐碱地也是一种珍贵的土地资源,许多科技工作者正以满腔热情投入到治理盐碱地的工作中,目前已有许多可喜的实质性进展。下列方法措施中,不能改良盐碱地的是 ____ (选填序号之一)。
A.向盐碱地里撒施大量熟石灰
B.春秋季平整土地,适时耙地,并适量灌水洗盐
C.施用有机肥料(能产生有机酸)和高效复合肥,并配合使用富含活性菌的土壤改良剂
D.种植沙枣、白榆、胡杨、滨柃、枸杞等耐盐碱的植物

(1)海水淡化。

①蒸馏法是常用的海水淡化方法,该方法是利用混合体系中各物质的 ____ 不同,将物质进行分离。
②图2所示为膜分离法淡化海水,水分子可以通过淡化膜(海水中体积较大的盐的离子和其他分子不能通过)进入左侧的淡水池,从而得到淡水。下列说法中正确的是 ____ (填字母序号)。
A.膜分离法的原理与滤纸过滤原理类似
B.膜分离法还可以浓缩海水中的盐类物质
C.该膜分离法的目的是除去海水中的不溶物
(2)海水制镁。步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是 ____ 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 ____ 。
(3)海水晒盐
①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是 ____ (填字母序号)。
A.在蒸发池中水蒸发所需能量主要为太阳能和风能
B.在结晶池中主要通过降温结晶使氯化钠析出
C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过 ____ 、过滤、
蒸发结晶等操作。蒸发结晶操作中要用到玻璃棒,其作用是 ____ 。
③通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是 ____ 。
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是 ____ 。
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH═X+NaClO+H2O,则X的化学式是 ____ 。
(6)我国有9900多万公顷盐碱地,根据土壤类型和气候条件,分为滨海盐渍区、黄准海平原盐渍区、荒漠及荒漠草原盐渍区、草原盐渍区四大类型。盐碱地影响农作物正常生长,农作物产量极低,甚至寸草不生。盐碱土形成的根本原因在于水分状况不良,各种易溶性盐类在集盐地区的土壤表层逐渐积聚起来。有些地区春季地表水分蒸发强烈,地下水中的盐分随毛管水上升而聚集在土壤表层,此即“返盐“季节;有些地区到了秋季,土壤中会析出芒硝(主要成分是Na2SO4•10H2O),人们将上述现象俗称为“春泛盐,秋泛硝”。
根据上述信息,试回答下列问题:
①由图4可知,50℃时,两者中溶解度较大的物质是 ____ 。
②将40℃等质量的NaCl和Na2SO4的饱和溶液同时降温到10℃,析出晶体较多的是 ____ 。
③40℃时,将25gNa2SO4固体放入50g水中,充分溶解后,可得到Na2SO4的 ____ 溶液。(选填“饱和”或“不饱和”)
④结合图4中的溶解度曲线,试解释“秋泛硝”的原理 ____ 。
⑤盐碱地也是一种珍贵的土地资源,许多科技工作者正以满腔热情投入到治理盐碱地的工作中,目前已有许多可喜的实质性进展。下列方法措施中,不能改良盐碱地的是 ____ (选填序号之一)。
A.向盐碱地里撒施大量熟石灰
B.春秋季平整土地,适时耙地,并适量灌水洗盐
C.施用有机肥料(能产生有机酸)和高效复合肥,并配合使用富含活性菌的土壤改良剂
D.种植沙枣、白榆、胡杨、滨柃、枸杞等耐盐碱的植物
题目解答
答案
解:(1)①蒸馏法是常用的海水淡化方法,该方法是利用混合体系中各物质的沸点不同,将物质分离;故答案为:沸点;
②A、海水中体积较大的盐的离子和其他分子不能通过淡化膜,故膜分离法的原理与滤纸过滤原理类似,故A正确;
B、膜分离法只能让水分子透过,故可以浓缩海水中的盐类物质,故B正确;
C、该膜分离法的目的是除去海水中的可溶性盐类物质,故C错误;
故选:AB;
(2)中和反应是酸和碱反应生成盐和水,分析流程图可知,氢氧化镁与盐酸反应生成氯化镁和水,则流程中发生中和反应的化学方程式是Mg(OH)2+2HCl=MgCl2+2H2O,母液是蒸发水后氯化钠的饱和溶液,步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是母液中镁离子浓度高,故答案为:Mg(OH)2+2HCl=MgCl2+2H2O;母液中Mg2+的浓度高;
(3)①A、在蒸发池中水蒸发所需能量主要为太阳能和风能,故A正确;
B、在结晶池中主要通过蒸发结晶使氯化钠析出,故B错误;
C、当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液,故C正确;
故选:AC;
②在实验室中除去粗盐中的难溶性杂质,可依次通过溶解、过滤、蒸发结晶等操作。蒸发结晶操作中要用到玻璃棒,其作用是搅拌,防止液体局部温度过高,导致液体飞溅,故答案为:溶解;搅拌,防止液体局部温度过高导致液体飞溅;
③由题意可知,要除去粗盐中的MgCl2、Na2SO4、CaCl2等可溶性杂质,加入过量的BaCl2溶液,氯化钡溶液能与硫酸钠反应生成了硫酸钡沉淀,再加入的碳酸钠能与过量的氯化钡、氯化钙反应,所以加入Na2CO3溶液的目的是除去CaCl2和过量的BaCl2,故答案为:除去钙离子和过量的钡离子;
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,同时产生了氯气和氢气,根据质量守恒定律,该反应中的反应物是氯化钠和水,故答案为:NaCl和水。
(5)化学反应前后原子的种类和个数守恒,分析Cl2+2NaOH═X+NaClO+H2O可知,反应前Cl、Na、O、H的个数分别为2、2、2、2,反应后已知物质中Cl、Na、O、H的个数分别为1、1、2、2,则X物质中含有1个Na和1个Cl,化学式为NaCl,故答案为:NaCl。
(6)①由溶解度曲线可知,50℃时,两者中溶解度较大的物质是硫酸钠,故答案为:Na2SO4;
②由溶解度曲线可知,硫酸钠的溶解度受温度影响较大,所以将40℃等质量的NaCl和Na2SO4的饱和溶液同时降温到10℃,析出晶体较多的是硫酸钠,故答案为:Na2SO4;
③由溶解度曲线可知,40℃时,硫酸钠的溶解度为48.8g,即在该温度的100g水中最多溶解48.8g硫酸钠就达到饱和状态,则在该温度下的50g水中最多溶解24.4g硫酸钠就达到饱和,即40℃时,将25gNa2SO4 固体放入50g水中,充分溶解后,可得到硫酸钠的饱和溶液,故答案为:饱和;
④夏季温度高,硫酸钠的溶解度随温度的升高明显增大,且水分蒸发快,溶液接近饱和,秋天时气温降低,硫酸钠的溶解度迅速变小从而析出,故答案为:Na2SO4的溶解度随温度(温度小于40℃时)的降低而减小,秋天温度低,Na2SO4的溶解度减小,所以土壤中会有Na2SO4析出。
⑤A、由题干信息可知,向盐碱地里撒施大量熟石灰不能改良盐碱地,符合题意,故A正确;
B、春秋季平整土地,适时耙地,并适量灌水洗盐可以改良盐碱地,不合题意,故B错误;
C、施用有机肥料(能产生有机酸)和高效复合肥,并配合使用富含活性菌的土壤改良剂可以改良盐碱地,不合题意,故C错误;
D、种植沙枣、白榆、胡杨、滨柃、枸杞等耐盐碱的植物,不合题意,故D错误。
故选:A。
②A、海水中体积较大的盐的离子和其他分子不能通过淡化膜,故膜分离法的原理与滤纸过滤原理类似,故A正确;
B、膜分离法只能让水分子透过,故可以浓缩海水中的盐类物质,故B正确;
C、该膜分离法的目的是除去海水中的可溶性盐类物质,故C错误;
故选:AB;
(2)中和反应是酸和碱反应生成盐和水,分析流程图可知,氢氧化镁与盐酸反应生成氯化镁和水,则流程中发生中和反应的化学方程式是Mg(OH)2+2HCl=MgCl2+2H2O,母液是蒸发水后氯化钠的饱和溶液,步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是母液中镁离子浓度高,故答案为:Mg(OH)2+2HCl=MgCl2+2H2O;母液中Mg2+的浓度高;
(3)①A、在蒸发池中水蒸发所需能量主要为太阳能和风能,故A正确;
B、在结晶池中主要通过蒸发结晶使氯化钠析出,故B错误;
C、当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液,故C正确;
故选:AC;
②在实验室中除去粗盐中的难溶性杂质,可依次通过溶解、过滤、蒸发结晶等操作。蒸发结晶操作中要用到玻璃棒,其作用是搅拌,防止液体局部温度过高,导致液体飞溅,故答案为:溶解;搅拌,防止液体局部温度过高导致液体飞溅;
③由题意可知,要除去粗盐中的MgCl2、Na2SO4、CaCl2等可溶性杂质,加入过量的BaCl2溶液,氯化钡溶液能与硫酸钠反应生成了硫酸钡沉淀,再加入的碳酸钠能与过量的氯化钡、氯化钙反应,所以加入Na2CO3溶液的目的是除去CaCl2和过量的BaCl2,故答案为:除去钙离子和过量的钡离子;
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,同时产生了氯气和氢气,根据质量守恒定律,该反应中的反应物是氯化钠和水,故答案为:NaCl和水。
(5)化学反应前后原子的种类和个数守恒,分析Cl2+2NaOH═X+NaClO+H2O可知,反应前Cl、Na、O、H的个数分别为2、2、2、2,反应后已知物质中Cl、Na、O、H的个数分别为1、1、2、2,则X物质中含有1个Na和1个Cl,化学式为NaCl,故答案为:NaCl。
(6)①由溶解度曲线可知,50℃时,两者中溶解度较大的物质是硫酸钠,故答案为:Na2SO4;
②由溶解度曲线可知,硫酸钠的溶解度受温度影响较大,所以将40℃等质量的NaCl和Na2SO4的饱和溶液同时降温到10℃,析出晶体较多的是硫酸钠,故答案为:Na2SO4;
③由溶解度曲线可知,40℃时,硫酸钠的溶解度为48.8g,即在该温度的100g水中最多溶解48.8g硫酸钠就达到饱和状态,则在该温度下的50g水中最多溶解24.4g硫酸钠就达到饱和,即40℃时,将25gNa2SO4 固体放入50g水中,充分溶解后,可得到硫酸钠的饱和溶液,故答案为:饱和;
④夏季温度高,硫酸钠的溶解度随温度的升高明显增大,且水分蒸发快,溶液接近饱和,秋天时气温降低,硫酸钠的溶解度迅速变小从而析出,故答案为:Na2SO4的溶解度随温度(温度小于40℃时)的降低而减小,秋天温度低,Na2SO4的溶解度减小,所以土壤中会有Na2SO4析出。
⑤A、由题干信息可知,向盐碱地里撒施大量熟石灰不能改良盐碱地,符合题意,故A正确;
B、春秋季平整土地,适时耙地,并适量灌水洗盐可以改良盐碱地,不合题意,故B错误;
C、施用有机肥料(能产生有机酸)和高效复合肥,并配合使用富含活性菌的土壤改良剂可以改良盐碱地,不合题意,故C错误;
D、种植沙枣、白榆、胡杨、滨柃、枸杞等耐盐碱的植物,不合题意,故D错误。
故选:A。