题目
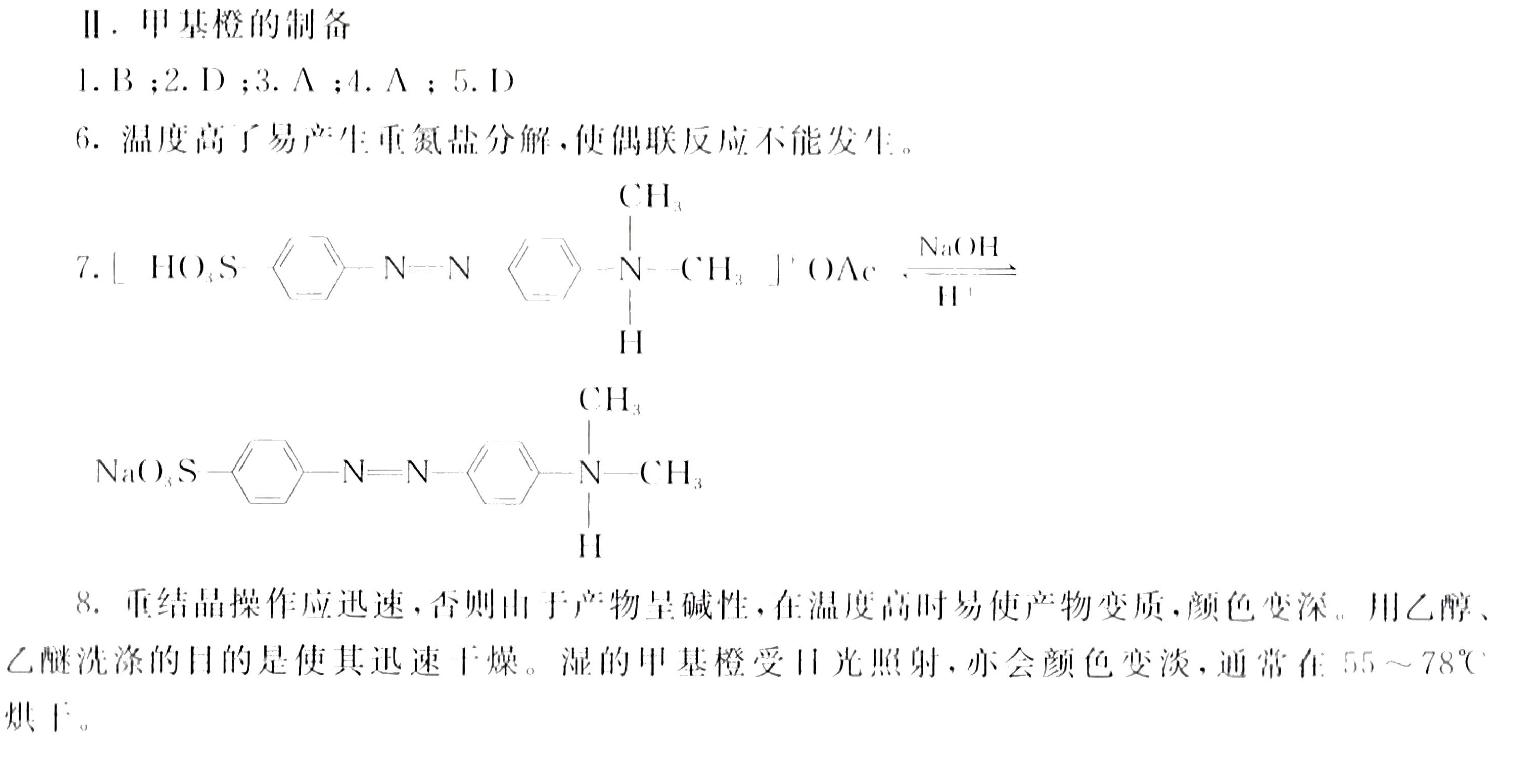
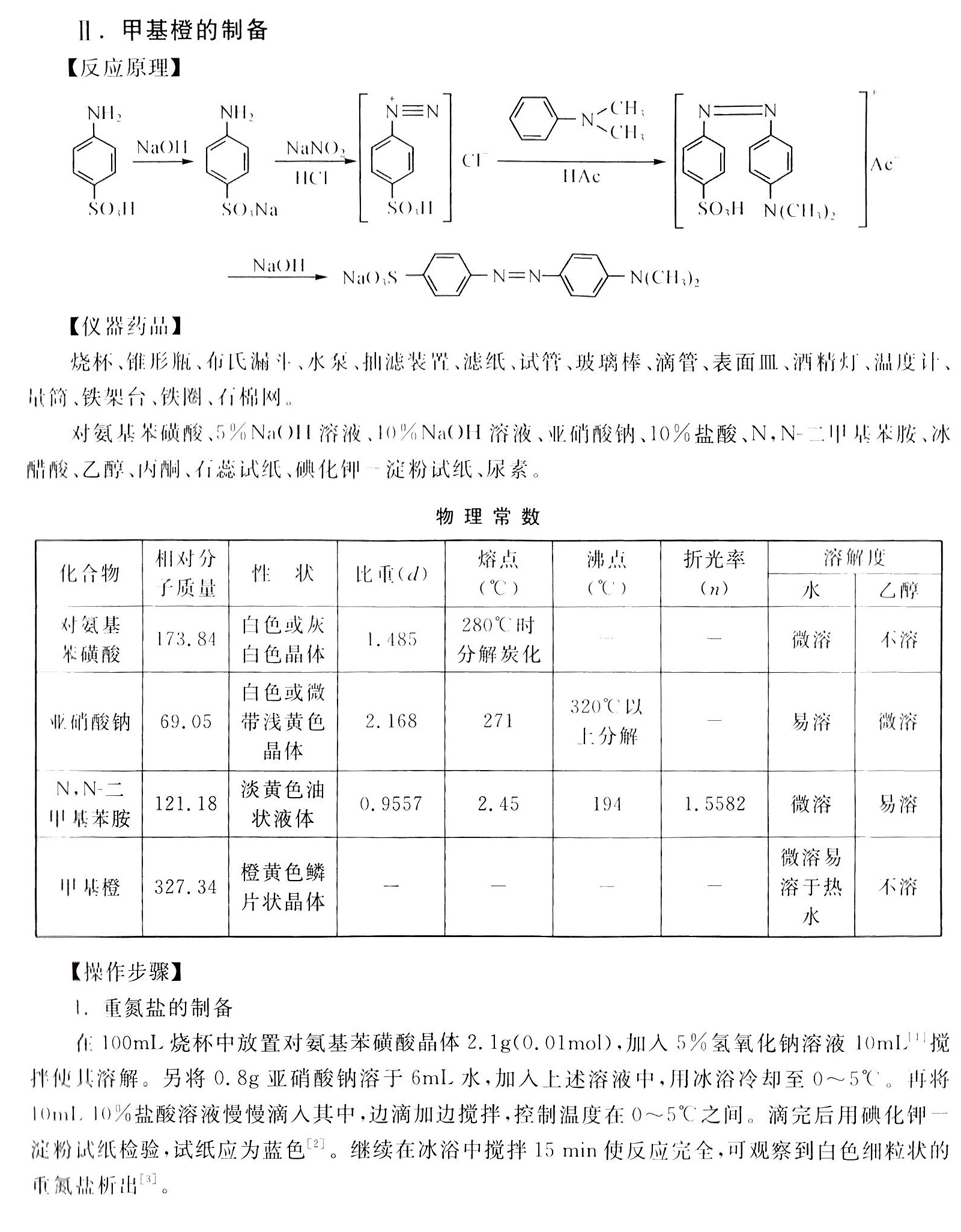
Ⅱ.甲基橙的制备-|||-[反应原理]-|||-NH2 NH2 equiv N 7 N-CH N N-|||-C'H-|||-NaOll NaNO2 Cl Ac-|||-IIC' 11AC-|||-SO3 SO3Na SO3H N(CH3)2-|||-NaO NaO3S 一 =N- 一 -N(CH3)2-|||-[仪器药品]-|||-烧杯、锥形瓶、布氏湔斗、水泵、抽滤装置、滤纸、试管、玻璃棒、滴管、表面皿、酒精灯、温度计、-|||-量筒、铁架台、铁圈、有棉网。-|||-对氨基苯磺酸、5%NaOH溶液、10%NaOH溶液、亚硝酸钠、10%盐酸、 ,N 二甲基苯胺、冰-|||-醋酸、乙醇、丙酮、石蕊试纸、碘化钾一淀粉试纸、尿素。-|||-物理常数-|||-化合物 相对分 性状 比重(d) (℃) ( ) (n) 水 乙醇-|||-熔点 沸点 折光率 溶解度-|||-子质量-|||-对氨基 173.84 白色或灰 280℃时 微溶 不溶-|||-苯磺酸 白色晶体 1.485 分解炭化-|||-白色或微-|||-业硝酸钠 69.05 带浅黄色 2.168 271 320℃以-|||-一 易溶 微溶-|||-晶体 上分解-|||-N,N-二 121.18 淡黄色油 0.9557 2.45 194 1.5582 微溶 易溶-|||-甲基苯胺 状液体-|||-甲 基橙 327.34 橙黄色鳞 微溶易-|||-片状晶体 一 溶于热 不溶-|||-水-|||-1.重氮盐的制备-|||-在100mL烧杯中放置对氨基苯磺酸晶体2.11g(0.01mol)),加入5%氢氧化钠溶液 (L)^111 搅-|||-拌使其溶解。另将0.8g亚硝酸钠溶于6mL水,加入上述溶液中,用冰浴冷却至 2.偶合-|||-重氮盐的冷的悬浊液中,同时用力搅拌,甲基橙呈红色沉淀析出。滴完后继续在冰浴中搅拌-|||-10min使耦合完全。向反应物中加入 sim 15mL10% 氢氧化钠溶液并搅拌,直至对石蕊试纸显-|||-碱性红色转变为橙色。将反应混合物用热水浴加热至 sim (65)^circ C ,使生成的甲基-|||-橙晶体基本溶解,冷却至室温后再以冰水浴冷却。待结晶完全后抽滤收集晶体,用少量冷水洗-|||-涤,再依次用少量乙醇和少量丙酮(或乙醚)洗涤,压干,得到粗产品。-|||-若要得到较纯产品,可用溶有少量氢氧化钠(约 1.重氮盐与芳胺类化合物发生偶联反应,在什么条件下进行为宜 ()-|||-A.强酸 B.弱酸性和中性 C.弱碱性和中性 D.强碱-|||-2.重氮化反应在下列哪一条件下进行 ()-|||-A.强碱 B.弱酸性和中性 C.弱碱性和中性 D.强酸-|||-3.制备重氮盐的温度范围是 ()-|||-A. sim (5)^circ C B. sim (9)^circ C C. (10sim {15)^circ C} D. sim (20)^circ C-|||-4.检验重氮化反应终点用什么方法 ()-|||-A.淀粉试纸变色 B.刚果红试纸变色-|||-C.石蕊试纸变色 D.酚酞试剂-|||-5.下列关于对氨基苯磺酸的说法错误的是 ()-|||-A.它是两性化合物 B.它的酸性强于碱性,可成内盐-|||-C.加碱后仍可成盐,且增加溶解度 D.它不能进行重氮化反应-|||-6.本实验中重氮盐的制备为什么要控制在 sim (5)^circ C 中进行?-|||-7.试简述甲基橙在酸碱介质中变色的原因,并用反应式表示之。-|||-8.为何重结晶操作应迅速?重结晶时待结晶析出完全后,抽滤收集的沉淀再依次川少量乙-|||-醇和少量丙酮(或乙醚)洗涤的目的是什么?.1sim 0.2g )的沸水进行重结晶。待结晶析出-|||-完全后抽滤收集。沉淀依次用少量乙醇和少量丙酮(或乙醚)洗涤,得到橙色的小叶片状甲基橙-|||-结晶。样品称重后再计算产率。-|||-溶解少许产品于水中,加几滴稀盐酸,然后用稀氢氧化钠溶液中和,观察颜色变化。-|||-[注释][1]对氨基苯磺酸是两性化合物,酸性强于碱性,以内盐形式存在,可与碱作用成盐-|||-而不能与酸成盐。重氮化作用要求在酸性水溶液中进行.故先使其与碱作用生成盐以利溶解。-|||-[2]试纸显蓝色表明有过量的亚硝酸存在,反应为:-|||-(O)_(2)-2KI+2HClarrow (H)_(2)NOuparrow +2(H)_(2)O+2KCl-|||-析出的碘遇淀粉显蓝色。本实验中亚硝酸的用量要准确,若亚硝酸不足,则重氮化作用不完全;-|||-如亚硝酸过量,则会与后面加入的N, 二甲苯胺发生亚硝化反应:-|||-^+ (H3C)2N= bigcirc )= N-OH-|||-.(({H)_(3)C)}_(2)N- 一 NO NaOH NaO bigcirc > +((C{H)_(3))}_(2)NH-|||-HNO2 →(H3C)2N-|||-生成的醌后或亚硝基物夹杂在产品中会使产品颜色暗褐。故正确的做法是:若试纸不显示蓝色,-|||-则应滴加亚硝酸钠溶液至刚刚出现蓝色。继续搅拌,反应15min后再检验。若试纸为蓝色,则应-|||-加入少许尿素分解过量的亚硝酸。-|||-[3]此重氮盐在水中可以电离形成中性内盐( Longrightarrow (({S)_(3)S-square )}^-N-Nequiv N ),在低温下难溶于水-|||-而析出。-|||-[4]用石蕊试纸检查以确保反应混合物为碱性,否则产品色泽不佳。当反应混合物已达碱-|||-性时,若再滴加碱液,则碱液接触反应物表面时将不再产生黄色,此亦可作为判据之一。-|||-[5]若反应物中含有未作用的N, 二甲基苯胺醋酸盐,在加入氢氧化钠后,就会有难溶于水-|||-的N, 二甲基苯胺析出,影响产物的纯度。湿的甲基橙在空气中受光的照射后,颜色很快变深,-|||-所以一般得紫红色粗产物。-|||-[6]重结晶操作应迅速,否则由于产物呈碱性,在温度高时易使产物变质,颜色变深。用乙-|||-醇、乙醚洗涤的目的是使其迅速干燥。-|||-[7]甲基橙的另一制法:在100mL烧杯中放置2.1g磨细的对氨基苯磺酸(0.012mol)和-|||-20mL水,在冰盐浴中冷却至0℃左右;然后加入0.8g磨细的亚硝酸钠,不断搅拌,直到对氨基苯-|||-磺酸全溶为止。sim (5)^circ C 。再将-|||-10mL10%盐酸溶液慢慢滴入其中,边滴加边搅拌,控制温度在 2.偶合-|||-重氮盐的冷的悬浊液中,同时用力搅拌,甲基橙呈红色沉淀析出。滴完后继续在冰浴中搅拌-|||-10min使耦合完全。向反应物中加入 sim 15mL10% 氢氧化钠溶液并搅拌,直至对石蕊试纸显-|||-碱性红色转变为橙色。将反应混合物用热水浴加热至 sim (65)^circ C ,使生成的甲基-|||-橙晶体基本溶解,冷却至室温后再以冰水浴冷却。待结晶完全后抽滤收集晶体,用少量冷水洗-|||-涤,再依次用少量乙醇和少量丙酮(或乙醚)洗涤,压干,得到粗产品。-|||-若要得到较纯产品,可用溶有少量氢氧化钠(约 1.重氮盐与芳胺类化合物发生偶联反应,在什么条件下进行为宜 ()-|||-A.强酸 B.弱酸性和中性 C.弱碱性和中性 D.强碱-|||-2.重氮化反应在下列哪一条件下进行 ()-|||-A.强碱 B.弱酸性和中性 C.弱碱性和中性 D.强酸-|||-3.制备重氮盐的温度范围是 ()-|||-A. sim (5)^circ C B. sim (9)^circ C C. (10sim {15)^circ C} D. sim (20)^circ C-|||-4.检验重氮化反应终点用什么方法 ()-|||-A.淀粉试纸变色 B.刚果红试纸变色-|||-C.石蕊试纸变色 D.酚酞试剂-|||-5.下列关于对氨基苯磺酸的说法错误的是 ()-|||-A.它是两性化合物 B.它的酸性强于碱性,可成内盐-|||-C.加碱后仍可成盐,且增加溶解度 D.它不能进行重氮化反应-|||-6.本实验中重氮盐的制备为什么要控制在 sim (5)^circ C 中进行?-|||-7.试简述甲基橙在酸碱介质中变色的原因,并用反应式表示之。-|||-8.为何重结晶操作应迅速?重结晶时待结晶析出完全后,抽滤收集的沉淀再依次川少量乙-|||-醇和少量丙酮(或乙醚)洗涤的目的是什么?.1sim 0.2g )的沸水进行重结晶。待结晶析出-|||-完全后抽滤收集。沉淀依次用少量乙醇和少量丙酮(或乙醚)洗涤,得到橙色的小叶片状甲基橙-|||-结晶。样品称重后再计算产率。-|||-溶解少许产品于水中,加几滴稀盐酸,然后用稀氢氧化钠溶液中和,观察颜色变化。-|||-[注释][1]对氨基苯磺酸是两性化合物,酸性强于碱性,以内盐形式存在,可与碱作用成盐-|||-而不能与酸成盐。重氮化作用要求在酸性水溶液中进行.故先使其与碱作用生成盐以利溶解。-|||-[2]试纸显蓝色表明有过量的亚硝酸存在,反应为:-|||-(O)_(2)-2KI+2HClarrow (H)_(2)NOuparrow +2(H)_(2)O+2KCl-|||-析出的碘遇淀粉显蓝色。本实验中亚硝酸的用量要准确,若亚硝酸不足,则重氮化作用不完全;-|||-如亚硝酸过量,则会与后面加入的N, 二甲苯胺发生亚硝化反应:-|||-^+ (H3C)2N= bigcirc )= N-OH-|||-.(({H)_(3)C)}_(2)N- 一 NO NaOH NaO bigcirc > +((C{H)_(3))}_(2)NH-|||-HNO2 →(H3C)2N-|||-生成的醌后或亚硝基物夹杂在产品中会使产品颜色暗褐。故正确的做法是:若试纸不显示蓝色,-|||-则应滴加亚硝酸钠溶液至刚刚出现蓝色。继续搅拌,反应15min后再检验。若试纸为蓝色,则应-|||-加入少许尿素分解过量的亚硝酸。-|||-[3]此重氮盐在水中可以电离形成中性内盐( Longrightarrow (({S)_(3)S-square )}^-N-Nequiv N ),在低温下难溶于水-|||-而析出。-|||-[4]用石蕊试纸检查以确保反应混合物为碱性,否则产品色泽不佳。当反应混合物已达碱-|||-性时,若再滴加碱液,则碱液接触反应物表面时将不再产生黄色,此亦可作为判据之一。-|||-[5]若反应物中含有未作用的N, 二甲基苯胺醋酸盐,在加入氢氧化钠后,就会有难溶于水-|||-的N, 二甲基苯胺析出,影响产物的纯度。湿的甲基橙在空气中受光的照射后,颜色很快变深,-|||-所以一般得紫红色粗产物。-|||-[6]重结晶操作应迅速,否则由于产物呈碱性,在温度高时易使产物变质,颜色变深。用乙-|||-醇、乙醚洗涤的目的是使其迅速干燥。-|||-[7]甲基橙的另一制法:在100mL烧杯中放置2.1g磨细的对氨基苯磺酸(0.012mol)和-|||-20mL水,在冰盐浴中冷却至0℃左右;然后加入0.8g磨细的亚硝酸钠,不断搅拌,直到对氨基苯-|||-磺酸全溶为止。sim (5)^circ C 之间。滴完后用碘化钾-|||-淀粉试纸检验,试纸应为蓝色221。继续在冰浴中搅拌15 min使反应完全,可观察到白色细粒状的-|||-重氮盐析出Ⅱ.甲基橙的制备-|||-[反应原理]-|||-NH2 NH2 equiv N 7 N-CH N N-|||-C'H-|||-NaOll NaNO2 Cl Ac-|||-IIC' 11AC-|||-SO3 SO3Na SO3H N(CH3)2-|||-NaO NaO3S 一 =N- 一 -N(CH3)2-|||-[仪器药品]-|||-烧杯、锥形瓶、布氏湔斗、水泵、抽滤装置、滤纸、试管、玻璃棒、滴管、表面皿、酒精灯、温度计、-|||-量筒、铁架台、铁圈、有棉网。-|||-对氨基苯磺酸、5%NaOH溶液、10%NaOH溶液、亚硝酸钠、10%盐酸、 ,N 二甲基苯胺、冰-|||-醋酸、乙醇、丙酮、石蕊试纸、碘化钾一淀粉试纸、尿素。-|||-物理常数-|||-化合物 相对分 性状 比重(d) (℃) ( ) (n) 水 乙醇-|||-熔点 沸点 折光率 溶解度-|||-子质量-|||-对氨基 173.84 白色或灰 280℃时 微溶 不溶-|||-苯磺酸 白色晶体 1.485 分解炭化-|||-白色或微-|||-业硝酸钠 69.05 带浅黄色 2.168 271 320℃以-|||-一 易溶 微溶-|||-晶体 上分解-|||-N,N-二 121.18 淡黄色油 0.9557 2.45 194 1.5582 微溶 易溶-|||-甲基苯胺 状液体-|||-甲 基橙 327.34 橙黄色鳞 微溶易-|||-片状晶体 一 溶于热 不溶-|||-水-|||-1.重氮盐的制备-|||-在100mL烧杯中放置对氨基苯磺酸晶体2.11g(0.01mol)),加入5%氢氧化钠溶液 (L)^111 搅-|||-拌使其溶解。另将0.8g亚硝酸钠溶于6mL水,加入上述溶液中,用冰浴冷却至 2.偶合-|||-重氮盐的冷的悬浊液中,同时用力搅拌,甲基橙呈红色沉淀析出。滴完后继续在冰浴中搅拌-|||-10min使耦合完全。向反应物中加入 sim 15mL10% 氢氧化钠溶液并搅拌,直至对石蕊试纸显-|||-碱性红色转变为橙色。将反应混合物用热水浴加热至 sim (65)^circ C ,使生成的甲基-|||-橙晶体基本溶解,冷却至室温后再以冰水浴冷却。待结晶完全后抽滤收集晶体,用少量冷水洗-|||-涤,再依次用少量乙醇和少量丙酮(或乙醚)洗涤,压干,得到粗产品。-|||-若要得到较纯产品,可用溶有少量氢氧化钠(约 1.重氮盐与芳胺类化合物发生偶联反应,在什么条件下进行为宜 ()-|||-A.强酸 B.弱酸性和中性 C.弱碱性和中性 D.强碱-|||-2.重氮化反应在下列哪一条件下进行 ()-|||-A.强碱 B.弱酸性和中性 C.弱碱性和中性 D.强酸-|||-3.制备重氮盐的温度范围是 ()-|||-A. sim (5)^circ C B. sim (9)^circ C C. (10sim {15)^circ C} D. sim (20)^circ C-|||-4.检验重氮化反应终点用什么方法 ()-|||-A.淀粉试纸变色 B.刚果红试纸变色-|||-C.石蕊试纸变色 D.酚酞试剂-|||-5.下列关于对氨基苯磺酸的说法错误的是 ()-|||-A.它是两性化合物 B.它的酸性强于碱性,可成内盐-|||-C.加碱后仍可成盐,且增加溶解度 D.它不能进行重氮化反应-|||-6.本实验中重氮盐的制备为什么要控制在 sim (5)^circ C 中进行?-|||-7.试简述甲基橙在酸碱介质中变色的原因,并用反应式表示之。-|||-8.为何重结晶操作应迅速?重结晶时待结晶析出完全后,抽滤收集的沉淀再依次川少量乙-|||-醇和少量丙酮(或乙醚)洗涤的目的是什么?.1sim 0.2g )的沸水进行重结晶。待结晶析出-|||-完全后抽滤收集。沉淀依次用少量乙醇和少量丙酮(或乙醚)洗涤,得到橙色的小叶片状甲基橙-|||-结晶。样品称重后再计算产率。-|||-溶解少许产品于水中,加几滴稀盐酸,然后用稀氢氧化钠溶液中和,观察颜色变化。-|||-[注释][1]对氨基苯磺酸是两性化合物,酸性强于碱性,以内盐形式存在,可与碱作用成盐-|||-而不能与酸成盐。重氮化作用要求在酸性水溶液中进行.故先使其与碱作用生成盐以利溶解。-|||-[2]试纸显蓝色表明有过量的亚硝酸存在,反应为:-|||-(O)_(2)-2KI+2HClarrow (H)_(2)NOuparrow +2(H)_(2)O+2KCl-|||-析出的碘遇淀粉显蓝色。本实验中亚硝酸的用量要准确,若亚硝酸不足,则重氮化作用不完全;-|||-如亚硝酸过量,则会与后面加入的N, 二甲苯胺发生亚硝化反应:-|||-^+ (H3C)2N= bigcirc )= N-OH-|||-.(({H)_(3)C)}_(2)N- 一 NO NaOH NaO bigcirc > +((C{H)_(3))}_(2)NH-|||-HNO2 →(H3C)2N-|||-生成的醌后或亚硝基物夹杂在产品中会使产品颜色暗褐。故正确的做法是:若试纸不显示蓝色,-|||-则应滴加亚硝酸钠溶液至刚刚出现蓝色。继续搅拌,反应15min后再检验。若试纸为蓝色,则应-|||-加入少许尿素分解过量的亚硝酸。-|||-[3]此重氮盐在水中可以电离形成中性内盐( Longrightarrow (({S)_(3)S-square )}^-N-Nequiv N ),在低温下难溶于水-|||-而析出。-|||-[4]用石蕊试纸检查以确保反应混合物为碱性,否则产品色泽不佳。当反应混合物已达碱-|||-性时,若再滴加碱液,则碱液接触反应物表面时将不再产生黄色,此亦可作为判据之一。-|||-[5]若反应物中含有未作用的N, 二甲基苯胺醋酸盐,在加入氢氧化钠后,就会有难溶于水-|||-的N, 二甲基苯胺析出,影响产物的纯度。湿的甲基橙在空气中受光的照射后,颜色很快变深,-|||-所以一般得紫红色粗产物。-|||-[6]重结晶操作应迅速,否则由于产物呈碱性,在温度高时易使产物变质,颜色变深。用乙-|||-醇、乙醚洗涤的目的是使其迅速干燥。-|||-[7]甲基橙的另一制法:在100mL烧杯中放置2.1g磨细的对氨基苯磺酸(0.012mol)和-|||-20mL水,在冰盐浴中冷却至0℃左右;然后加入0.8g磨细的亚硝酸钠,不断搅拌,直到对氨基苯-|||-磺酸全溶为止。sim (5)^circ C 。再将-|||-10mL10%盐酸溶液慢慢滴入其中,边滴加边搅拌,控制温度在 2.偶合-|||-重氮盐的冷的悬浊液中,同时用力搅拌,甲基橙呈红色沉淀析出。滴完后继续在冰浴中搅拌-|||-10min使耦合完全。向反应物中加入 sim 15mL10% 氢氧化钠溶液并搅拌,直至对石蕊试纸显-|||-碱性红色转变为橙色。将反应混合物用热水浴加热至 sim (65)^circ C ,使生成的甲基-|||-橙晶体基本溶解,冷却至室温后再以冰水浴冷却。待结晶完全后抽滤收集晶体,用少量冷水洗-|||-涤,再依次用少量乙醇和少量丙酮(或乙醚)洗涤,压干,得到粗产品。-|||-若要得到较纯产品,可用溶有少量氢氧化钠(约 1.重氮盐与芳胺类化合物发生偶联反应,在什么条件下进行为宜 ()-|||-A.强酸 B.弱酸性和中性 C.弱碱性和中性 D.强碱-|||-2.重氮化反应在下列哪一条件下进行 ()-|||-A.强碱 B.弱酸性和中性 C.弱碱性和中性 D.强酸-|||-3.制备重氮盐的温度范围是 ()-|||-A. sim (5)^circ C B. sim (9)^circ C C. (10sim {15)^circ C} D. sim (20)^circ C-|||-4.检验重氮化反应终点用什么方法 ()-|||-A.淀粉试纸变色 B.刚果红试纸变色-|||-C.石蕊试纸变色 D.酚酞试剂-|||-5.下列关于对氨基苯磺酸的说法错误的是 ()-|||-A.它是两性化合物 B.它的酸性强于碱性,可成内盐-|||-C.加碱后仍可成盐,且增加溶解度 D.它不能进行重氮化反应-|||-6.本实验中重氮盐的制备为什么要控制在 sim (5)^circ C 中进行?-|||-7.试简述甲基橙在酸碱介质中变色的原因,并用反应式表示之。-|||-8.为何重结晶操作应迅速?重结晶时待结晶析出完全后,抽滤收集的沉淀再依次川少量乙-|||-醇和少量丙酮(或乙醚)洗涤的目的是什么?.1sim 0.2g )的沸水进行重结晶。待结晶析出-|||-完全后抽滤收集。沉淀依次用少量乙醇和少量丙酮(或乙醚)洗涤,得到橙色的小叶片状甲基橙-|||-结晶。样品称重后再计算产率。-|||-溶解少许产品于水中,加几滴稀盐酸,然后用稀氢氧化钠溶液中和,观察颜色变化。-|||-[注释][1]对氨基苯磺酸是两性化合物,酸性强于碱性,以内盐形式存在,可与碱作用成盐-|||-而不能与酸成盐。重氮化作用要求在酸性水溶液中进行.故先使其与碱作用生成盐以利溶解。-|||-[2]试纸显蓝色表明有过量的亚硝酸存在,反应为:-|||-(O)_(2)-2KI+2HClarrow (H)_(2)NOuparrow +2(H)_(2)O+2KCl-|||-析出的碘遇淀粉显蓝色。本实验中亚硝酸的用量要准确,若亚硝酸不足,则重氮化作用不完全;-|||-如亚硝酸过量,则会与后面加入的N, 二甲苯胺发生亚硝化反应:-|||-^+ (H3C)2N= bigcirc )= N-OH-|||-.(({H)_(3)C)}_(2)N- 一 NO NaOH NaO bigcirc > +((C{H)_(3))}_(2)NH-|||-HNO2 →(H3C)2N-|||-生成的醌后或亚硝基物夹杂在产品中会使产品颜色暗褐。故正确的做法是:若试纸不显示蓝色,-|||-则应滴加亚硝酸钠溶液至刚刚出现蓝色。继续搅拌,反应15min后再检验。若试纸为蓝色,则应-|||-加入少许尿素分解过量的亚硝酸。-|||-[3]此重氮盐在水中可以电离形成中性内盐( Longrightarrow (({S)_(3)S-square )}^-N-Nequiv N ),在低温下难溶于水-|||-而析出。-|||-[4]用石蕊试纸检查以确保反应混合物为碱性,否则产品色泽不佳。当反应混合物已达碱-|||-性时,若再滴加碱液,则碱液接触反应物表面时将不再产生黄色,此亦可作为判据之一。-|||-[5]若反应物中含有未作用的N, 二甲基苯胺醋酸盐,在加入氢氧化钠后,就会有难溶于水-|||-的N, 二甲基苯胺析出,影响产物的纯度。湿的甲基橙在空气中受光的照射后,颜色很快变深,-|||-所以一般得紫红色粗产物。-|||-[6]重结晶操作应迅速,否则由于产物呈碱性,在温度高时易使产物变质,颜色变深。用乙-|||-醇、乙醚洗涤的目的是使其迅速干燥。-|||-[7]甲基橙的另一制法:在100mL烧杯中放置2.1g磨细的对氨基苯磺酸(0.012mol)和-|||-20mL水,在冰盐浴中冷却至0℃左右;然后加入0.8g磨细的亚硝酸钠,不断搅拌,直到对氨基苯-|||-磺酸全溶为止。sim (5)^circ C 之间。滴完后用碘化钾-|||-淀粉试纸检验,试纸应为蓝色221。继续在冰浴中搅拌15 min使反应完全,可观察到白色细粒状的-|||-重氮盐析出Ⅱ.甲基橙的制备-|||-[反应原理]-|||-NH2 NH2 equiv N 7 N-CH N N-|||-C'H-|||-NaOll NaNO2 Cl Ac-|||-IIC' 11AC-|||-SO3 SO3Na SO3H N(CH3)2-|||-NaO NaO3S 一 =N- 一 -N(CH3)2-|||-[仪器药品]-|||-烧杯、锥形瓶、布氏湔斗、水泵、抽滤装置、滤纸、试管、玻璃棒、滴管、表面皿、酒精灯、温度计、-|||-量筒、铁架台、铁圈、有棉网。-|||-对氨基苯磺酸、5%NaOH溶液、10%NaOH溶液、亚硝酸钠、10%盐酸、 ,N 二甲基苯胺、冰-|||-醋酸、乙醇、丙酮、石蕊试纸、碘化钾一淀粉试纸、尿素。-|||-物理常数-|||-化合物 相对分 性状 比重(d) (℃) ( ) (n) 水 乙醇-|||-熔点 沸点 折光率 溶解度-|||-子质量-|||-对氨基 173.84 白色或灰 280℃时 微溶 不溶-|||-苯磺酸 白色晶体 1.485 分解炭化-|||-白色或微-|||-业硝酸钠 69.05 带浅黄色 2.168 271 320℃以-|||-一 易溶 微溶-|||-晶体 上分解-|||-N,N-二 121.18 淡黄色油 0.9557 2.45 194 1.5582 微溶 易溶-|||-甲基苯胺 状液体-|||-甲 基橙 327.34 橙黄色鳞 微溶易-|||-片状晶体 一 溶于热 不溶-|||-水-|||-1.重氮盐的制备-|||-在100mL烧杯中放置对氨基苯磺酸晶体2.11g(0.01mol)),加入5%氢氧化钠溶液 (L)^111 搅-|||-拌使其溶解。另将0.8g亚硝酸钠溶于6mL水,加入上述溶液中,用冰浴冷却至 2.偶合-|||-重氮盐的冷的悬浊液中,同时用力搅拌,甲基橙呈红色沉淀析出。滴完后继续在冰浴中搅拌-|||-10min使耦合完全。向反应物中加入 sim 15mL10% 氢氧化钠溶液并搅拌,直至对石蕊试纸显-|||-碱性红色转变为橙色。将反应混合物用热水浴加热至 sim (65)^circ C ,使生成的甲基-|||-橙晶体基本溶解,冷却至室温后再以冰水浴冷却。待结晶完全后抽滤收集晶体,用少量冷水洗-|||-涤,再依次用少量乙醇和少量丙酮(或乙醚)洗涤,压干,得到粗产品。-|||-若要得到较纯产品,可用溶有少量氢氧化钠(约 1.重氮盐与芳胺类化合物发生偶联反应,在什么条件下进行为宜 ()-|||-A.强酸 B.弱酸性和中性 C.弱碱性和中性 D.强碱-|||-2.重氮化反应在下列哪一条件下进行 ()-|||-A.强碱 B.弱酸性和中性 C.弱碱性和中性 D.强酸-|||-3.制备重氮盐的温度范围是 ()-|||-A. sim (5)^circ C B. sim (9)^circ C C. (10sim {15)^circ C} D. sim (20)^circ C-|||-4.检验重氮化反应终点用什么方法 ()-|||-A.淀粉试纸变色 B.刚果红试纸变色-|||-C.石蕊试纸变色 D.酚酞试剂-|||-5.下列关于对氨基苯磺酸的说法错误的是 ()-|||-A.它是两性化合物 B.它的酸性强于碱性,可成内盐-|||-C.加碱后仍可成盐,且增加溶解度 D.它不能进行重氮化反应-|||-6.本实验中重氮盐的制备为什么要控制在 sim (5)^circ C 中进行?-|||-7.试简述甲基橙在酸碱介质中变色的原因,并用反应式表示之。-|||-8.为何重结晶操作应迅速?重结晶时待结晶析出完全后,抽滤收集的沉淀再依次川少量乙-|||-醇和少量丙酮(或乙醚)洗涤的目的是什么?.1sim 0.2g )的沸水进行重结晶。待结晶析出-|||-完全后抽滤收集。沉淀依次用少量乙醇和少量丙酮(或乙醚)洗涤,得到橙色的小叶片状甲基橙-|||-结晶。样品称重后再计算产率。-|||-溶解少许产品于水中,加几滴稀盐酸,然后用稀氢氧化钠溶液中和,观察颜色变化。-|||-[注释][1]对氨基苯磺酸是两性化合物,酸性强于碱性,以内盐形式存在,可与碱作用成盐-|||-而不能与酸成盐。重氮化作用要求在酸性水溶液中进行.故先使其与碱作用生成盐以利溶解。-|||-[2]试纸显蓝色表明有过量的亚硝酸存在,反应为:-|||-(O)_(2)-2KI+2HClarrow (H)_(2)NOuparrow +2(H)_(2)O+2KCl-|||-析出的碘遇淀粉显蓝色。本实验中亚硝酸的用量要准确,若亚硝酸不足,则重氮化作用不完全;-|||-如亚硝酸过量,则会与后面加入的N, 二甲苯胺发生亚硝化反应:-|||-^+ (H3C)2N= bigcirc )= N-OH-|||-.(({H)_(3)C)}_(2)N- 一 NO NaOH NaO bigcirc > +((C{H)_(3))}_(2)NH-|||-HNO2 →(H3C)2N-|||-生成的醌后或亚硝基物夹杂在产品中会使产品颜色暗褐。故正确的做法是:若试纸不显示蓝色,-|||-则应滴加亚硝酸钠溶液至刚刚出现蓝色。继续搅拌,反应15min后再检验。若试纸为蓝色,则应-|||-加入少许尿素分解过量的亚硝酸。-|||-[3]此重氮盐在水中可以电离形成中性内盐( Longrightarrow (({S)_(3)S-square )}^-N-Nequiv N ),在低温下难溶于水-|||-而析出。-|||-[4]用石蕊试纸检查以确保反应混合物为碱性,否则产品色泽不佳。当反应混合物已达碱-|||-性时,若再滴加碱液,则碱液接触反应物表面时将不再产生黄色,此亦可作为判据之一。-|||-[5]若反应物中含有未作用的N, 二甲基苯胺醋酸盐,在加入氢氧化钠后,就会有难溶于水-|||-的N, 二甲基苯胺析出,影响产物的纯度。湿的甲基橙在空气中受光的照射后,颜色很快变深,-|||-所以一般得紫红色粗产物。-|||-[6]重结晶操作应迅速,否则由于产物呈碱性,在温度高时易使产物变质,颜色变深。用乙-|||-醇、乙醚洗涤的目的是使其迅速干燥。-|||-[7]甲基橙的另一制法:在100mL烧杯中放置2.1g磨细的对氨基苯磺酸(0.012mol)和-|||-20mL水,在冰盐浴中冷却至0℃左右;然后加入0.8g磨细的亚硝酸钠,不断搅拌,直到对氨基苯-|||-磺酸全溶为止。sim (5)^circ C 。再将-|||-10mL10%盐酸溶液慢慢滴入其中,边滴加边搅拌,控制温度在 2.偶合-|||-重氮盐的冷的悬浊液中,同时用力搅拌,甲基橙呈红色沉淀析出。滴完后继续在冰浴中搅拌-|||-10min使耦合完全。向反应物中加入 sim 15mL10% 氢氧化钠溶液并搅拌,直至对石蕊试纸显-|||-碱性红色转变为橙色。将反应混合物用热水浴加热至 sim (65)^circ C ,使生成的甲基-|||-橙晶体基本溶解,冷却至室温后再以冰水浴冷却。待结晶完全后抽滤收集晶体,用少量冷水洗-|||-涤,再依次用少量乙醇和少量丙酮(或乙醚)洗涤,压干,得到粗产品。-|||-若要得到较纯产品,可用溶有少量氢氧化钠(约 1.重氮盐与芳胺类化合物发生偶联反应,在什么条件下进行为宜 ()-|||-A.强酸 B.弱酸性和中性 C.弱碱性和中性 D.强碱-|||-2.重氮化反应在下列哪一条件下进行 ()-|||-A.强碱 B.弱酸性和中性 C.弱碱性和中性 D.强酸-|||-3.制备重氮盐的温度范围是 ()-|||-A. sim (5)^circ C B. sim (9)^circ C C. (10sim {15)^circ C} D. sim (20)^circ C-|||-4.检验重氮化反应终点用什么方法 ()-|||-A.淀粉试纸变色 B.刚果红试纸变色-|||-C.石蕊试纸变色 D.酚酞试剂-|||-5.下列关于对氨基苯磺酸的说法错误的是 ()-|||-A.它是两性化合物 B.它的酸性强于碱性,可成内盐-|||-C.加碱后仍可成盐,且增加溶解度 D.它不能进行重氮化反应-|||-6.本实验中重氮盐的制备为什么要控制在 sim (5)^circ C 中进行?-|||-7.试简述甲基橙在酸碱介质中变色的原因,并用反应式表示之。-|||-8.为何重结晶操作应迅速?重结晶时待结晶析出完全后,抽滤收集的沉淀再依次川少量乙-|||-醇和少量丙酮(或乙醚)洗涤的目的是什么?.1sim 0.2g )的沸水进行重结晶。待结晶析出-|||-完全后抽滤收集。沉淀依次用少量乙醇和少量丙酮(或乙醚)洗涤,得到橙色的小叶片状甲基橙-|||-结晶。样品称重后再计算产率。-|||-溶解少许产品于水中,加几滴稀盐酸,然后用稀氢氧化钠溶液中和,观察颜色变化。-|||-[注释][1]对氨基苯磺酸是两性化合物,酸性强于碱性,以内盐形式存在,可与碱作用成盐-|||-而不能与酸成盐。重氮化作用要求在酸性水溶液中进行.故先使其与碱作用生成盐以利溶解。-|||-[2]试纸显蓝色表明有过量的亚硝酸存在,反应为:-|||-(O)_(2)-2KI+2HClarrow (H)_(2)NOuparrow +2(H)_(2)O+2KCl-|||-析出的碘遇淀粉显蓝色。本实验中亚硝酸的用量要准确,若亚硝酸不足,则重氮化作用不完全;-|||-如亚硝酸过量,则会与后面加入的N, 二甲苯胺发生亚硝化反应:-|||-^+ (H3C)2N= bigcirc )= N-OH-|||-.(({H)_(3)C)}_(2)N- 一 NO NaOH NaO bigcirc > +((C{H)_(3))}_(2)NH-|||-HNO2 →(H3C)2N-|||-生成的醌后或亚硝基物夹杂在产品中会使产品颜色暗褐。故正确的做法是:若试纸不显示蓝色,-|||-则应滴加亚硝酸钠溶液至刚刚出现蓝色。继续搅拌,反应15min后再检验。若试纸为蓝色,则应-|||-加入少许尿素分解过量的亚硝酸。-|||-[3]此重氮盐在水中可以电离形成中性内盐( Longrightarrow (({S)_(3)S-square )}^-N-Nequiv N ),在低温下难溶于水-|||-而析出。-|||-[4]用石蕊试纸检查以确保反应混合物为碱性,否则产品色泽不佳。当反应混合物已达碱-|||-性时,若再滴加碱液,则碱液接触反应物表面时将不再产生黄色,此亦可作为判据之一。-|||-[5]若反应物中含有未作用的N, 二甲基苯胺醋酸盐,在加入氢氧化钠后,就会有难溶于水-|||-的N, 二甲基苯胺析出,影响产物的纯度。湿的甲基橙在空气中受光的照射后,颜色很快变深,-|||-所以一般得紫红色粗产物。-|||-[6]重结晶操作应迅速,否则由于产物呈碱性,在温度高时易使产物变质,颜色变深。用乙-|||-醇、乙醚洗涤的目的是使其迅速干燥。-|||-[7]甲基橙的另一制法:在100mL烧杯中放置2.1g磨细的对氨基苯磺酸(0.012mol)和-|||-20mL水,在冰盐浴中冷却至0℃左右;然后加入0.8g磨细的亚硝酸钠,不断搅拌,直到对氨基苯-|||-磺酸全溶为止。sim (5)^circ C 之间。滴完后用碘化钾-|||-淀粉试纸检验,试纸应为蓝色221。继续在冰浴中搅拌15 min使反应完全,可观察到白色细粒状的-|||-重氮盐析出


题目解答
答案