题目
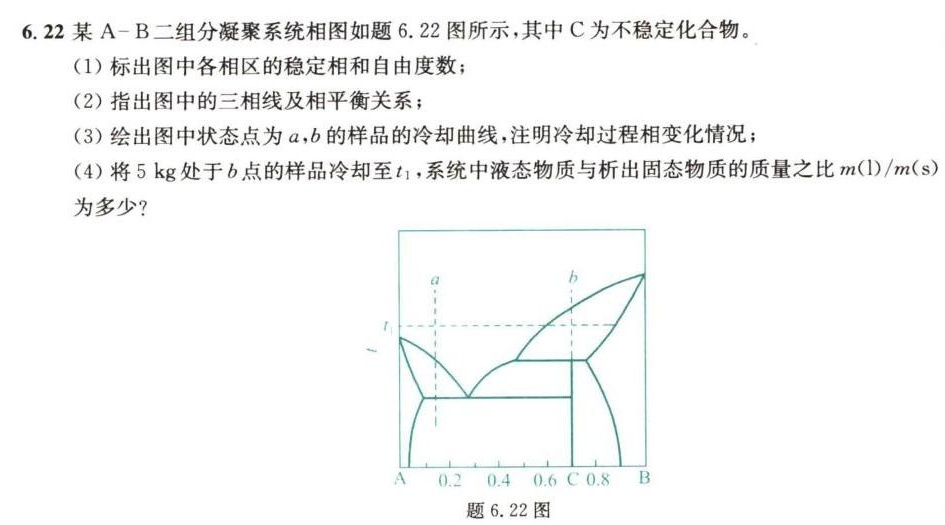
6.22某 A-B 二组分凝聚系统相图如题6.22图所示,其中C为不稳定化合物。-|||-(1)标出图中各相区的稳定相和自由度数;-|||-(2)指出图中的三相线及相平衡关系;-|||-(3)绘出图中状态点为a,b的样品的冷却曲线,注明冷却过程相变化情况;-|||-(4)将5kg处于b点的样品冷却至t1,系统中液态物质与析出固态物质的质量之比 m(1)/m(s)-|||-为多少?-|||-a b-|||-r-|||-A 0.2 0.4 0.6 C 0.8 B-|||-题6.22图
题目解答
答案
解析
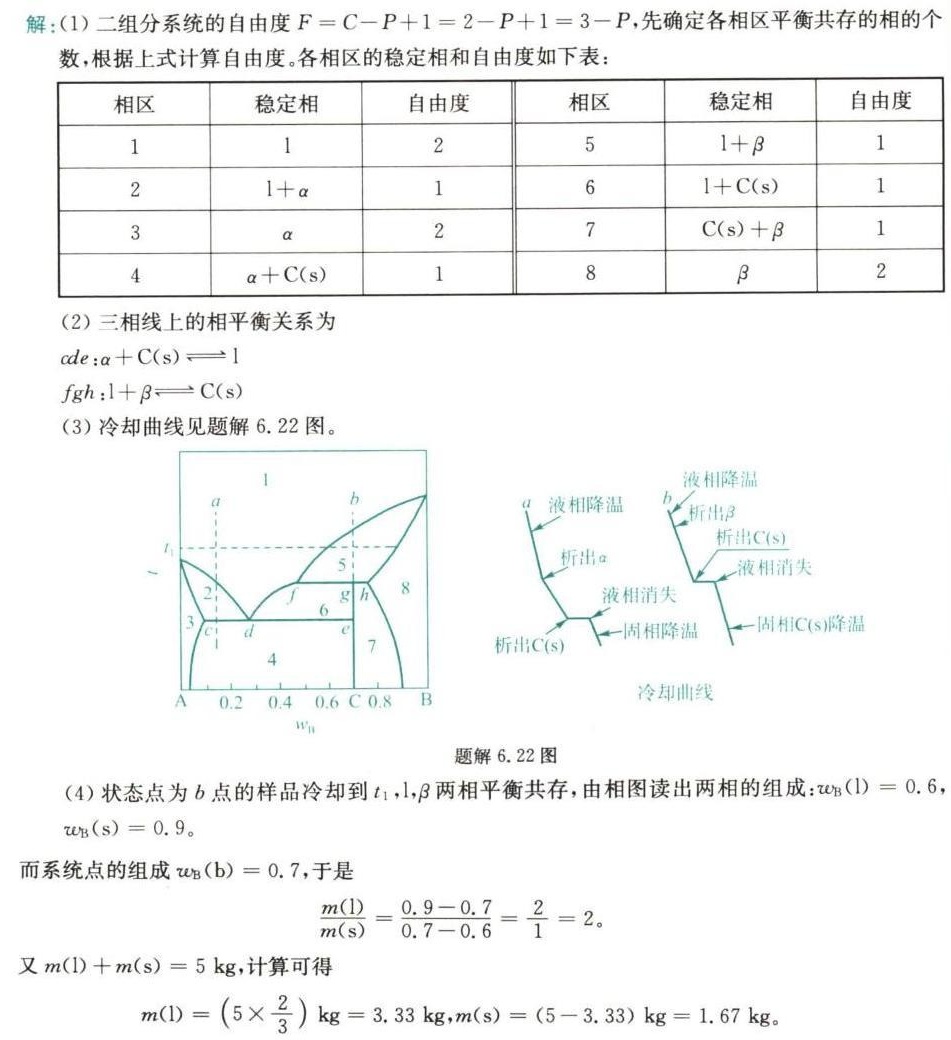
步骤 1:确定各相区的稳定相和自由度数
根据相图,我们可以确定每个相区的稳定相和自由度数。自由度数由相图中的相数决定,相数越多,自由度数越少。在二组分系统中,自由度数F = 2 - P + 1,其中P是相数。
步骤 2:确定三相线及相平衡关系
三相线是相图中相数为3的线,相平衡关系由相图中的相区和相线决定。
步骤 3:绘制冷却曲线
根据相图,我们可以绘制出状态点为a和b的样品的冷却曲线,注明冷却过程中的相变化情况。
步骤 4:计算液态物质与析出固态物质的质量比
根据相图,我们可以计算出将5kg处于b点的样品冷却至t1时,系统中液态物质与析出固态物质的质量比。
根据相图,我们可以确定每个相区的稳定相和自由度数。自由度数由相图中的相数决定,相数越多,自由度数越少。在二组分系统中,自由度数F = 2 - P + 1,其中P是相数。
步骤 2:确定三相线及相平衡关系
三相线是相图中相数为3的线,相平衡关系由相图中的相区和相线决定。
步骤 3:绘制冷却曲线
根据相图,我们可以绘制出状态点为a和b的样品的冷却曲线,注明冷却过程中的相变化情况。
步骤 4:计算液态物质与析出固态物质的质量比
根据相图,我们可以计算出将5kg处于b点的样品冷却至t1时,系统中液态物质与析出固态物质的质量比。