题目
11.298K时电池 (Z)_(2)(Cl)_(2)(b=0.005molcdot (Kg)^-1)|(Hg)_(2)(Cl)_(2)(s) |Hg的电动势为1.227 V。-|||-已知该电池的标准电动势 ^theta =1.031V, 计算 .005molcdot (kg)^-1Zn(Cl)_(2) 溶液的离子平均活度-|||-系数y±。

题目解答
答案
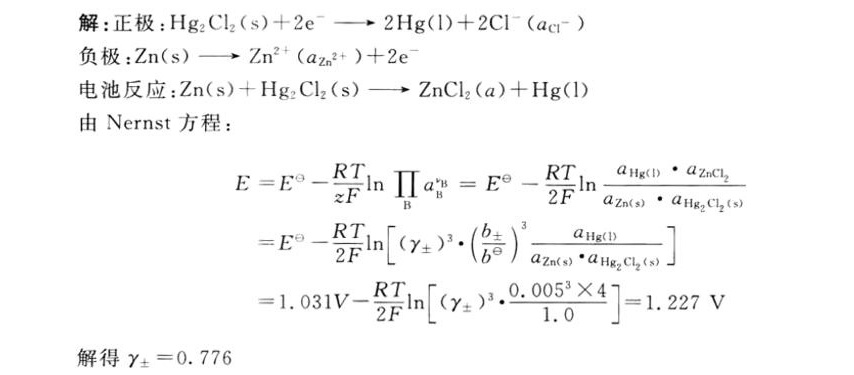
解析
本题考查电池电动势的计算以及离子平均活度系数的求解,解题思路是先根据电池反应写出能斯特方程,再结合离子平均活度与离子平均活度系数、质量摩尔浓度的关系,最后代入已知数据求解离子平均活度系数。
- 写出电池反应和能斯特方程
- 正极反应:$Hg_{2}Cl_{2}(s)+2e^{-}\rightarrow 2Hg(l)+2Cl^{-}(a_{Cl^{-}})$
- 负极反应:$Zn(s)\rightarrow Zn^{2 + }(a_{Zn^{2+}})+2e^{-}$
- 电池反应:$Zn(s)+Hg_{2}Cl_{2}(s)\rightarrow ZnCl_{2}(a)+2Hg(l)$
- 根据能斯特方程$E = E^{\theta}-\frac{RT}{zF}\ln Q$,对于该电池反应$z = 2$,反应商$Q=\frac{a_{ZnCl_{2}}\cdot a_{Hg(l)}^{2}}{a_{Zn(s)}\cdot a_{Hg_{2}Cl_{2}(s)}}$,因为纯固体和纯液体的活度为$1$,所以$Q = a_{ZnCl_{2}}$,则能斯特方程为$E = E^{\theta}-\frac{RT}{2F}\ln a_{ZnCl_{2}}$。
- 计算$ZnCl_{2}$的离子平均活度$a_{\pm}$与离子平均活度系数$\gamma_{\pm}$、质量摩尔浓度$b$的关系
- 对于$ZnCl_{2}$,$v_{+}=1$,$v_{-}=2$,$v = v_{+}+v_{-}=3$。
- 离子平均质量摩尔浓度$b_{\pm}=(b_{+}^{v_{+}}\cdot b_{-}^{v_{-}})^{\frac{1}{v}}$,其中$b_{+}=b = 0.005mol\cdot kg^{-1}$,$b_{-}=2b = 0.01mol\cdot kg^{-1}$,则$b_{\pm}=(b\cdot(2b)^{2})^{\frac{1}{3}}=(4b^{3})^{\frac{1}{3}} = 4^{\frac{1}{3}}b$。
- 离子平均活度$a_{\pm}=\gamma_{\pm}\frac{b_{\pm}}{b^{\theta}}$,$b^{\theta}=1mol\cdot kg^{-1}$,所以$a_{\pm}=\gamma_{\pm}\cdot 4^{\frac{1}{3}}\frac{b}{b^{\theta}}$。
- 而$a_{ZnCl_{2}}=a_{+}^{v_{+}}\cdot a_{-}^{v_{-}}=a_{\pm}^{v}=(\gamma_{\pm}\cdot 4^{\frac{1}{3}}\frac{b}{b^{\theta}})^{3}$。
- 代入数据求解$\gamma_{\pm}$
- 已知$E = 1.227V$,$E^{\theta}=1.031V$,$T = 298K$,$R = 8.314J\cdot mol^{-1}\cdot K^{-1}$,$F = 96485C\cdot mol^{-1}$,代入能斯特方程$E = E^{\theta}-\frac{RT}{2F}\ln a_{ZnCl_{2}}$可得:
$1.227V=1.031V-\frac{8.314J\cdot mol^{-1}\cdot K^{-1}\times298K}{2\times96485C\cdot mol^{-1}}\ln(\gamma_{\pm}\cdot 4^{\frac{1}{3}}\frac{0.005mol\cdot kg^{-1}}{1mol\cdot kg^{-1}})^{3}$ - 先计算$\frac{8.314J\cdot mol^{-1}\cdot K^{-1}\times298K}{2\times96485C\cdot mol^{-1}}\approx0.0128V$,则方程变为:
$1.227V = 1.031V-0.0128V\times3\ln(\gamma_{\pm}\cdot 4^{\frac{1}{3}}\times0.005)$
$1.227V = 1.031V - 0.0384V\times\ln(\gamma_{\pm}\cdot 4^{\frac{1}{3}}\times0.005)$
$0.0384V\times\ln(\gamma_{\pm}\cdot 4^{\frac{1}{3}}\times0.005)=1.031V - 1.227V=-0.196V$
$\ln(\gamma_{\pm}\cdot 4^{\frac{1}{3}}\times0.005)=\frac{-0.196V}{0.0384V}\approx - 5.104$
$\gamma_{\pm}\cdot 4^{\frac{1}{3}}\times0.005 = e^{-5.104}\approx0.006$
$\gamma_{\pm}=\frac{0.006}{4^{\frac{1}{3}}\times0.005}\approx0.776$
- 已知$E = 1.227V$,$E^{\theta}=1.031V$,$T = 298K$,$R = 8.314J\cdot mol^{-1}\cdot K^{-1}$,$F = 96485C\cdot mol^{-1}$,代入能斯特方程$E = E^{\theta}-\frac{RT}{2F}\ln a_{ZnCl_{2}}$可得: