题目
某小组做镁在空气中燃烧的实验时,发现生成物中有少许黑色固体,针对这现象,他们开展了以下探究,请仔细阅读并完成探究报告。【探究目的】探究黑色固体是镁与空气中什么物质反应产生的。【分析猜想】分析空气中各种成分,寻找猜想依据:空气成分一:氧气;空气成分二:水蒸气;空气成分三:氮气;空气成分四:二氧化碳;空气成分五:稀有气体。小组同学认为不可能是稀有气体,因为 ____ 。【实验一】镁带与氧气的反应(1)请写出镁带与氧气反应的文字表达式 ____ 。(2)将燃着的镁条伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。实验结论:镁与氧气反应生成白色的氧化镁。【实验二】镁(粉)与水蒸气的反应(实验装置如图所示)镁粉 干燥管-|||-D-|||-水 。-|||-o-|||-冰水混合物-|||-B-|||-肥皂液-|||-A(1)为了防止玻璃管中原有空气对实验的干扰,实验开始时,应先点燃 ____ (选填“A”或“B”)处精灯。(2)生成的气体通入肥皂液中,用燃着的木条靠近肥泡,有爆鸣声,后有肥皂泡上升到空中,说明生成的气体是 ____ 。实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体。【实验三】镁带与氮气的反应将1.44g打磨光亮的镁带在氮气中充分燃烧,实验结束后,集气瓶内壁附着一层淡黄色的固体,称得其质量为2.00g。实验结论:镁与氮气在点燃的条件下发生化合反应生成黄色的氮化镁,试根据数据求出氮化镁的化学式为 ____ 。【探究结论】根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应产生的,该黑色固体是 ____ (写出化学式)。
某小组做镁在空气中燃烧的实验时,发现生成物中有少许黑色固体,针对这现象,他们开展了以下探究,请仔细阅读并完成探究报告。
【探究目的】探究黑色固体是镁与空气中什么物质反应产生的。
【分析猜想】分析空气中各种成分,寻找猜想依据:
空气成分一:氧气;空气成分二:水蒸气;空气成分三:氮气;空气成分四:二氧化碳;空气成分五:稀有气体。小组同学认为不可能是稀有气体,因为 ____ 。
【实验一】镁带与氧气的反应
(1)请写出镁带与氧气反应的文字表达式 ____ 。
(2)将燃着的镁条伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。
实验结论:镁与氧气反应生成白色的氧化镁。
【实验二】镁(粉)与水蒸气的反应(实验装置如图所示)
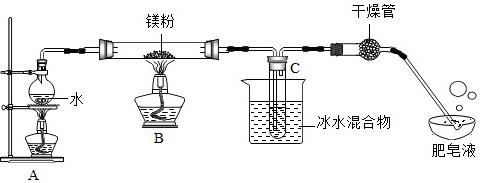
(1)为了防止玻璃管中原有空气对实验的干扰,实验开始时,应先点燃 ____ (选填“A”或“B”)处精灯。
(2)生成的气体通入肥皂液中,用燃着的木条靠近肥泡,有爆鸣声,后有肥皂泡上升到空中,说明生成的气体是 ____ 。
实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体。
【实验三】镁带与氮气的反应
将1.44g打磨光亮的镁带在氮气中充分燃烧,实验结束后,集气瓶内壁附着一层淡黄色的固体,称得其质量为2.00g。
实验结论:镁与氮气在点燃的条件下发生化合反应生成黄色的氮化镁,试根据数据求出氮化镁的化学式为 ____ 。
【探究结论】根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应产生的,该黑色固体是 ____ (写出化学式)。
【探究目的】探究黑色固体是镁与空气中什么物质反应产生的。
【分析猜想】分析空气中各种成分,寻找猜想依据:
空气成分一:氧气;空气成分二:水蒸气;空气成分三:氮气;空气成分四:二氧化碳;空气成分五:稀有气体。小组同学认为不可能是稀有气体,因为 ____ 。
【实验一】镁带与氧气的反应
(1)请写出镁带与氧气反应的文字表达式 ____ 。
(2)将燃着的镁条伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。
实验结论:镁与氧气反应生成白色的氧化镁。
【实验二】镁(粉)与水蒸气的反应(实验装置如图所示)

(1)为了防止玻璃管中原有空气对实验的干扰,实验开始时,应先点燃 ____ (选填“A”或“B”)处精灯。
(2)生成的气体通入肥皂液中,用燃着的木条靠近肥泡,有爆鸣声,后有肥皂泡上升到空中,说明生成的气体是 ____ 。
实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体。
【实验三】镁带与氮气的反应
将1.44g打磨光亮的镁带在氮气中充分燃烧,实验结束后,集气瓶内壁附着一层淡黄色的固体,称得其质量为2.00g。
实验结论:镁与氮气在点燃的条件下发生化合反应生成黄色的氮化镁,试根据数据求出氮化镁的化学式为 ____ 。
【探究结论】根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应产生的,该黑色固体是 ____ (写出化学式)。
题目解答
答案
解:【分析猜想】
小组同学认为不可能是稀有气体,因为稀有气体极不活泼,不能和镁反应。
故答案为:稀有气体极不活泼,不能和镁反应。
【实验一】
(1)镁带与氧气反应生成氧化镁,反应的文字表达式:镁+氧气$\stackrel{点燃}{→}$氧化镁。
故答案为:镁+氧气$\stackrel{点燃}{→}$氧化镁。
【实验二】
(1)为了防止玻璃管中原有空气对实验的干扰,实验开始时,应先点燃A处精灯,利用水蒸气把空气排尽。
故答案为:A。
(2)生成的气体通入肥皂液中,用燃着的木条靠近肥泡,有爆鸣声,后有肥皂泡上升到空中,说明生成的气体是氢气,是因为氢气密度比空气小,燃烧生成水。
故答案为:氢气。
【实验三】
反应的氮气质量:2.00g-1.44g=0.56g,氮化镁中镁原子和氮原子个数比:$\frac{1.44g}{24}$:$\frac{0.56g}{14}$=3:2,氮化镁的化学式为Mg3N2。
故答案为:Mg3N2。
【探究结论】
根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应产生的碳,碳的化学式是C。
故答案为:C。
小组同学认为不可能是稀有气体,因为稀有气体极不活泼,不能和镁反应。
故答案为:稀有气体极不活泼,不能和镁反应。
【实验一】
(1)镁带与氧气反应生成氧化镁,反应的文字表达式:镁+氧气$\stackrel{点燃}{→}$氧化镁。
故答案为:镁+氧气$\stackrel{点燃}{→}$氧化镁。
【实验二】
(1)为了防止玻璃管中原有空气对实验的干扰,实验开始时,应先点燃A处精灯,利用水蒸气把空气排尽。
故答案为:A。
(2)生成的气体通入肥皂液中,用燃着的木条靠近肥泡,有爆鸣声,后有肥皂泡上升到空中,说明生成的气体是氢气,是因为氢气密度比空气小,燃烧生成水。
故答案为:氢气。
【实验三】
反应的氮气质量:2.00g-1.44g=0.56g,氮化镁中镁原子和氮原子个数比:$\frac{1.44g}{24}$:$\frac{0.56g}{14}$=3:2,氮化镁的化学式为Mg3N2。
故答案为:Mg3N2。
【探究结论】
根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应产生的碳,碳的化学式是C。
故答案为:C。
解析
步骤 1:分析猜想
小组同学认为不可能是稀有气体,因为稀有气体极不活泼,不能和镁反应。
步骤 2:实验一
(1)镁带与氧气反应生成氧化镁,反应的文字表达式:镁+氧气$\stackrel{点燃}{→}$氧化镁。
(2)将燃着的镁条伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。
实验结论:镁与氧气反应生成白色的氧化镁。
步骤 3:实验二
(1)为了防止玻璃管中原有空气对实验的干扰,实验开始时,应先点燃A处精灯,利用水蒸气把空气排尽。
(2)生成的气体通入肥皂液中,用燃着的木条靠近肥泡,有爆鸣声,后有肥皂泡上升到空中,说明生成的气体是氢气,是因为氢气密度比空气小,燃烧生成水。
实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体。
步骤 4:实验三
反应的氮气质量:2.00g-1.44g=0.56g,氮化镁中镁原子和氮原子个数比:$\frac{1.44g}{24}$:$\frac{0.56g}{14}$=3:2,氮化镁的化学式为Mg_3N_2。
步骤 5:探究结论
根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应产生的碳,碳的化学式是C。
小组同学认为不可能是稀有气体,因为稀有气体极不活泼,不能和镁反应。
步骤 2:实验一
(1)镁带与氧气反应生成氧化镁,反应的文字表达式:镁+氧气$\stackrel{点燃}{→}$氧化镁。
(2)将燃着的镁条伸入盛满氧气的集气瓶中,产生大量白烟,生成白色固体。
实验结论:镁与氧气反应生成白色的氧化镁。
步骤 3:实验二
(1)为了防止玻璃管中原有空气对实验的干扰,实验开始时,应先点燃A处精灯,利用水蒸气把空气排尽。
(2)生成的气体通入肥皂液中,用燃着的木条靠近肥泡,有爆鸣声,后有肥皂泡上升到空中,说明生成的气体是氢气,是因为氢气密度比空气小,燃烧生成水。
实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体。
步骤 4:实验三
反应的氮气质量:2.00g-1.44g=0.56g,氮化镁中镁原子和氮原子个数比:$\frac{1.44g}{24}$:$\frac{0.56g}{14}$=3:2,氮化镁的化学式为Mg_3N_2。
步骤 5:探究结论
根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应产生的碳,碳的化学式是C。