题目
4.在吸收塔内用清水吸收空气中的SO2,操作条件为常压,30℃,相平衡常数 =26.7 在塔内某一截-|||-面上测得气相中SO2的分压为31mmHg,液相中的SO2浓度为 .05kmol(m)^3, 气相分传质系数 kG=-|||-https:/img.zuoyebang.cc/zyb_5f655e371d8e3fcb8f37f6e46f7743e0.jpg.5kmol((m)^2cdot hcdot am), 液相分传质系数 _(L)=0.39m/h, 溶液密度近似同温度下水的密度。试求在塔内该截面上:-|||-(1)气-液相界面上的浓度 _(1)(kmol/(m)^3) 和pi(atm);-|||-(2)总传质系数KG和KL及相应的推动力。

题目解答
答案
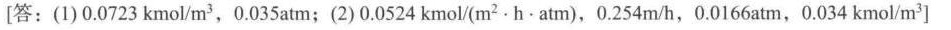
解析
步骤 1:计算气-液相界面上的浓度 ${C}_{1}(kmol/{m}^{3})$ 和pi(atm)
根据相平衡关系,气相中SO2的分压与液相中SO2的浓度之间存在关系:$p_i = m \cdot C_i$,其中 $m$ 是相平衡常数,$p_i$ 是气相中SO2的分压,$C_i$ 是液相中SO2的浓度。
步骤 2:计算总传质系数KG和KL
总传质系数KG和KL可以通过气相分传质系数kG和液相分传质系数kL计算得到。总传质系数KG和KL的计算公式分别为:$KG = \frac{kG}{1 + \frac{kG}{kL} \cdot m}$ 和 $KL = \frac{kL}{1 + \frac{kL}{kG} \cdot \frac{1}{m}}$。
步骤 3:计算相应的推动力
推动力可以通过气相中SO2的分压与液相中SO2的浓度之间的差值计算得到。推动力的计算公式为:$\Delta p = p_i - p_{i,0}$ 和 $\Delta C = C_i - C_{i,0}$,其中 $p_{i,0}$ 和 $C_{i,0}$ 分别是气相和液相中SO2的分压和浓度的初始值。
根据相平衡关系,气相中SO2的分压与液相中SO2的浓度之间存在关系:$p_i = m \cdot C_i$,其中 $m$ 是相平衡常数,$p_i$ 是气相中SO2的分压,$C_i$ 是液相中SO2的浓度。
步骤 2:计算总传质系数KG和KL
总传质系数KG和KL可以通过气相分传质系数kG和液相分传质系数kL计算得到。总传质系数KG和KL的计算公式分别为:$KG = \frac{kG}{1 + \frac{kG}{kL} \cdot m}$ 和 $KL = \frac{kL}{1 + \frac{kL}{kG} \cdot \frac{1}{m}}$。
步骤 3:计算相应的推动力
推动力可以通过气相中SO2的分压与液相中SO2的浓度之间的差值计算得到。推动力的计算公式为:$\Delta p = p_i - p_{i,0}$ 和 $\Delta C = C_i - C_{i,0}$,其中 $p_{i,0}$ 和 $C_{i,0}$ 分别是气相和液相中SO2的分压和浓度的初始值。