题目
已知298K时;_(m)(C(H)_(3)OH,g)=-200.7k/omo(l)^-1_(m)(C(H)_(3)OH,g)=-200.7k/omo(l)^-1试计算此时反应C(石墨)+2H2(g)+_(m)(C(H)_(3)OH,g)=-200.7k/omo(l)^-1的熵变。
已知298K时;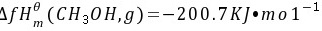
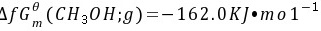 试计算此时反应
试计算此时反应
C(石墨)+2H2(g)+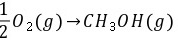 的熵变。
的熵变。
题目解答
答案
解: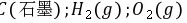 的
的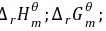 均为零
均为零
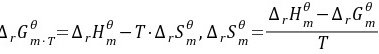
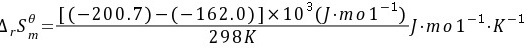
=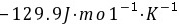
解析
步骤 1:确定反应物和生成物的标准摩尔生成焓
根据题目给出的信息,反应物C(石墨)、H2(g)、O2(g)的标准摩尔生成焓为零,而生成物CH3OH(g)的标准摩尔生成焓为-200.7 kJ/mol。
步骤 2:计算反应的焓变
反应的焓变ΔrHmθ可以通过反应物和生成物的标准摩尔生成焓计算得出。由于反应物的标准摩尔生成焓为零,所以反应的焓变等于生成物的标准摩尔生成焓,即ΔrHmθ = -200.7 kJ/mol。
步骤 3:计算反应的吉布斯自由能变
反应的吉布斯自由能变ΔrGmθ可以通过反应物和生成物的标准摩尔生成吉布斯自由能计算得出。由于反应物的标准摩尔生成吉布斯自由能为零,所以反应的吉布斯自由能变等于生成物的标准摩尔生成吉布斯自由能,即ΔrGmθ = -162.0 kJ/mol。
步骤 4:计算反应的熵变
反应的熵变ΔrSmθ可以通过反应的焓变和吉布斯自由能变计算得出。根据公式ΔrGmθ = ΔrHmθ - TΔrSmθ,可以解出ΔrSmθ = (ΔrHmθ - ΔrGmθ) / T。将已知数值代入,得到ΔrSmθ = (-200.7 kJ/mol - (-162.0 kJ/mol)) / 298 K = -129.9 J/mol·K。
根据题目给出的信息,反应物C(石墨)、H2(g)、O2(g)的标准摩尔生成焓为零,而生成物CH3OH(g)的标准摩尔生成焓为-200.7 kJ/mol。
步骤 2:计算反应的焓变
反应的焓变ΔrHmθ可以通过反应物和生成物的标准摩尔生成焓计算得出。由于反应物的标准摩尔生成焓为零,所以反应的焓变等于生成物的标准摩尔生成焓,即ΔrHmθ = -200.7 kJ/mol。
步骤 3:计算反应的吉布斯自由能变
反应的吉布斯自由能变ΔrGmθ可以通过反应物和生成物的标准摩尔生成吉布斯自由能计算得出。由于反应物的标准摩尔生成吉布斯自由能为零,所以反应的吉布斯自由能变等于生成物的标准摩尔生成吉布斯自由能,即ΔrGmθ = -162.0 kJ/mol。
步骤 4:计算反应的熵变
反应的熵变ΔrSmθ可以通过反应的焓变和吉布斯自由能变计算得出。根据公式ΔrGmθ = ΔrHmθ - TΔrSmθ,可以解出ΔrSmθ = (ΔrHmθ - ΔrGmθ) / T。将已知数值代入,得到ΔrSmθ = (-200.7 kJ/mol - (-162.0 kJ/mol)) / 298 K = -129.9 J/mol·K。