(10分)钠及其化合物在人类生产生活中有着重大的作用。金属钠要隔绝空气密封保存,请用化学方程式表示原因(Na参与的反应) ______________、______________。I.加热条件下,Na可以在氧气中燃烧,反应的化学方程式为_________; 现象是_______。某课外活动小组设计了如图装置,证实二氧化碳跟过氧化钠反应时需要与水接触。K1 ⑤-|||-盐酸 碱石灰-|||-K 过氧化钠 a= 带火星的木条-|||-⑥-|||-④-|||-CaCO-|||-① ② ③(装置分析)(1)装置①中反应的离子方程式是________。(2)装置②中的试剂是为了除去CO2中混有的HCl,则可选用的试剂为_________。a.饱和NaOH溶液 b. 饱和Na2CO3溶液 c.饱和NaHCO3溶液(3)装置③中的试剂是___________。(进行实验)步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。(4)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是_______、_______。(5)过氧化钠跟二氧化碳反应的化学方程式并用双线桥标出电子转移:_________。(6)若要证明CO2和Na2O2发生了反应,需要取出少量反应后的固体,______________(请补全实验方案)。Ⅱ.(7)面粉发酵时会产生有机酸(用HA表示其化学式,HA酸性强于碳酸),影响口感。我们可以加入膨松剂(主要含NaHCO3),那么蒸出来的馒头蓬松柔软,且口感好。若加入过量的膨松剂,请写出蒸馒头时反应的化学方程式_______,_______。该过程能体现出Na2CO3和NaHCO3的热稳定性_________>_________。
(10分)钠及其化合物在人类生产生活中有着重大的作用。金属钠要隔绝空气密封保存,请用化学方程式表示原因(Na参与的反应) ______________、______________。
I.加热条件下,Na可以在氧气中燃烧,反应的化学方程式为_________; 现象是_______。某课外活动小组设计了如图装置,证实二氧化碳跟过氧化钠反应时需要与水接触。
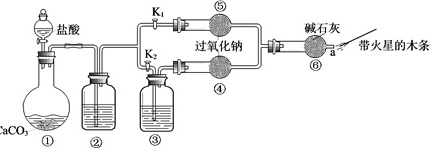
(装置分析)
(1)装置①中反应的离子方程式是________。
(2)装置②中的试剂是为了除去CO2中混有的HCl,则可选用的试剂为_________。
a.饱和NaOH溶液 b. 饱和Na2CO3溶液 c.饱和NaHCO3溶液
(3)装置③中的试剂是___________。
(进行实验)
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。
(4)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是_______、_______。
(5)过氧化钠跟二氧化碳反应的化学方程式并用双线桥标出电子转移:_________。
(6)若要证明CO2和Na2O2发生了反应,需要取出少量反应后的固体,______________(请补全实验方案)。
Ⅱ.(7)面粉发酵时会产生有机酸(用HA表示其化学式,HA酸性强于碳酸),影响口感。我们可以加入膨松剂(主要含NaHCO3),那么蒸出来的馒头蓬松柔软,且口感好。若加入过量的膨松剂,请写出蒸馒头时反应的化学方程式_______,_______。该过程能体现出Na2CO3和NaHCO3的热稳定性_________>_________。
题目解答
答案
[答案]4Na+O2=2Na2O 2Na+2H2O=2NaOH+H2↑ Na先熔化成闪亮的小球,然后剧烈燃烧,最终生成淡黄色的固体 2Na+O2 Na2O2 CaCO3+2H+═Ca2++H2O+CO2↑ c 浓硫酸 木条不复燃 木条复燃
Na2O2 CaCO3+2H+═Ca2++H2O+CO2↑ c 浓硫酸 木条不复燃 木条复燃 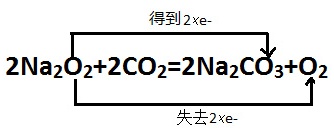 加入稀盐酸,将产生的气体通入澄清的石灰水中(或加BaCl2溶液等体现检验
加入稀盐酸,将产生的气体通入澄清的石灰水中(或加BaCl2溶液等体现检验 的方法即可) NaHCO3+HA=NaA+H2O+CO2↑ 2 NaHCO3
的方法即可) NaHCO3+HA=NaA+H2O+CO2↑ 2 NaHCO3 Na2CO3+H2O+CO2↑ Na2CO3 NaHCO3
Na2CO3+H2O+CO2↑ Na2CO3 NaHCO3
解析
金属钠在空气中会与氧气反应生成氧化钠,与水反应生成氢氧化钠和氢气,因此需要隔绝空气密封保存。
步骤 2:钠在氧气中燃烧的化学方程式
钠在氧气中燃烧生成过氧化钠,反应的化学方程式为:2Na + O2 → Na2O2。
步骤 3:钠在氧气中燃烧的现象
钠在氧气中燃烧时,钠先熔化成闪亮的小球,然后剧烈燃烧,最终生成淡黄色的固体。
步骤 4:装置①中反应的离子方程式
装置①中碳酸钙与盐酸反应生成二氧化碳气体,反应的离子方程式为:CaCO3 + 2H+ → Ca2+ + H2O + CO2↑。
步骤 5:装置②中试剂的选择
装置②中试剂是为了除去CO2中混有的HCl,应选用饱和NaHCO3溶液,因为NaHCO3可以与HCl反应生成CO2,而不会引入新的杂质。
步骤 6:装置③中的试剂
装置③中的试剂是浓硫酸,用于干燥二氧化碳气体。
步骤 7:步骤1和步骤2中a处带火星的木条现象
步骤1中,由于CO2中混有HCl,带火星的木条不复燃;步骤2中,由于CO2中没有HCl,带火星的木条复燃。
步骤 8:过氧化钠跟二氧化碳反应的化学方程式
过氧化钠跟二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2 + 2CO2 → 2Na2CO3 + O2。
步骤 9:证明CO2和Na2O2发生了反应的实验方案
取出少量反应后的固体,加入稀盐酸,将产生的气体通入澄清的石灰水中,若石灰水变浑浊,则证明CO2和Na2O2发生了反应。
步骤 10:蒸馒头时反应的化学方程式
蒸馒头时,NaHCO3与有机酸反应生成NaA、H2O和CO2,反应的化学方程式为:NaHCO3 + HA → NaA + H2O + CO2↑;若加入过量的膨松剂,NaHCO3受热分解生成Na2CO3、H2O和CO2,反应的化学方程式为:2NaHCO3 → Na2CO3 + H2O + CO2↑。
步骤 11:Na2CO3和NaHCO3的热稳定性
Na2CO3的热稳定性大于NaHCO3。