题目
7.下列离子方程式中,正确的是 () 。-|||-A.将稀硫酸滴在铁片上: +6(H)^+=!=!= 2(Fe)^3++3(H)_(2)uparrow -|||-B.将碳酸氢钠溶液与稀盐酸混合: (HC{O)_(3)}^-+(H)^+=!=!= (H)_(2)O+C(O)_(2)uparrow 7.下列离子方程式中,正确的是 () 。-|||-A.将稀硫酸滴在铁片上: +6(H)^+=!=!= 2(Fe)^3++3(H)_(2)uparrow -|||-B.将碳酸氢钠溶液与稀盐酸混合: (HC{O)_(3)}^-+(H)^+=!=!= (H)_(2)O+C(O)_(2)uparrow
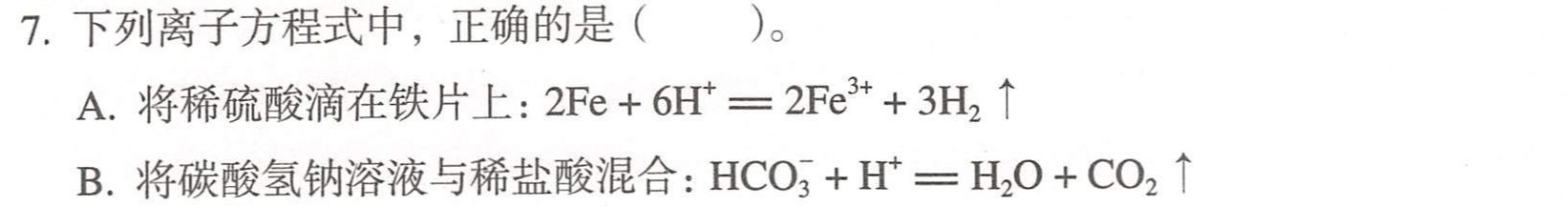

题目解答
答案
B. 将碳酸氢钠溶液与稀盐酸混合: ${HC{O}_{3}}^{-}+{H}^{+}=\!=\!= {H}_{2}O+C{O}_{2}\uparrow $
解析
本题考查离子方程式的书写是否正确,需掌握以下关键点:
- 强弱电解质的拆分:强电解质(如强酸、强碱、可溶性盐)需拆解为离子,弱电解质(如弱酸、难溶物)保持分子形式。
- 反应的实质:离子间直接结合生成沉淀、气体或水的反应,需写出实际参与反应的离子。
- 产物的准确性:根据反应物性质判断产物的正确价态(如铁与酸反应生成Fe²⁺而非Fe³⁺)。
选项A
错误。铁与稀硫酸反应生成Fe²⁺而非Fe³⁺,正确方程式应为:
$Fe + 2H^+ \rightarrow Fe^{2+} + H_2 \uparrow$
选项B
正确。碳酸氢钠中的HCO₃⁻与盐酸中的H⁺反应生成水和CO₂:
$HCO_3^- + H^+ \rightarrow H_2O + CO_2 \uparrow$
选项C
错误。硫酸铜(CuSO₄)为可溶性盐,应拆分为Cu²⁺和SO₄²⁻,正确方程式应为:
$Cu^{2+} + 2OH^- \rightarrow Cu(OH)_2 \downarrow$
选项D
错误。硝酸银(AgNO₃)应拆分为Ag⁺和NO₃⁻,正确方程式应为:
$Ag^+ + Cl^- \rightarrow AgCl \downarrow$
选项中未拆分AgNO₃,书写不规范。