题目
在25℃时1 mol O2从1000 kPa自由膨胀到100 kPa,求此过程的ΔU、ΔH、ΔS,ΔA、ΔG(设O2为理想气体)。
在25℃时1 mol O2从1000 kPa自由膨胀到100 kPa,求此过程的ΔU、ΔH、ΔS,ΔA、ΔG(设O2为理想气体)。
题目解答
答案
解:U = 0,H = 0,
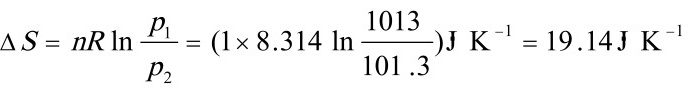
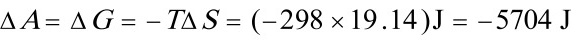
解析
考查要点:本题主要考查理想气体在自由膨胀过程中的热力学函数变化,包括内能(ΔU)、焓(ΔH)、熵变(ΔS)、赫姆霍兹自由能(ΔA)和吉布斯自由能(ΔG)的计算。
解题核心思路:
- 理想气体性质:内能(U)和焓(H)仅是温度的函数。若温度不变,则ΔU=0,ΔH=0。
- 自由膨胀特点:无外界做功(W=0),且过程迅速,通常视为绝热过程。对于理想气体,绝热自由膨胀中ΔU=0,温度不变。
- 熵变计算:利用理想气体状态方程,通过压力或体积的变化计算熵变ΔS。
- 自由能计算:根据公式ΔA=ΔU−TΔS和ΔG=ΔH−TΔS,结合已知量代入求解。
破题关键点:
- 明确自由膨胀中温度不变,直接得出ΔU=0,ΔH=0。
- 正确应用理想气体熵变公式ΔS = nR ln(P₁/P₂)。
- 注意单位统一(温度用开尔文,压力比值需为同单位)。
1. ΔU和ΔH的计算
- 理想气体性质:内能U和焓H仅与温度有关。题目中未涉及温度变化(自由膨胀为绝热过程,ΔU=0),因此:
$\Delta U = 0, \quad \Delta H = 0$
2. ΔS的计算
- 公式选择:理想气体在温度不变时,熵变可通过压力变化计算:
$\Delta S = nR \ln \frac{P_1}{P_2}$ - 代入数据:n=1 mol,R=8.314 J/mol·K,P₁=1000 kPa,P₂=100 kPa:
$\Delta S = 1 \times 8.314 \times \ln \frac{1000}{100} = 8.314 \times \ln 10 \approx 19.14 \, \text{J/K}$
3. ΔA和ΔG的计算
- 赫姆霍兹自由能:
$\Delta A = \Delta U - T\Delta S = 0 - 298 \times 19.14 \approx -5704 \, \text{J}$ - 吉布斯自由能:
$\Delta G = \Delta H - T\Delta S = 0 - 298 \times 19.14 \approx -5704 \, \text{J}$