题目
实验室需要配制1200cm3防冻溶液,它由30%的甲醇(1)和70%的H2O(2)(摩尔比)组成。试求需要多少体积的25℃的甲醇与水混合。已知甲醇和水在25℃、30%(摩尔分数)的甲醇溶液的偏摩尔体积: overline ({V)_(1)}=38.632(cm)^3/mol , overline ({V)_(2)}=17.765(cm)^3/mol 。25℃下纯物质的体积:-|||-_(1)=40.727(cm)^3/mol , _(2)=18.068(cm)^3/mol 。
实验室需要配制1200cm3防冻溶液,它由30%的甲醇(1)和70%的H2O(2)(摩尔比)组成。试求需要多少体积的25℃的甲醇与水混合。已知甲醇和水在25℃、30%(摩尔分数)的甲醇溶液的偏摩尔体积: 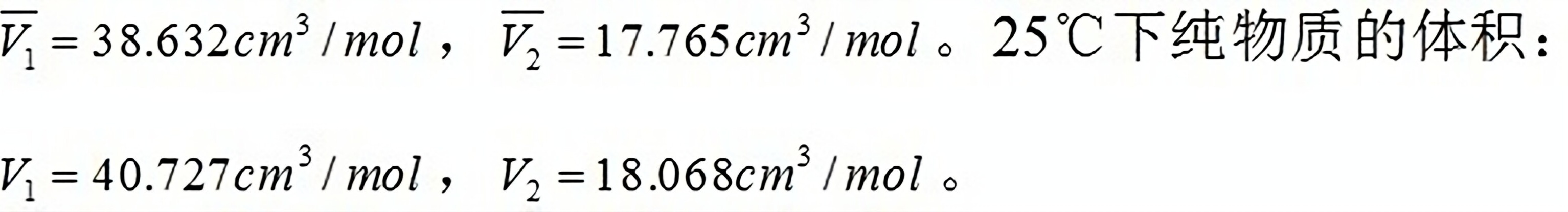
题目解答
答案

解析
步骤 1:计算混合溶液的平均摩尔体积
根据题目给出的偏摩尔体积,我们可以计算出混合溶液的平均摩尔体积。混合溶液的平均摩尔体积 $V$ 可以通过以下公式计算:
$$
V = x_1 \overline{V_1} + x_2 \overline{V_2}
$$
其中,$x_1$ 和 $x_2$ 分别是甲醇和水的摩尔分数,$\overline{V_1}$ 和 $\overline{V_2}$ 分别是甲醇和水的偏摩尔体积。代入题目给出的数值,我们得到:
$$
V = 0.3 \times 38.632 + 0.7 \times 17.765 = 24.03 \text{ cm}^3/\text{mol}
$$
步骤 2:计算所需物质的量
根据题目要求,需要配制1200 cm^3的防冻溶液。因此,我们可以计算出所需物质的量 $n$:
$$
n = \frac{1200}{24.03} = 49.95 \text{ mol}
$$
步骤 3:计算所需甲醇和水的物质的量
根据题目给出的摩尔比,我们可以计算出所需甲醇和水的物质的量。甲醇的物质的量 $n_1$ 和水的物质的量 $n_2$ 分别为:
$$
n_1 = 0.3 \times 49.95 = 14.985 \text{ mol}
$$
$$
n_2 = 0.7 \times 49.95 = 34.965 \text{ mol}
$$
步骤 4:计算所需甲醇和水的体积
根据题目给出的纯物质体积,我们可以计算出所需甲醇和水的体积。甲醇的体积 $V_1$ 和水的体积 $V_2$ 分别为:
$$
V_1 = 14.985 \times 40.727 = 610.29 \text{ cm}^3
$$
$$
V_2 = 34.965 \times 18.068 = 631.75 \text{ cm}^3
$$
步骤 5:计算混合后生成的溶液体积
将两种组分的体积简单加和,得到混合后生成的溶液体积 $V_{total}$:
$$
V_{total} = V_1 + V_2 = 610.29 + 631.75 = 1242.04 \text{ cm}^3
$$
步骤 6:计算混合后生成的溶液体积缩小的百分比
根据题目要求,我们需要计算混合后生成的溶液体积缩小的百分比。混合后生成的溶液体积缩小的百分比为:
$$
\frac{1242.04 - 1200}{1200} = 3.503\%
$$
根据题目给出的偏摩尔体积,我们可以计算出混合溶液的平均摩尔体积。混合溶液的平均摩尔体积 $V$ 可以通过以下公式计算:
$$
V = x_1 \overline{V_1} + x_2 \overline{V_2}
$$
其中,$x_1$ 和 $x_2$ 分别是甲醇和水的摩尔分数,$\overline{V_1}$ 和 $\overline{V_2}$ 分别是甲醇和水的偏摩尔体积。代入题目给出的数值,我们得到:
$$
V = 0.3 \times 38.632 + 0.7 \times 17.765 = 24.03 \text{ cm}^3/\text{mol}
$$
步骤 2:计算所需物质的量
根据题目要求,需要配制1200 cm^3的防冻溶液。因此,我们可以计算出所需物质的量 $n$:
$$
n = \frac{1200}{24.03} = 49.95 \text{ mol}
$$
步骤 3:计算所需甲醇和水的物质的量
根据题目给出的摩尔比,我们可以计算出所需甲醇和水的物质的量。甲醇的物质的量 $n_1$ 和水的物质的量 $n_2$ 分别为:
$$
n_1 = 0.3 \times 49.95 = 14.985 \text{ mol}
$$
$$
n_2 = 0.7 \times 49.95 = 34.965 \text{ mol}
$$
步骤 4:计算所需甲醇和水的体积
根据题目给出的纯物质体积,我们可以计算出所需甲醇和水的体积。甲醇的体积 $V_1$ 和水的体积 $V_2$ 分别为:
$$
V_1 = 14.985 \times 40.727 = 610.29 \text{ cm}^3
$$
$$
V_2 = 34.965 \times 18.068 = 631.75 \text{ cm}^3
$$
步骤 5:计算混合后生成的溶液体积
将两种组分的体积简单加和,得到混合后生成的溶液体积 $V_{total}$:
$$
V_{total} = V_1 + V_2 = 610.29 + 631.75 = 1242.04 \text{ cm}^3
$$
步骤 6:计算混合后生成的溶液体积缩小的百分比
根据题目要求,我们需要计算混合后生成的溶液体积缩小的百分比。混合后生成的溶液体积缩小的百分比为:
$$
\frac{1242.04 - 1200}{1200} = 3.503\%
$$