题目
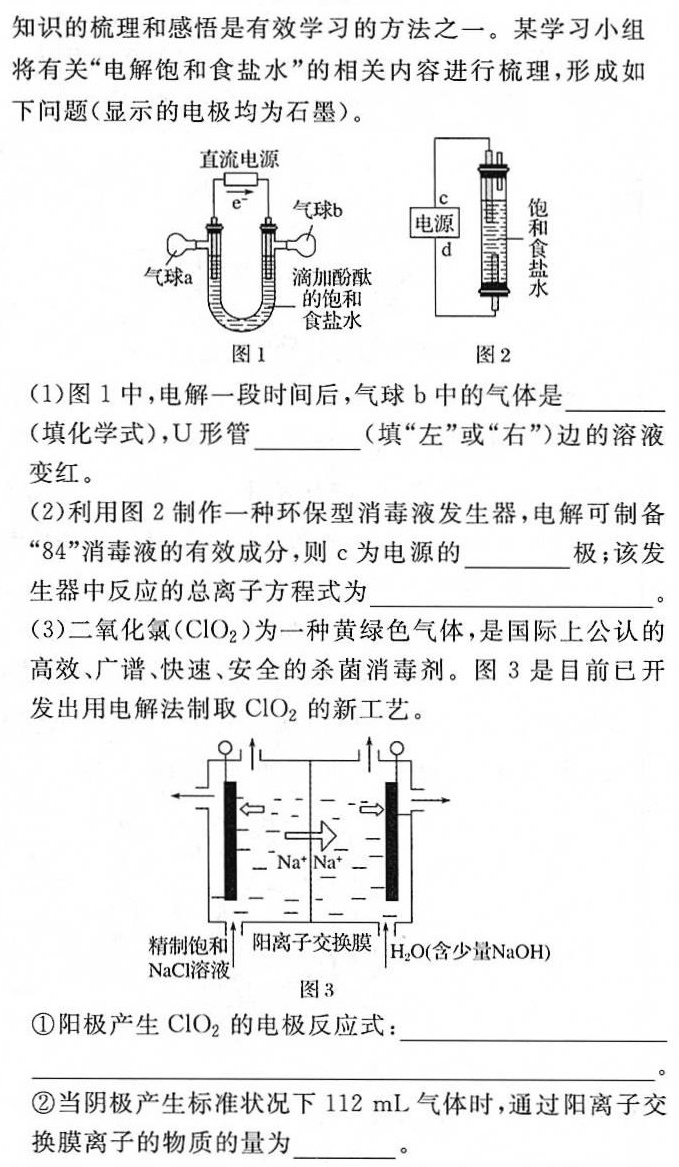
知识的梳理和感悟是有效学习的方法之一。某学习小组-|||-将有关"电解饱和食盐水"的相关内容进行梳理,形成如-|||-下问题(显示的电极均为石墨)。-|||-直流电源 血-|||-e 气球b 电源 食-|||-c-|||-d-|||-气球a 滴加酚酞-|||-的饱和-|||-盐水-|||-图1 图2-|||-(1)图1中,电解一段时间后,气球b中的气体是 __-|||-(填化学式),U形管 __ (填"左"或"右`)边的溶液-|||-变红。-|||-(2)利用图2制作一种环保型消毒液发生器,电解可制备-|||-"84"消毒液的有效成分,则c为电源的 __ 极;该发-|||-生器中反应的总离子方程式为 __ 。-|||-(3)二氧化氯(ClO 2)为一种黄绿色气体,是国际上公认的-|||-高效、广谱、快速、安全的杀菌消毒剂。图3是目前已开-|||-发出用电解法制取ClO2的新工艺。-|||-__ ↑O-|||-7-|||-Na^+ Na^+-|||-二-|||-精制饱和 阳离子交换膜 H2O(含少量NaOH)-|||-NaCl溶液-|||-图3-|||-①阳极产生ClO2的电极反应式: __-|||-②当阴极产生标准状况下112mL气体时,通过阳离子交-|||-换膜离子的物质的量为 __ 。
题目解答
答案

解析
步骤 1:图1中电解过程分析
在图1中,电解饱和食盐水,阳极(气球b)产生氯气(Cl2),阴极(气球a)产生氢气(H2)。由于阴极附近生成NaOH,U形管右边的溶液变红(酚酞遇碱变红)。
步骤 2:图2中电解过程分析
在图2中,电解饱和食盐水,c为电源的负极,d为正极。电解过程中,氯离子(Cl-)在阳极放电生成氯气(Cl2),氢离子(H+)在阴极放电生成氢气(H2),同时生成NaOH。反应的总离子方程式为:${Cl}^{-}+{H}_{2}O\xlongequal {通电}{ClO}^{-}+{H}_{2}\uparrow $。
步骤 3:图3中电解过程分析
在图3中,阳极产生ClO2,电极反应式为:${Cl}^{-}-5{e}^{-}+2{H}_{2}O=\!=\!= Cl{O}_{2}\uparrow +4{H}^{+}$。阴极产生氢气,电极反应式为:$2{H}_{2}O+2{e}^{-}=\!=\!= {H}_{2}\uparrow +2O{H}^{-}$。当阴极产生标准状况下112mL气体时,即0.005mol氢气,通过阳离子交换膜的离子为0.01mol(因为每生成1mol氢气,需要2mol氢离子通过阳离子交换膜)。
在图1中,电解饱和食盐水,阳极(气球b)产生氯气(Cl2),阴极(气球a)产生氢气(H2)。由于阴极附近生成NaOH,U形管右边的溶液变红(酚酞遇碱变红)。
步骤 2:图2中电解过程分析
在图2中,电解饱和食盐水,c为电源的负极,d为正极。电解过程中,氯离子(Cl-)在阳极放电生成氯气(Cl2),氢离子(H+)在阴极放电生成氢气(H2),同时生成NaOH。反应的总离子方程式为:${Cl}^{-}+{H}_{2}O\xlongequal {通电}{ClO}^{-}+{H}_{2}\uparrow $。
步骤 3:图3中电解过程分析
在图3中,阳极产生ClO2,电极反应式为:${Cl}^{-}-5{e}^{-}+2{H}_{2}O=\!=\!= Cl{O}_{2}\uparrow +4{H}^{+}$。阴极产生氢气,电极反应式为:$2{H}_{2}O+2{e}^{-}=\!=\!= {H}_{2}\uparrow +2O{H}^{-}$。当阴极产生标准状况下112mL气体时,即0.005mol氢气,通过阳离子交换膜的离子为0.01mol(因为每生成1mol氢气,需要2mol氢离子通过阳离子交换膜)。