题目
电解 /L(H)_(2)S(O)_(4) 和 .1mol/LCuS(O)_(4) 混合溶液,当 ^2+ 离子的浓度已降低到 ^-7-|||-.mol/L 时,阴极的电位等于多少?若已知氢在铜上析出的过电位是0.23V,试问在不让氢析-|||-出的条件下,阴极电位最低能达到多少?

题目解答
答案
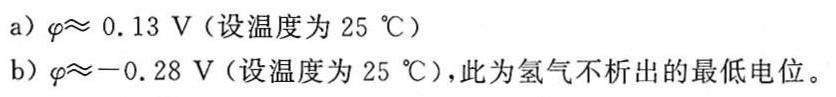
解析
步骤 1:确定阴极电位
在电解过程中,阴极电位由阴极反应决定。对于铜离子的还原反应,阴极电位可以通过能斯特方程计算。能斯特方程为:
$$
\varphi = \varphi^{\circ} - \frac{RT}{nF} \ln Q
$$
其中,$\varphi^{\circ}$ 是标准电极电位,$R$ 是气体常数,$T$ 是温度,$n$ 是电子转移数,$F$ 是法拉第常数,$Q$ 是反应商。
对于铜离子的还原反应,标准电极电位 $\varphi^{\circ} = 0.34 V$,$n = 2$,$Q = [Cu^{2+}]$。
步骤 2:计算阴极电位
将已知数据代入能斯特方程,计算阴极电位。
$$
\varphi = 0.34 V - \frac{8.314 J/(mol\cdot K) \times 298 K}{2 \times 96485 C/mol} \ln (10^{-7})
$$
步骤 3:计算氢气析出的最低电位
氢气在铜上析出的过电位是0.23V,因此氢气析出的最低电位为:
$$
\varphi_{H_{2}} = \varphi_{H^{+}/H_{2}} - \eta_{H_{2}}
$$
其中,$\varphi_{H^{+}/H_{2}}$ 是氢离子的标准电极电位,$\eta_{H_{2}}$ 是氢气的过电位。
在电解过程中,阴极电位由阴极反应决定。对于铜离子的还原反应,阴极电位可以通过能斯特方程计算。能斯特方程为:
$$
\varphi = \varphi^{\circ} - \frac{RT}{nF} \ln Q
$$
其中,$\varphi^{\circ}$ 是标准电极电位,$R$ 是气体常数,$T$ 是温度,$n$ 是电子转移数,$F$ 是法拉第常数,$Q$ 是反应商。
对于铜离子的还原反应,标准电极电位 $\varphi^{\circ} = 0.34 V$,$n = 2$,$Q = [Cu^{2+}]$。
步骤 2:计算阴极电位
将已知数据代入能斯特方程,计算阴极电位。
$$
\varphi = 0.34 V - \frac{8.314 J/(mol\cdot K) \times 298 K}{2 \times 96485 C/mol} \ln (10^{-7})
$$
步骤 3:计算氢气析出的最低电位
氢气在铜上析出的过电位是0.23V,因此氢气析出的最低电位为:
$$
\varphi_{H_{2}} = \varphi_{H^{+}/H_{2}} - \eta_{H_{2}}
$$
其中,$\varphi_{H^{+}/H_{2}}$ 是氢离子的标准电极电位,$\eta_{H_{2}}$ 是氢气的过电位。