2.磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在.它的单质和化合物在工农业生产中有着重要的应用.Ⅰ.白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在电炉中高温(约1550℃)下通过下面两个反应共熔得到.①2Ca3(PO4)2(s)+5C(s)=6CaO(s)+P4(s)+5CO2(g)△H1=+Ql kJ•mol-1②CaO(s)+SiO2(s)=CaSiO3(s)△H2=-Q2 kJ•mol-1(1)写出电炉中发生总反应的热化学方程式2Ca3(PO4)2(s)+6SiO2(s)+5C(s)高温_" role="presentation" style="font-size: 122%; position: relative;">高温–––––––高温_6CaSiO3(s)+P4(s)+5CO2(g))△H=(Ql-6Q2 )kJ•mol-1Ⅱ.三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料.氯化水解法生产三氯氧磷的流程如图甲:氯气-|||-三氯化磷 三氯氧磷-|||-反应釜 冷凝器-|||-水 吸收塔 → 副产品-|||-甲-|||-0.4 -1 100 0.5 7100-|||-0.3 80 0.4 . 80-|||-残留溶解性 残留溶解性-|||-浓度 60 .3k , 浓度 60-|||-0.2-|||-→ 回收率-|||-、 40 0.2 → 回收率 40-|||-0.1 20 .1k 20-|||-HH 1-|||-8 8.5 9 9.5 10 10.5 ll 12 0 5 10 30 60 120 180-|||-pH 反应时间(min)-|||-图1水样中溶解性磷浓度及回收率与pH的关系-|||-图2水样中溶解性磷浓度及回收率与反应时间的关系(2)写出氯化水解法生产三氯氧磷的化学方程式为PCl3+H2O+Cl2=POCl3+2HCl.氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水.在废水中先加入适量漂1白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收.(3)POCl3、H3PO4、H3PO3中磷元素的化合价分别为+5、+5、+3.(4)在沉淀前先加入适量漂白粉的作用是将+3价的磷氧化为+5价的磷(将H3PO3氧化为H3PO4).Ⅲ.如图乙是不同条件对磷的沉淀回收率的影响图象.(5)处理该厂废水最合适的工艺条件为bc(选填字母).a.调节pH=9 b.调节pH=10 c.反应时间30min d.反应时间120min(6)己知磷酸是三元酸,其各级电离常数如下:K1=7.1×10-3 K2=6.3×l0-8 K3=4.2×10-13,则0.1mol/L的NaH2PO4溶液的pH<7(填>,=,<).
Ⅰ.白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在电炉中高温(约1550℃)下通过下面两个反应共熔得到.
①2Ca3(PO4)2(s)+5C(s)=6CaO(s)+P4(s)+5CO2(g)△H1=+Ql kJ•mol-1
②CaO(s)+SiO2(s)=CaSiO3(s)△H2=-Q2 kJ•mol-1
(1)写出电炉中发生总反应的热化学方程式2Ca3(PO4)2(s)+6SiO2(s)+5C(s)6CaSiO3(s)+P4(s)+5CO2(g))△H=(Ql-6Q2 )kJ•mol-1
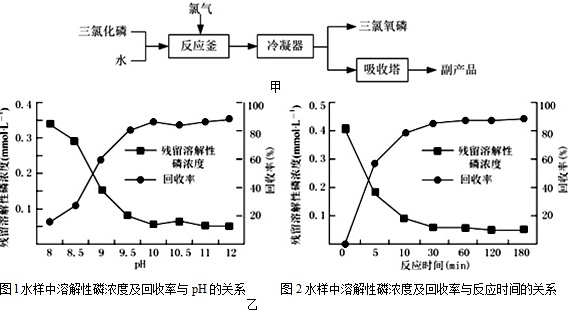
Ⅱ.三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料.氯化水解法生产三氯氧磷的流程如图甲:
(2)写出氯化水解法生产三氯氧磷的化学方程式为PCl3+H2O+Cl2=POCl3+2HCl.
氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水.在废水中先加入适量漂1白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收.
(3)POCl3、H3PO4、H3PO3中磷元素的化合价分别为+5、+5、+3.
(4)在沉淀前先加入适量漂白粉的作用是将+3价的磷氧化为+5价的磷(将H3PO3氧化为H3PO4).
Ⅲ.如图乙是不同条件对磷的沉淀回收率的影响图象.
(5)处理该厂废水最合适的工艺条件为bc(选填字母).
a.调节pH=9 b.调节pH=10 c.反应时间30min d.反应时间120min
(6)己知磷酸是三元酸,其各级电离常数如下:K1=7.1×10-3 K2=6.3×l0-8 K3=4.2×10-13,则0.1mol/L的NaH2PO4溶液的pH<7(填>,=,<).
题目解答
答案
分析 Ⅰ.(1)依据热化学方程式和盖斯定律计算所需化学方程式,反应的焓变与化学计量数成正比;
Ⅱ.(2)氯化水解法产物是三氯氧磷和盐酸,结合原子守恒分析;
(3)根据化合价规则计算元素的化合价,在化合物中正负化合价代数和为零;
(4)在沉淀前先加入适量漂白粉使废水中的H3PO3氧化为PO43-,加入生石灰后能完全转化为磷酸的钙盐,达到较高的回收率;
Ⅲ.(5)根据图1、2分析磷的沉淀回收率;
(6)NaH2PO4溶液中存在水解平衡:H2PO4-+H2O?H3PO4+OH-,电离平衡:H2PO4-?HPO42-+H+,电离常数K1>K2>K3,H2PO4-在水溶液里电离程度大于水解程度.
解答 解:Ⅰ.(1)①2Ca3(PO4)2(s)+5C(s)=6CaO(s)+P4(s)+5CO2(g)△H1=+Ql kJ•mol-1
②CaO(s)+SiO2(s)=CaSiO3(s)△H2=-Q2 kJ•mol-1
依据热化学方程式和盖斯定律计算得到①-②×6得到化学方程式为:2Ca3(PO4)2(s)+6SiO2(s)+5C(s)6CaSiO3(s)+P4(s)+5CO2(g))△H=(Ql-6Q2 )kJ•mol-1,
故答案为:2Ca3(PO4)2(s)+6SiO2(s)+5C(s)6CaSiO3(s)+P4(s)+5CO2(g))△H=(Ql-6Q2 )kJ•mol-1;
Ⅱ.(2)氯化水解法是用三氯化磷、氯气与水反应生成三氯氧磷和盐酸,其化学方程式为:PCl3+H2O+Cl2=POCl3+2HCl,
故答案为:PCl3+H2O+Cl2=POCl3+2HCl;
(3)氯元素显-1价,氢元素显+1价,氧元素显-2价,设磷元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:POCl3、H3PO4、H3PO3中磷元素的化合价分别为+5、+5、+3,
故答案为:+5、+5、+3;
(4)氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水,在废水中先加入适量漂白粉,使废水中的H3PO3氧化为PO43-,使其加入生石灰后能完全转化为磷酸的钙盐,达到较高的回收率;
故答案为:将+3价的磷氧化为+5价的磷(将H3PO3氧化为H3PO4);
Ⅲ.(5)根据图1、2可确定pH=10、反应时间30 min时磷的沉淀回收率较高,则处理该厂废水最合适的工艺条件为pH=10、反应时间30 min,
故答案为:bc;
(6)NaH2PO4溶液中存在水解平衡:H2PO4-+H2O?H3PO4+OH-,电离平衡:H2PO4-?HPO42-+H+;磷酸是三元酸,其各级电离常数如下:K1=7.1×10-3 K2=6.3×l0-8 K3=4.2×10-13,K1>K2>K3,H2PO4-在水溶液里电离程度大于水解程度,0.1mol/L的NaH2PO4溶液中按三级电离全部电离2CK3<K2,所以NaH2PO4溶液中按二级电离粗略计算,0.1mol/L>6.3×l0-8 ,所以溶液的pH=-lgc(H+)≈1,实际略小于1,显酸性,即PH<7,
故答案为:<.
点评 本题考查了物质的制备方案设计,题目涉及热化学方程式的书写、氧化还原的应用、化合价的计算、PH的应用等,题目综合性较强,难度中等,侧重于考查学生的分析能力和对基础知识的综合应用能力.