题目
我国化学家侯德榜发明的侯氏制碱法,开创了世界制碱工业的新纪元。制碱工艺中的关键反应为:NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl。室温(20℃)下,某兴趣小组在实验室利用如图装置模拟该反应。盐酸 A 浓氨水-|||-a-|||-碳酸钙 饱和碳酸 饱和食盐水 .氢氧化钠-|||-氢钠溶液-|||-A B C D已知:①20℃时,几种盐的溶解度如表。 物质 NaCl NaHCO3 NH4Cl 溶解度/g 36.0 9.6 37.2 ②氨气极易溶于饱和食盐水,形成的溶液呈碱性。(1)为配制饱和食盐水,应向100g水中至少加入 ____ gNaCl固体。(2)仪器a的名称是 ____ ,装置D的作用是 ____ 。(3)装置A制取的CO2中会混有HCl,用饱和NaHCO3溶液吸收HCl的化学方程式为 ____ 。(4)为使CO2在装置C中能充分吸收,可采取的措施是 ____ 。充分反应后,装置C中有晶体析出。为分析晶体产生的原因,兴趣小组继续开展探究。查阅资料:一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。(5)装置C中析出的晶体主要成分是NaHCO3而不是NH4Cl原因是 ____ 。(6)装置C中的物质过滤后得到的滤液在工业上称为母液。侯氏制碱法通过向母液中加入食盐,使NH4Cl结晶析出,析出晶体的原因是 ____ 。
我国化学家侯德榜发明的侯氏制碱法,开创了世界制碱工业的新纪元。制碱工艺中的关键反应为:NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl。室温(20℃)下,某兴趣小组在实验室利用如图装置模拟该反应。
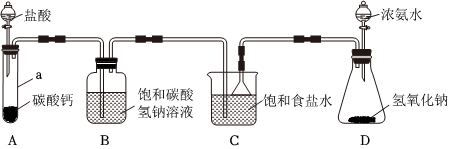
已知:
①20℃时,几种盐的溶解度如表。
②氨气极易溶于饱和食盐水,形成的溶液呈碱性。
(1)为配制饱和食盐水,应向100g水中至少加入 ____ gNaCl固体。
(2)仪器a的名称是 ____ ,装置D的作用是 ____ 。
(3)装置A制取的CO2中会混有HCl,用饱和NaHCO3溶液吸收HCl的化学方程式为 ____ 。
(4)为使CO2在装置C中能充分吸收,可采取的措施是 ____ 。
充分反应后,装置C中有晶体析出。为分析晶体产生的原因,兴趣小组继续开展探究。
查阅资料:一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。
(5)装置C中析出的晶体主要成分是NaHCO3而不是NH4Cl原因是 ____ 。
(6)装置C中的物质过滤后得到的滤液在工业上称为母液。侯氏制碱法通过向母液中加入食盐,使NH4Cl结晶析出,析出晶体的原因是 ____ 。

已知:
①20℃时,几种盐的溶解度如表。
| 物质 | NaCl | NaHCO3 | NH4Cl |
| 溶解度/g | 36.0 | 9.6 | 37.2 |
(1)为配制饱和食盐水,应向100g水中至少加入 ____ gNaCl固体。
(2)仪器a的名称是 ____ ,装置D的作用是 ____ 。
(3)装置A制取的CO2中会混有HCl,用饱和NaHCO3溶液吸收HCl的化学方程式为 ____ 。
(4)为使CO2在装置C中能充分吸收,可采取的措施是 ____ 。
充分反应后,装置C中有晶体析出。为分析晶体产生的原因,兴趣小组继续开展探究。
查阅资料:一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。
(5)装置C中析出的晶体主要成分是NaHCO3而不是NH4Cl原因是 ____ 。
(6)装置C中的物质过滤后得到的滤液在工业上称为母液。侯氏制碱法通过向母液中加入食盐,使NH4Cl结晶析出,析出晶体的原因是 ____ 。
题目解答
答案
解:(1)根据20℃时,几种盐的溶解度表可知,20℃时NaCl的溶解度是36.0g,即20℃时100g水中溶解36.0gNaCl固体达到饱和状态,所以为配制饱和食盐水,应向100g水中至少加入36.0gNaCl固体。
(2)据图可知,仪器a是试管;由于氨气极易溶于饱和食盐水,为防止倒吸,用装置D产生氨气。
(3)饱和NaHCO3溶液与HCl反应生成氯化钠、水和二氧化碳,化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑。
(4)由于氨气极易溶于饱和食盐水,形成的溶液呈碱性,碱性溶液能充分吸收二氧化碳。所以为使CO2在装置C中能充分吸收,可采取的措施是先打开装置D分液漏斗活塞,再打开装置A分液漏斗活塞。
(5)由于相同条件下,生成NaHCO3溶解度比NHaCl的小,以晶体形式析出,所以装置C中析出的晶体主要成分是NaHCO3而不是NH4Cl。
(6)一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。所以增大Cl-浓度,生成氯化铵更多,所以氯化铵结晶析出。
故答案为:(1)36.0。
(2)试管;产生氨气,防止倒吸。
(3)NaHCO3+HCl=NaCl+H2O+CO2↑。
(4)先打开装置D分液漏斗活塞,再打开装置A分液漏斗活塞。
(5)相同条件下,生成NaHCO3溶解度比NH4Cl的小,以晶体形式析出。
(6)增大Cl-浓度,生成氯化铵更多,所以氯化铵结晶析出。
(2)据图可知,仪器a是试管;由于氨气极易溶于饱和食盐水,为防止倒吸,用装置D产生氨气。
(3)饱和NaHCO3溶液与HCl反应生成氯化钠、水和二氧化碳,化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑。
(4)由于氨气极易溶于饱和食盐水,形成的溶液呈碱性,碱性溶液能充分吸收二氧化碳。所以为使CO2在装置C中能充分吸收,可采取的措施是先打开装置D分液漏斗活塞,再打开装置A分液漏斗活塞。
(5)由于相同条件下,生成NaHCO3溶解度比NHaCl的小,以晶体形式析出,所以装置C中析出的晶体主要成分是NaHCO3而不是NH4Cl。
(6)一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。所以增大Cl-浓度,生成氯化铵更多,所以氯化铵结晶析出。
故答案为:(1)36.0。
(2)试管;产生氨气,防止倒吸。
(3)NaHCO3+HCl=NaCl+H2O+CO2↑。
(4)先打开装置D分液漏斗活塞,再打开装置A分液漏斗活塞。
(5)相同条件下,生成NaHCO3溶解度比NH4Cl的小,以晶体形式析出。
(6)增大Cl-浓度,生成氯化铵更多,所以氯化铵结晶析出。
解析
步骤 1:配制饱和食盐水
根据20℃时NaCl的溶解度是36.0g,即100g水中溶解36.0gNaCl固体达到饱和状态,所以为配制饱和食盐水,应向100g水中至少加入36.0gNaCl固体。
步骤 2:仪器a的名称和装置D的作用
仪器a是试管;由于氨气极易溶于饱和食盐水,为防止倒吸,用装置D产生氨气。
步骤 3:用饱和NaHCO_3溶液吸收HCl的化学方程式
饱和NaHCO_3溶液与HCl反应生成氯化钠、水和二氧化碳,化学方程式为NaHCO_3+HCl=NaCl+H_2O+CO_2↑。
步骤 4:使CO_2在装置C中能充分吸收的措施
由于氨气极易溶于饱和食盐水,形成的溶液呈碱性,碱性溶液能充分吸收二氧化碳。所以为使CO_2在装置C中能充分吸收,可采取的措施是先打开装置D分液漏斗活塞,再打开装置A分液漏斗活塞。
步骤 5:装置C中析出的晶体主要成分是NaHCO_3而不是NH_4Cl的原因
由于相同条件下,生成NaHCO_3溶解度比NH_4Cl的小,以晶体形式析出,所以装置C中析出的晶体主要成分是NaHCO_3而不是NH_4Cl。
步骤 6:向母液中加入食盐,使NH_4Cl结晶析出的原因
一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。所以增大Cl^{-}浓度,生成氯化铵更多,所以氯化铵结晶析出。
根据20℃时NaCl的溶解度是36.0g,即100g水中溶解36.0gNaCl固体达到饱和状态,所以为配制饱和食盐水,应向100g水中至少加入36.0gNaCl固体。
步骤 2:仪器a的名称和装置D的作用
仪器a是试管;由于氨气极易溶于饱和食盐水,为防止倒吸,用装置D产生氨气。
步骤 3:用饱和NaHCO_3溶液吸收HCl的化学方程式
饱和NaHCO_3溶液与HCl反应生成氯化钠、水和二氧化碳,化学方程式为NaHCO_3+HCl=NaCl+H_2O+CO_2↑。
步骤 4:使CO_2在装置C中能充分吸收的措施
由于氨气极易溶于饱和食盐水,形成的溶液呈碱性,碱性溶液能充分吸收二氧化碳。所以为使CO_2在装置C中能充分吸收,可采取的措施是先打开装置D分液漏斗活塞,再打开装置A分液漏斗活塞。
步骤 5:装置C中析出的晶体主要成分是NaHCO_3而不是NH_4Cl的原因
由于相同条件下,生成NaHCO_3溶解度比NH_4Cl的小,以晶体形式析出,所以装置C中析出的晶体主要成分是NaHCO_3而不是NH_4Cl。
步骤 6:向母液中加入食盐,使NH_4Cl结晶析出的原因
一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。所以增大Cl^{-}浓度,生成氯化铵更多,所以氯化铵结晶析出。