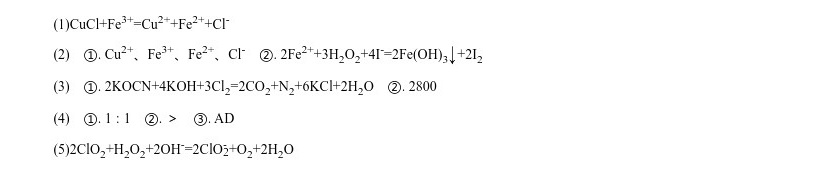题目
2 . 从化合价的角度分析氯及其化合物的性质,并按要求回答下列问题。(1)氯化亚铜(CuCl)是重要的化工原料,工业上常通过下列反应制备CuCl: 2CuSO4+Na2SO3+2NaCl+Na2CO3=2CuCl↓+3Na2SO4+CO2↑查阅资料可得,CuCl可以溶解在FeCl3溶液中,请写出该反应的离子方程式___________。(2)已知:Cu2O在酸性溶液中发生歧化反应:Cu2O+2H+=Cu2++Cu+H2O。现将一定量混合物(Fe2O3、Cu2O、CuCl、Fe)溶解于过量稀盐酸中,反应完全后,得到W(包括溶液和少量剩余固体)。①继续往W中通入足量的氯气,不断搅拌,充分反应,溶液中哪些离子的物质的量一定有明显变化?___________(用离子符号表示)。②不通入气体,改往W中加入过量铁粉,过滤,调pH约为7,加入淀粉-KI溶液和H2O2溶液,溶液呈蓝色并有红褐色沉淀生成。当消耗2 mol I-时,共转移3 mol电子,该反应的离子方程式是___________(3)某工厂废水中含KCN,其浓度为650 mg·L-1,现用氯氧化法处理,发生如下反应(化合物中N化合价均为-3) :KCN+2KOH+Cl2=KOCN+2KCl+H2O。①通入过量氯气,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:________KOCN+_____KOH+___ Cl2=_____ CO2+____ N2+____KCl+____H2O。②若将5 m3含KCN的浓度为650 mg·L-1的废水中KCN氧化成N2除去,需要标准状况下的氯气的体积为___________L。(4)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理:2NaClO3+4HCl=2ClO2 ↑+Cl2↑+2H2O+2NaCl。①该反应中,氧化剂和还原剂的物质的量之比为___________,依据氧化还原反应规律判断,氧化性强弱为NaClO3___________ (填“>"<"或“=")Cl2.。②ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO),需将其转化为Cl-除去,下列试剂中,可将ClO转化为Cl-的是___________ (填字母)。A.FeSO4 B.O3 C.KMnO4 D.SO2(5)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如下:请将流程中反应②的离子方程式补充完整:__________ClO2+_____H2O2+_____=_____ ClO+ ____O2+_____。
2 . 从化合价的角度分析氯及其化合物的性质,并按要求回答下列问题。
(1)氯化亚铜(CuCl)是重要的化工原料,工业上常通过下列反应制备CuCl: 2CuSO4+Na2SO3+2NaCl+Na2CO3=2CuCl↓+3Na2SO4+CO2↑
查阅资料可得,CuCl可以溶解在FeCl3溶液中,请写出该反应的离子方程式___________ 。
(2)已知:Cu2O在酸性溶液中发生歧化反应:Cu2O+2H+=Cu2++Cu+H2O。
现将一定量混合物(Fe2O3、Cu2O、CuCl、Fe)溶解于过量稀盐酸中,反应完全后,得到W(包括溶液和少量剩余固体)。
①继续往W中通入足量的氯气,不断搅拌,充分反应,溶液中哪些离子的物质的量一定有明显变化?___________ (用离子符号表示)。
②不通入气体,改往W中加入过量铁粉,过滤,调pH约为7,加入淀粉-KI溶液和H2O2溶液,溶液呈蓝色并有红褐色沉淀生成。当消耗2 mol I-时,共转移3 mol电子,该反应的离子方程式是___________
(3)某工厂废水中含KCN,其浓度为650 mg·L-1,现用氯氧化法处理,发生如下反应(化合物中N化合价均为-3) :KCN+2KOH+Cl2=KOCN+2KCl+H2O。
①通入过量氯气,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:____
____KOCN+_____KOH+___ Cl2=_____ CO2+____ N2+____KCl+____H2O。
②若将5 m3含KCN的浓度为650 mg·L-1的废水中KCN氧化成N2除去,需要标准状况下的氯气的体积为___________ L。
(4)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理:2NaClO3+4HCl=2ClO2 ↑+Cl2↑+2H2O+2NaCl。
①该反应中,氧化剂和还原剂的物质的量之比为___________ ,依据氧化还原反应规律判断,氧化性强弱为NaClO3___________ (填“>"<"或“=")Cl2.。
②ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中,可将ClO
),需将其转化为Cl-除去,下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是___________ (填字母)。
A.FeSO4 B.O3 C.KMnO4 D.SO2
(5)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如下:
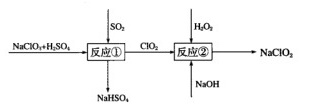
请将流程中反应②的离子方程式补充完整:_____
_____ClO2+_____H2O2+_____=_____ ClO + ____O2+_____。
+ ____O2+_____。
(1)氯化亚铜(CuCl)是重要的化工原料,工业上常通过下列反应制备CuCl: 2CuSO4+Na2SO3+2NaCl+Na2CO3=2CuCl↓+3Na2SO4+CO2↑
查阅资料可得,CuCl可以溶解在FeCl3溶液中,请写出该反应的离子方程式
(2)已知:Cu2O在酸性溶液中发生歧化反应:Cu2O+2H+=Cu2++Cu+H2O。
现将一定量混合物(Fe2O3、Cu2O、CuCl、Fe)溶解于过量稀盐酸中,反应完全后,得到W(包括溶液和少量剩余固体)。
①继续往W中通入足量的氯气,不断搅拌,充分反应,溶液中哪些离子的物质的量一定有明显变化?
②不通入气体,改往W中加入过量铁粉,过滤,调pH约为7,加入淀粉-KI溶液和H2O2溶液,溶液呈蓝色并有红褐色沉淀生成。当消耗2 mol I-时,共转移3 mol电子,该反应的离子方程式是
(3)某工厂废水中含KCN,其浓度为650 mg·L-1,现用氯氧化法处理,发生如下反应(化合物中N化合价均为-3) :KCN+2KOH+Cl2=KOCN+2KCl+H2O。
①通入过量氯气,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
____KOCN+_____KOH+___ Cl2=_____ CO2+____ N2+____KCl+____H2O。
②若将5 m3含KCN的浓度为650 mg·L-1的废水中KCN氧化成N2除去,需要标准状况下的氯气的体积为
(4)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理:2NaClO3+4HCl=2ClO2 ↑+Cl2↑+2H2O+2NaCl。
①该反应中,氧化剂和还原剂的物质的量之比为
②ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去,下列试剂中,可将ClO
),需将其转化为Cl-除去,下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是A.FeSO4 B.O3 C.KMnO4 D.SO2
(5)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如下:

请将流程中反应②的离子方程式补充完整:
_____ClO2+_____H2O2+_____=_____ ClO
 + ____O2+_____。
+ ____O2+_____。题目解答
答案