碳是地球上组成生命的最基本元素之一,可以sp^3、sp^3和sp^3杂化轨道成共价键,具有很强的结合能力,与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。请回答下列问题:基态碳原子核外有____种空间运动状态的电子,其价电子排布图为_____________。光气的分子式为sp^3,又称碳酰氯,是一种重要的含碳化合物,判断其分子立体构型为________,其碳原子杂化轨道类型为________杂化。碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:碳酸盐sp^3sp^3sp^3热分解温度sp^340290011721360阳离子半径sp^36699112135试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?_____________________。碳的一种同素异形体sp^3,又名足球烯,是一种高度对称的球碳分子。立方烷分子式:sp^3,结构如立方体:sp^3是比sp^3约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与sp^3的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原sp^3晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为___________。sp^3碳的另一种同素异形体sp^3石墨,其晶体结构如上图所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为________个。已知石墨的密度为sp^3,sp^3键长为sp^3,阿伏伽德罗常数的值为sp^3,计算石墨晶体的层间距为________sp^3。sp^3碳的第三种同素异形体sp^3金刚石,其晶胞如上图所示。已知金属钠的晶胞体心立方堆积沿其体对角线垂直在纸平面上的投影图如下图A所示,则金刚石晶胞沿其体对角线垂直在纸平面上的投影图应该是下图_______从sp^3图中选填。sp^3化学sp^3选修3:物质结构与性质2018年7月5日sp^3科学sp^3杂志在线报道:美国研究人员合成一种新的具有超高热导率半导体材料砷化硼sp^3。回答下列问题:基态As原子价层电子的电子排布图轨道表达式为________,基态B原子核外电子占据最高能级的电子云轮廓图为________。通过反应sp^3,晶体sp^3可制备BAs晶体,sp^3结构如图所示。sp^3sp^3分子空间构型为________,其中B原子杂化方式是________。sp^3分子中键角为________度,分子中成键电子对与孤电子对数目之比为________。晶态单质硼有多种结构,它们都以sp^3结构如图sp^3所示为基本的结构单元。sp^3结构单元为________面体。单质硼的熔点为sp^3,它属于________晶体。sp^3晶胞结构如图sp^3所示,已知晶胞参数为sp^3,阿伏加德罗常数的值为sp^3。As原子的配位数为________;BAs晶体的密度为________sp^3列出计算式。化学sp^3物质结构与性质氮、铬及其相关化合物用途非常广泛:回答下列问题:基态N原子的核外电子排布式为_________,Cr位于元素周期表第四周期________族。sp^3与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为_________;sp^3的熔点sp^3比sp^3的熔点sp^3低得多,这是因为_______________________________。sp^3的一种配合物结构如图所示:sp^3阴离子sp^3的空间构型为_______形。配离子中,中心离子的配位数为_______,N与中心原子形成的化学键称为________键。配体sp^3乙二胺中碳原子的杂化方式是________,分子中三种元素电负性从大到小的顺序为____________。氮化铬的熔点为sp^3,它的一种晶体的晶胞结构如图所示,其密度为sp^3,氮化铬的晶胞边长为____________列出计算式sp^3。sp^3铁、钴、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:铁、钴、镍的基态原子核外未成对电子数最多的是________。酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是_______填1、2、3、sp^3,三种非金属原子的电负性由大到小的顺序为_____________用相应的元素符号表示;氮原子的杂化轨道类型为_________________。sp^3sp^3,常温下呈液态,熔点为sp^3,沸点为sp^3,易溶于非极性溶剂,据此可判断,晶体属于__________填晶体类型,若配合物的中心原子价电子数与配体提供电子数之和为18,则sp^3_______。sp^3、FeO的晶体结构类型与氯化钠的相同,sp^3和的离子半径分别为69pm和78pm,则熔点NiO____sp^3填“”“”或“”,原因是____________。sp^3的晶胞结构如图所示:sp^3镍离子的配位数为__________。若阿伏加德罗常数的值为sp^3,晶体密度为sp^3,则该晶胞中最近的sp^3之间的距离为______cm。写出计算表达式【化学sp^3选修3:物质结构与性质】第ⅢA族元素及其化合物广泛应用于材料科学。请回答下列问题:sp^3基态B原子的核外电子排布图为________。sp^3是新型无机非金属材料。同周期元素中第一电离能处于B和N之间不包括B和sp^3有________种元素,其中电负性最大的元素的基态原子核外电子占据________个能级。sp^3、sp^3是有机合成中常用的还原剂。sp^3可由硼酸制得,硼酸的结构如图1所示。硼酸中,1个B原子与相邻3个O原子构成的形状是________填空间构型名称。硼酸晶体中不存在的作用力类型有________填字母。范德华力sp^3氢键c.sp^3键d.键sp^3是一元弱酸,在水中电离方程式为sp^3,sp^3中B原子的杂化方式为________。根据对角线规则,B和________填元素符号的性质相似。某镁铝合金的晶胞为立方结构,其结构如图2所示,该晶体中Al原子的配位数为________。sp^3、GaN的结构均与金刚石相似,GaAs的熔点低于GaN的主要原因为________。sp^3砷化镓晶胞结构如图3所示。已知:砷化镓晶体密度为dsp^3,阿伏加德罗常数的值为sp^3。连接面心上6个砷原子构成正八面体,该正八面体的边长为________sp^3用含d和sp^3的代数式表示。sp^3和As之间的最近距离为________sp^3用含d和sp^3的代数式表示。【化学sp^3选修3:物质结构与性质】教材插图是对教材内容高度概括的体现,也是为说明、理解、深化文字内容服务的。请回答下列问题:图一为构造原理示意图,其含义是从H原子开始随着原子核电荷数递增,原子核每增加一个质子,核外便增加一个电子,电子大多按如图顺序填充。第四周期中,基态4s能级半充满的元素有________种,其中原子序数最大的基态原子的外围电子排布式为________。sp^3图一图二中,每条折线代表周期表中sp^3某一族元素简单氢化物的沸点变化,其他三条折线与x所在折线变化趋势不完全相同的原因为________;与x点对应的简单氢化物互为等电子体的离子为________写一种。sp^3图二图三为卟啉配合物叶绿素的结构示意图,1号N原子和3号N原子与sp^3形成的化学键类型为________;5号C原子和6号C原子的杂化方式分别为________、________;该分子中所含非金属元素的电负性由小到大的顺序为________。sp^3图三从石墨晶体结构示意图中截取石墨的晶胞如图四所示,设阿伏加德罗常数为sp^3,已知sp^3,石墨晶体的密度为________sp^3列出计算式。sp^3图四化学sp^3选修3:物质结构与性质sp^3、sp^3和sp^3均可用作电极材料。请回答下列问题:基态sp^3的价层电子轨道表达式为________________;同周期元素中,基态原子的未成对电子数与基态sp^3相同的元素为________。sp^3的空间构型为________________,其中P原子的杂化方式为________;写出一种与互为等电子体且中心原子与P不同主族的阴离子:________填离子符号。sp^3为紫色晶体,其中1mol阳离子中所含sp^3键的数目为________;配位键中提供孤电子对的原子为________填元素符号。已知物质间的转化关系如图甲所示,其中a、c均大于0。sp^3基态Na原子的第一电离能可表示为________。相同条件下,sp^3的晶格能________填“”“”或“”sp^3,原因为________________________________________________________________________。sp^3的立方晶胞结构如图乙所示。若紧邻的两个之间的距离为dpm,阿伏加德罗常数的值为sp^3,晶体的密度为sp^3,则Na的摩尔质量可表示为________________sp^3用含有d、、sp^3的代数式表示。据报道,某科研团队成功合成了钛掺杂、镧镍锂氧化物包覆的“双重修饰”富镍三元正极材料。请回答下列问题:基态钛原子的外围电子排布图为____________。sp^3是一种还原剂,可将羧酸直接还原为醇:sp^3sp^3sp^3。sp^3中存在的作用力类型有_____填字母。离子键sp^3配位键sp^3氢键sp^3非极性键乙醚sp^3、乙醇的沸点分别为sp^3、sp^3,导致二者沸点差异的主要原因是___________________________。sp^3分子中C原子的杂化方式为_______;所含sp^3键和键的数目之比为_____;键角____填“”“”或“”sp^3。sp^3sp^3的晶胞结构如图甲所示,其中白球代表__填“Ti”或“O”,黑球的配位数为____。sp^3氧化镍的立方晶胞结构如图乙所示。已知氧化镍晶体的密度为sp^3,sp^3为阿伏加德罗常数的值。sp^3坐标参数表示原子在晶体中的相对位置。已知A、B的坐标参数分别为0,、1,,则C的坐标参数为_________。晶胞面心上的6个氧离子构成正八面体形,镍离子位于体心,该正八面体的边长为_____sp^3用含有d、sp^3的代数式表示。第四周期某些过渡元素在工业生产中有着极其重要的作用sp^3铬是最硬的金属单质,被称为“不锈钢的添加剂”sp^3写出Cr在周期表中的位置________;其原子核外电子排布的最高能层符号________sp^3在sp^3其中Cr为价中,含有过氧键的数目为________
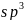 、
、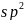 和
和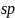 杂化轨道成共价键,具有很强的结合能力,与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。请回答下列问题:基态碳原子核外有____种空间运动状态的电子,其价电子排布图为_____________。光气的分子式为
杂化轨道成共价键,具有很强的结合能力,与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。请回答下列问题:基态碳原子核外有____种空间运动状态的电子,其价电子排布图为_____________。光气的分子式为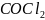 ,又称碳酰氯,是一种重要的含碳化合物,判断其分子立体构型为________,其碳原子杂化轨道类型为________杂化。
,又称碳酰氯,是一种重要的含碳化合物,判断其分子立体构型为________,其碳原子杂化轨道类型为________杂化。碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
碳酸盐
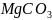
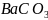
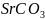
热分解温度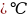
402
900
1172
1360
阳离子半径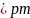
66
99
112
135
试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?_____________________。碳的一种同素异形体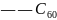 ,又名足球烯,是一种高度对称的球碳分子。立方烷分子式:
,又名足球烯,是一种高度对称的球碳分子。立方烷分子式: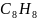 ,结构如立方体:
,结构如立方体: 是比
是比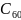 约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与
约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与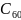 的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原
的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原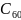 晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为___________。
晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为___________。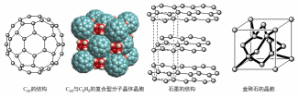 碳的另一种同素异形体
碳的另一种同素异形体 石墨,其晶体结构如上图所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为________个。已知石墨的密度为
石墨,其晶体结构如上图所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为________个。已知石墨的密度为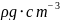 ,
,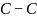 键长为
键长为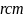 ,阿伏伽德罗常数的值为
,阿伏伽德罗常数的值为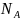 ,计算石墨晶体的层间距为________
,计算石墨晶体的层间距为________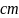 。
。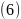 碳的第三种同素异形体
碳的第三种同素异形体 金刚石,其晶胞如上图所示。已知金属钠的晶胞体心立方堆积沿其体对角线垂直在纸平面上的投影图如下图A所示,则金刚石晶胞沿其体对角线垂直在纸平面上的投影图应该是下图_______从
金刚石,其晶胞如上图所示。已知金属钠的晶胞体心立方堆积沿其体对角线垂直在纸平面上的投影图如下图A所示,则金刚石晶胞沿其体对角线垂直在纸平面上的投影图应该是下图_______从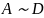 图中选填。
图中选填。
化学 选修3:物质结构与性质
选修3:物质结构与性质
2018年7月5日 科学
科学 杂志在线报道:美国研究人员合成一种新的具有超高热导率半导体材料砷化硼
杂志在线报道:美国研究人员合成一种新的具有超高热导率半导体材料砷化硼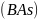 。回答下列问题:
。回答下列问题:
基态As原子价层电子的电子排布图轨道表达式为________,基态B原子核外电子占据最高能级的电子云轮廓图为________。
通过反应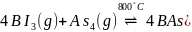 ,晶体
,晶体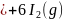 可制备BAs晶体,
可制备BAs晶体,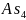 结构如图所示。
结构如图所示。
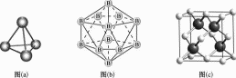
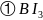 分子空间构型为________,其中B原子杂化方式是________。
分子空间构型为________,其中B原子杂化方式是________。
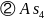 分子中键角为________度,分子中成键电子对与孤电子对数目之比为________。
分子中键角为________度,分子中成键电子对与孤电子对数目之比为________。
晶态单质硼有多种结构,它们都以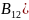 结构如图
结构如图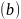 所示为基本的结构单元。
所示为基本的结构单元。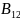 结构单元为________面体。单质硼的熔点为
结构单元为________面体。单质硼的熔点为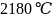 ,它属于________晶体。
,它属于________晶体。
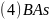 晶胞结构如图
晶胞结构如图 所示,已知晶胞参数为
所示,已知晶胞参数为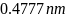 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为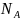 。As原子的配位数为________;BAs晶体的密度为________
。As原子的配位数为________;BAs晶体的密度为________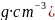 列出计算式。
列出计算式。
化学 物质结构与性质
物质结构与性质
氮、铬及其相关化合物用途非常广泛:回答下列问题:
基态N原子的核外电子排布式为_________,Cr位于元素周期表第四周期________族。
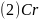 与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为_________;
与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为_________;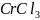 的熔点
的熔点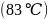 比
比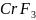 的熔点
的熔点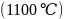 低得多,这是因为_______________________________。
低得多,这是因为_______________________________。
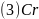 的一种配合物结构如图所示:
的一种配合物结构如图所示: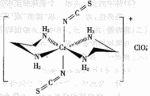
阴离子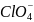 的空间构型为_______形。
的空间构型为_______形。
配离子中,中心离子的配位数为_______,N与中心原子形成的化学键称为________键。
配体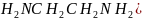 乙二胺中碳原子的杂化方式是________,分子中三种元素电负性从大到小的顺序为____________。
乙二胺中碳原子的杂化方式是________,分子中三种元素电负性从大到小的顺序为____________。
氮化铬的熔点为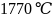 ,它的一种晶体的晶胞结构如图所示,其密度为
,它的一种晶体的晶胞结构如图所示,其密度为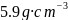 ,氮化铬的晶胞边长为____________列出计算式
,氮化铬的晶胞边长为____________列出计算式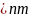 。
。

铁、钴、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
铁、钴、镍的基态原子核外未成对电子数最多的是________。
酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是_______填1、2、3、 ,三种非金属原子的电负性由大到小的顺序为_____________用相应的元素符号表示;氮原子的杂化轨道类型为_________________。
,三种非金属原子的电负性由大到小的顺序为_____________用相应的元素符号表示;氮原子的杂化轨道类型为_________________。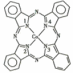
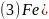 ,常温下呈液态,熔点为
,常温下呈液态,熔点为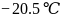 ,沸点为
,沸点为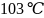 ,易溶于非极性溶剂,据此可判断,晶体属于__________填晶体类型,若配合物的中心原子价电子数与配体提供电子数之和为18,则
,易溶于非极性溶剂,据此可判断,晶体属于__________填晶体类型,若配合物的中心原子价电子数与配体提供电子数之和为18,则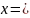 _______。
_______。
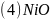 、FeO的晶体结构类型与氯化钠的相同,
、FeO的晶体结构类型与氯化钠的相同,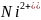 和的离子半径分别为69pm和78pm,则熔点NiO____
和的离子半径分别为69pm和78pm,则熔点NiO____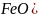 填“”“”或“”,原因是____________。
填“”“”或“”,原因是____________。
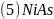 的晶胞结构如图所示:
的晶胞结构如图所示: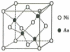
镍离子的配位数为__________。
若阿伏加德罗常数的值为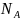 ,晶体密度为
,晶体密度为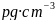 ,则该晶胞中最近的
,则该晶胞中最近的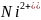 之间的距离为______cm。写出计算表达式
之间的距离为______cm。写出计算表达式
【化学 选修3:物质结构与性质】第ⅢA族元素及其化合物广泛应用于材料科学。请回答下列问题:
选修3:物质结构与性质】第ⅢA族元素及其化合物广泛应用于材料科学。请回答下列问题: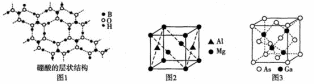
基态B原子的核外电子排布图为________。
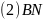 是新型无机非金属材料。同周期元素中第一电离能处于B和N之间不包括B和
是新型无机非金属材料。同周期元素中第一电离能处于B和N之间不包括B和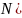 有________种元素,其中电负性最大的元素的基态原子核外电子占据________个能级。
有________种元素,其中电负性最大的元素的基态原子核外电子占据________个能级。
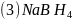 、
、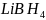 是有机合成中常用的还原剂。
是有机合成中常用的还原剂。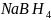 可由硼酸制得,硼酸的结构如图1所示。
可由硼酸制得,硼酸的结构如图1所示。
硼酸中,1个B原子与相邻3个O原子构成的形状是________填空间构型名称。
硼酸晶体中不存在的作用力类型有________填字母。
范德华力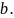 氢键c.
氢键c.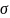 键d.键
键d.键
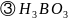 是一元弱酸,在水中电离方程式为
是一元弱酸,在水中电离方程式为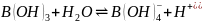 ,
,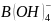 中B原子的杂化方式为________。
中B原子的杂化方式为________。
根据对角线规则,B和________填元素符号的性质相似。
某镁铝合金的晶胞为立方结构,其结构如图2所示,该晶体中Al原子的配位数为________。
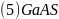 、GaN的结构均与金刚石相似,GaAs的熔点低于GaN的主要原因为________。
、GaN的结构均与金刚石相似,GaAs的熔点低于GaN的主要原因为________。
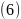 砷化镓晶胞结构如图3所示。已知:砷化镓晶体密度为d
砷化镓晶胞结构如图3所示。已知:砷化镓晶体密度为d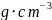 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为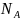 。
。
连接面心上6个砷原子构成正八面体,该正八面体的边长为________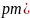 用含d和
用含d和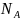 的代数式表示。
的代数式表示。
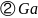 和As之间的最近距离为________
和As之间的最近距离为________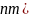 用含d和
用含d和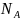 的代数式表示。
的代数式表示。
【化学 选修3:物质结构与性质】
选修3:物质结构与性质】
教材插图是对教材内容高度概括的体现,也是为说明、理解、深化文字内容服务的。请回答下列问题:
图一为构造原理示意图,其含义是从H原子开始随着原子核电荷数递增,原子核每增加一个质子,核外便增加一个电子,电子大多按如图顺序填充。第四周期中,基态4s能级半充满的元素有________种,其中原子序数最大的基态原子的外围电子排布式为________。
 图一
图一
图二中,每条折线代表周期表中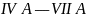 某一族元素简单氢化物的沸点变化,其他三条折线与x所在折线变化趋势不完全相同的原因为________;与x点对应的简单氢化物互为等电子体的离子为________写一种。
某一族元素简单氢化物的沸点变化,其他三条折线与x所在折线变化趋势不完全相同的原因为________;与x点对应的简单氢化物互为等电子体的离子为________写一种。
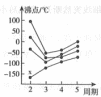 图二
图二
图三为卟啉配合物叶绿素的结构示意图,1号N原子和3号N原子与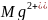 形成的化学键类型为________;5号C原子和6号C原子的杂化方式分别为________、________;该分子中所含非金属元素的电负性由小到大的顺序为________。
形成的化学键类型为________;5号C原子和6号C原子的杂化方式分别为________、________;该分子中所含非金属元素的电负性由小到大的顺序为________。
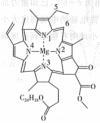 图三
图三
从石墨晶体结构示意图中截取石墨的晶胞如图四所示,设阿伏加德罗常数为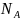 ,已知
,已知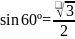 ,石墨晶体的密度为________
,石墨晶体的密度为________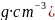 列出计算式。
列出计算式。
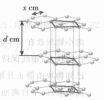 图四
图四
化学 选修3:物质结构与性质
选修3:物质结构与性质
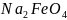 、
、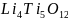 和
和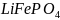 均可用作电极材料。请回答下列问题:
均可用作电极材料。请回答下列问题:
基态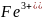 的价层电子轨道表达式为________________;同周期元素中,基态原子的未成对电子数与基态
的价层电子轨道表达式为________________;同周期元素中,基态原子的未成对电子数与基态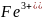 相同的元素为________。
相同的元素为________。
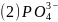 的空间构型为________________,其中P原子的杂化方式为________;写出一种与互为等电子体且中心原子与P不同主族的阴离子:________填离子符号。
的空间构型为________________,其中P原子的杂化方式为________;写出一种与互为等电子体且中心原子与P不同主族的阴离子:________填离子符号。
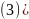 为紫色晶体,其中1mol阳离子中所含
为紫色晶体,其中1mol阳离子中所含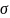 键的数目为________;配位键中提供孤电子对的原子为________填元素符号。
键的数目为________;配位键中提供孤电子对的原子为________填元素符号。
已知物质间的转化关系如图甲所示,其中a、c均大于0。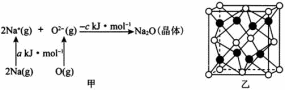
基态Na原子的第一电离能可表示为________。
相同条件下,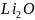 的晶格能________填“”“”或“”
的晶格能________填“”“”或“”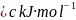 ,原因为________________________________________________________________________。
,原因为________________________________________________________________________。
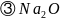 的立方晶胞结构如图乙所示。若紧邻的两个之间的距离为dpm,阿伏加德罗常数的值为
的立方晶胞结构如图乙所示。若紧邻的两个之间的距离为dpm,阿伏加德罗常数的值为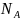 ,晶体的密度为
,晶体的密度为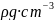 ,则Na的摩尔质量可表示为________________
,则Na的摩尔质量可表示为________________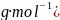 用含有d、、
用含有d、、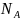 的代数式表示。
的代数式表示。
据报道,某科研团队成功合成了钛掺杂、镧镍锂氧化物包覆的“双重修饰”富镍三元正极材料。请回答下列问题:
基态钛原子的外围电子排布图为____________。
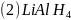 是一种还原剂,可将羧酸直接还原为醇:
是一种还原剂,可将羧酸直接还原为醇: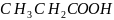
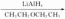
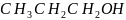 。
。
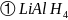 中存在的作用力类型有_____填字母。
中存在的作用力类型有_____填字母。
离子键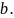 配位键
配位键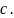 氢键
氢键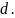 非极性键
非极性键
乙醚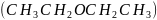 、乙醇的沸点分别为
、乙醇的沸点分别为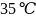 、
、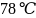 ,导致二者沸点差异的主要原因是___________________________。
,导致二者沸点差异的主要原因是___________________________。
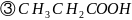 分子中C原子的杂化方式为_______;所含
分子中C原子的杂化方式为_______;所含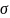 键和键的数目之比为_____;键角____填“”“”或“”
键和键的数目之比为_____;键角____填“”“”或“”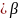 。
。
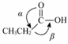
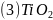 的晶胞结构如图甲所示,其中白球代表__填“Ti”或“O”,黑球的配位数为____。
的晶胞结构如图甲所示,其中白球代表__填“Ti”或“O”,黑球的配位数为____。
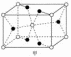
氧化镍的立方晶胞结构如图乙所示。已知氧化镍晶体的密度为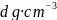 ,
, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。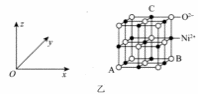
坐标参数表示原子在晶体中的相对位置。已知A、B的坐标参数分别为0,、1,,则C的坐标参数为_________。
晶胞面心上的6个氧离子构成正八面体形,镍离子位于体心,该正八面体的边长为_____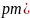 用含有d、
用含有d、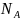 的代数式表示。
的代数式表示。
第四周期某些过渡元素在工业生产中有着极其重要的作用
铬是最硬的金属单质,被称为“不锈钢的添加剂” 写出Cr在周期表中的位置________;其原子核外电子排布的最高能层符号________
写出Cr在周期表中的位置________;其原子核外电子排布的最高能层符号________
在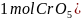 其中Cr为价中,含有过氧键的数目为________
其中Cr为价中,含有过氧键的数目为________
题目解答
答案
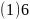 ;
; ;平面三角形;
;平面三角形;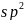 ;碳酸盐分解实际过程是晶体中阳离子结合碳酸根离子中氧离子,使碳酸根离子分解为二氧化碳的过程,阳离子所带电荷相同时,阳离子半径越小,其结合氧离子能力越强,对应的碳酸盐就越容易分解;
;碳酸盐分解实际过程是晶体中阳离子结合碳酸根离子中氧离子,使碳酸根离子分解为二氧化碳的过程,阳离子所带电荷相同时,阳离子半径越小,其结合氧离子能力越强,对应的碳酸盐就越容易分解;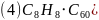 或
或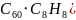 ;
;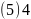 ;
;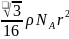 ;
;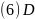 。
。【解析】【分析】本题是对物质结构与性质的考查,涉及核外电子排布、微粒结构与性质、晶胞结构与计算等,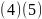 为易错点、难点,需要学生具备一定的数学计算能力和一定的空间想象。【解答】碳原子核外有6个电子,核外电子排布式为
为易错点、难点,需要学生具备一定的数学计算能力和一定的空间想象。【解答】碳原子核外有6个电子,核外电子排布式为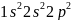 ,有1s、2s、
,有1s、2s、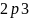 个能级,故核外有6种空间运动状态的电子,碳原子价电子排布式为
个能级,故核外有6种空间运动状态的电子,碳原子价电子排布式为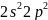 ,根据泡利原理与洪特规则,价电子排布图为
,根据泡利原理与洪特规则,价电子排布图为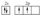 ;故答案为:6;
;故答案为:6;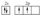 ;光气的分子式为
;光气的分子式为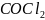 ,其分子中C原子形成3个
,其分子中C原子形成3个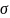 键,没有孤对电子,空间结构为平面三角形,杂化轨道数目为3,C原子采取
键,没有孤对电子,空间结构为平面三角形,杂化轨道数目为3,C原子采取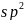 杂化;故答案为:平面三角形;
杂化;故答案为:平面三角形;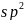 ;碳酸盐分解实际过程是晶体中阳离子结合碳酸根离子中氧离子,使碳酸根离子分解为二氧化碳的过程,阳离子所带电荷相同时,阳离子半径越小,其结合氧离子能力越强,对应的碳酸盐就越容易分解;故答案为:碳酸盐分解实际过程是晶体中阳离子结合碳酸根离子中氧离子,使碳酸根离子分解为二氧化碳的过程,阳离子所带电荷相同时,阳离子半径越小,其结合氧离子能力越强,对应的碳酸盐就越容易分解;晶体结构中
;碳酸盐分解实际过程是晶体中阳离子结合碳酸根离子中氧离子,使碳酸根离子分解为二氧化碳的过程,阳离子所带电荷相同时,阳离子半径越小,其结合氧离子能力越强,对应的碳酸盐就越容易分解;故答案为:碳酸盐分解实际过程是晶体中阳离子结合碳酸根离子中氧离子,使碳酸根离子分解为二氧化碳的过程,阳离子所带电荷相同时,阳离子半径越小,其结合氧离子能力越强,对应的碳酸盐就越容易分解;晶体结构中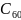 处于顶点与面心,立方烷分子填充在原
处于顶点与面心,立方烷分子填充在原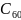 晶体分子的八面体空隙中,则立方烷处于晶体结构单元的体心和棱心位置,结构单元中有
晶体分子的八面体空隙中,则立方烷处于晶体结构单元的体心和棱心位置,结构单元中有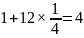 分子
分子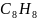 ,结构单元中
,结构单元中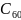 数目为
数目为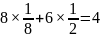 ,则化学式为
,则化学式为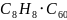 或
或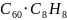 ;故答案为:
;故答案为: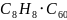 或
或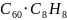 ;由图可知石墨的晶胞结构为
;由图可知石墨的晶胞结构为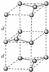 ,设晶胞的底边长为acm,晶胞的高为
,设晶胞的底边长为acm,晶胞的高为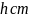 ,层间距为dcm,则
,层间距为dcm,则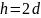 ,底面图为
,底面图为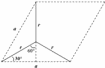 ,则
,则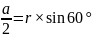 ,可得
,可得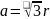 ,则底面面积为,晶胞中C原子数目为
,则底面面积为,晶胞中C原子数目为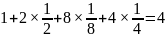 ,晶胞质量为
,晶胞质量为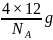 ,则:
,则: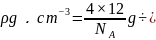 ,整理可得
,整理可得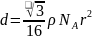 ;故答案为:4;
;故答案为:4;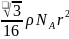 ;
;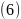 体对角线上的原子投影重合,投影在正六边形中心,另外6个顶点原子投影形成正六边形,面心上6个C原子投影也形成小的正六边形,图形D符合。故答案为:D。2.【答案】
体对角线上的原子投影重合,投影在正六边形中心,另外6个顶点原子投影形成正六边形,面心上6个C原子投影也形成小的正六边形,图形D符合。故答案为:D。2.【答案】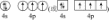 ;纺锤形或哑铃形;平面三角形;
;纺锤形或哑铃形;平面三角形;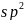 ;
; 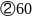 ;
;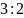 ;二十;原子;
;二十;原子;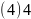 ;
;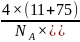 .
.
【解析】【分析】本题考查核外电子排布,杂化方式、空间构型以及晶胞的相关知识,试题具有一定的综合性,有利于考查学生分析问题和解决问题的能力,试题难度一般。【解答】砷的价电子数为5,位于周期表的第四周期,因此其价电子排布图为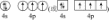 ,基态B原子核外电子占据最高能级为2p能级,因此电子云轮廓图为纺锤形或哑铃形,故答案为:
,基态B原子核外电子占据最高能级为2p能级,因此电子云轮廓图为纺锤形或哑铃形,故答案为: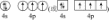 ;纺锤形或哑铃形;
;纺锤形或哑铃形;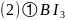 中硼原子形成的价电子对数为3,因此B原子的采取
中硼原子形成的价电子对数为3,因此B原子的采取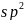 杂化,其空间构型为平面三角形,故答案为:平面三角形;
杂化,其空间构型为平面三角形,故答案为:平面三角形;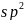 ;根据
;根据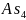 分子的空间结构分析可知其键角为60度,分子中成键电子对为6对,孤电子对为4对,二者的数目之比为
分子的空间结构分析可知其键角为60度,分子中成键电子对为6对,孤电子对为4对,二者的数目之比为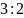 ,故答案为:60;
,故答案为:60;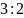 ;根据
;根据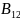 的结构分析可知每个面上平均有五分之三个B原子,因此其面数为
的结构分析可知每个面上平均有五分之三个B原子,因此其面数为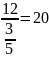 ,根据单质硼的熔点为
,根据单质硼的熔点为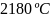 可知该晶体为原子晶体,故答案为:二十;原子;根据砷化硼的晶胞结构分析可知As原子的配位数为4,根据晶胞结构分析可知每个晶胞中含有4个B原子和4个As原子,因此晶胞的密度为
可知该晶体为原子晶体,故答案为:二十;原子;根据砷化硼的晶胞结构分析可知As原子的配位数为4,根据晶胞结构分析可知每个晶胞中含有4个B原子和4个As原子,因此晶胞的密度为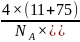 ,故答案为:4;
,故答案为:4;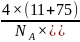 。3.【答案】
。3.【答案】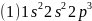 ;ⅥB;
;ⅥB;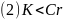 ;
;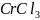 是分子晶体,
是分子晶体,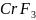 是离子晶体;
是离子晶体;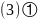 正四面体;
正四面体;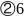 ;配位;
;配位;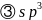 ;
;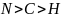 ;
;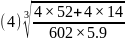 。
。
【解析】【分析】本题考查物质结构和性质,涉及了核外电子排布式、晶体类型、杂化轨道理论、配合物理论和晶胞的计算等,这些知识点都是学习重点、高考热点,难点是确定配晶体计算,应注意晶体中所含微粒数目。【解答】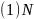 原子为7号元素,基态N原子的核外电子排布式为
原子为7号元素,基态N原子的核外电子排布式为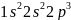 ;铬的原子序数为24,位于周期表第4周期ⅥB族;故答案为:
;铬的原子序数为24,位于周期表第4周期ⅥB族;故答案为: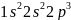 ;ⅥB;同一周期元素,第一电力能从左往右呈增大趋势,所以Cr与K两种元素原子第一电离能的大小关系为
;ⅥB;同一周期元素,第一电力能从左往右呈增大趋势,所以Cr与K两种元素原子第一电离能的大小关系为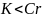 ;
;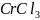 是分子晶体,
是分子晶体,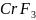 是离子晶体,所以两者的熔点相差较大,;故答案为:
是离子晶体,所以两者的熔点相差较大,;故答案为: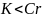 ;
;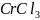 是分子晶体,
是分子晶体,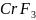 是离子晶体;
是离子晶体;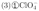 的中心原子Cl原子的电子对数
的中心原子Cl原子的电子对数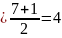 ,孤电子对数为0,所以阴离子
,孤电子对数为0,所以阴离子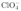 的空间构型为正四面体形;由图可知,配离子中,中心离子
的空间构型为正四面体形;由图可知,配离子中,中心离子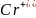 的配位数为6;N与中心原子形成的化学键称为配位键;故答案为:6;配位;配体
的配位数为6;N与中心原子形成的化学键称为配位键;故答案为:6;配位;配体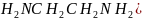 乙二胺中碳原子的杂化方式是
乙二胺中碳原子的杂化方式是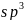 ;因为N原子的2p轨道处于半充满的状态,故分子中C、H、N、三种元素电负性从大到小的顺序为
;因为N原子的2p轨道处于半充满的状态,故分子中C、H、N、三种元素电负性从大到小的顺序为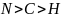 ;故答案为:
;故答案为: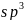 ;
;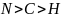 ;该晶胞中N原子的个数为:
;该晶胞中N原子的个数为: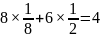 ,Cr原子的个数为:
,Cr原子的个数为: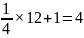 ;该晶胞的质量
;该晶胞的质量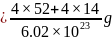 ,该晶胞的体积
,该晶胞的体积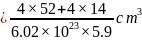 ,则氮化铬的晶胞边长
,则氮化铬的晶胞边长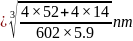 ;故答案为:
;故答案为: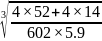 。4.【答案】
。4.【答案】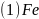 ;
;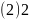 、4;
、4;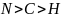 ;
;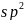 、
、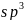 ;分子晶体;5;
;分子晶体;5;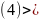 ;
;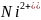 、的电荷相同,
、的电荷相同,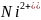 的离子半径小于的离子半径,故晶格能:
的离子半径小于的离子半径,故晶格能: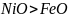 ,所以熔点
,所以熔点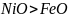 ;
;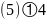 ;
;
【解析】【分析】本题是对物质与性质的考查,涉及核外电子排布、配合物、电负性、杂化轨道、分子性质、晶格能、熔点高低比较、晶胞计算等,是对物质结构主干知识的综合考查,需要学生具备扎实的基础,掌握均摊法进行晶胞的有关计算。【解答】铁、钴、镍的基态原子的价电子排布式分别为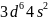 、
、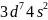 、
、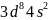 ,三种元素原子的核外未成对电子数分别为4、3、2,未成对电子数最多的是Fe;故答案为:Fe;有孤对电子的N原子与Co通过配位键结合,形成配位键后形成4对共用电子对,形成3对共用电子对的N原子形成普通的共价键,1号、3号N原子形成3对共用电子对,为普通共价键,2号、4号N原子形成4对共用电子对,与Co通过配位键结合;酞菁钴中三种非金属原子为C、N、H,同周期自左而右电负性增大,非金属性越强电负性越大,故电负性
,三种元素原子的核外未成对电子数分别为4、3、2,未成对电子数最多的是Fe;故答案为:Fe;有孤对电子的N原子与Co通过配位键结合,形成配位键后形成4对共用电子对,形成3对共用电子对的N原子形成普通的共价键,1号、3号N原子形成3对共用电子对,为普通共价键,2号、4号N原子形成4对共用电子对,与Co通过配位键结合;酞菁钴中三种非金属原子为C、N、H,同周期自左而右电负性增大,非金属性越强电负性越大,故电负性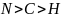 ;分子中N原子有形成3个
;分子中N原子有形成3个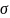 键,含有1对孤对电子,有形成4个
键,含有1对孤对电子,有形成4个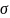 键,没有孤对电子,杂化轨道数目为4,N原子的杂化轨道类型为
键,没有孤对电子,杂化轨道数目为4,N原子的杂化轨道类型为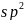 、
、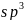 ;故答案为:2、4;
;故答案为:2、4;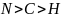 ;
;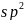 、
、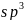 ;配合物的熔沸点比较低,易溶于非极性溶剂,应属于分子晶体;Fe原子价电子数为8,CO提供一对孤对电子,与Fe原子形成配位键,则
;配合物的熔沸点比较低,易溶于非极性溶剂,应属于分子晶体;Fe原子价电子数为8,CO提供一对孤对电子,与Fe原子形成配位键,则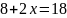 ,解得;故答案为:分子晶体;5;
,解得;故答案为:分子晶体;5;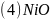 、FeO的晶体结构类型均与氯化钠的相同,说明二者都是离子晶体,
、FeO的晶体结构类型均与氯化钠的相同,说明二者都是离子晶体,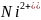 、的电荷相同,
、的电荷相同,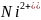 的离子半径小于的离子半径,故晶格能:
的离子半径小于的离子半径,故晶格能: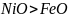 ,所以熔点
,所以熔点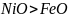 ;故答案为:;
;故答案为:;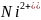 、的电荷相同,
、的电荷相同,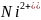 的离子半径小于的离子半径,故晶格能:
的离子半径小于的离子半径,故晶格能: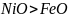 ,所以熔点
,所以熔点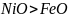 ;晶胞中As原子数目为4,Ni原子数目
;晶胞中As原子数目为4,Ni原子数目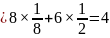 ,二者为1:1,由晶胞结构可知As原子配位数为4,故Ni的配位数为4;故答案为:4;面心与顶点上的Ni原子距离最近,最近的
,二者为1:1,由晶胞结构可知As原子配位数为4,故Ni的配位数为4;故答案为:4;面心与顶点上的Ni原子距离最近,最近的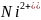 之间的距离为晶胞棱长的
之间的距离为晶胞棱长的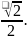 晶胞质量
晶胞质量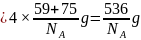 ,晶胞体积
,晶胞体积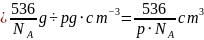 ,晶胞棱长
,晶胞棱长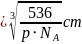 ,故最近的
,故最近的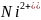 之间的距离
之间的距离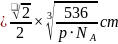 ,故答案为:
,故答案为: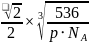 。5.【答案】
。5.【答案】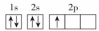
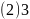 ;3
;3 平面三角形
平面三角形
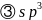
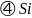
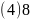
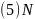 原子的半径小于As原子半径,
原子的半径小于As原子半径,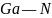 键的键长小于
键的键长小于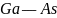 键,
键,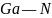 键的键能大于
键的键能大于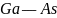 键
键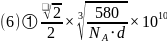
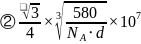
【解析】【分析】本题为物质结构题,掌握原子核外电子排布规律、杂化轨道理论、晶胞的计算是解题的关键,难度较大。【解答】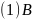 的原子序数为5,核外电子排布图为:
的原子序数为5,核外电子排布图为: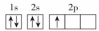 ,故答案为:
,故答案为: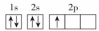 ;同周期从左到右第一电离能呈增大的趋势,但ⅡA族核外原子轨道全充满,ⅤA族元素p轨道半充满,第一电离能比相邻元素大,同周期元素中第一电离能处于B和N之间有Be、C、O三种元素,同周期从左到右,元素的电负性逐渐增大,第二周期电负性最大的元素为F,占据1s、2s、2p3个能级,故答案为:3;3;由图示可知B与3个O氧原子相连,采取
;同周期从左到右第一电离能呈增大的趋势,但ⅡA族核外原子轨道全充满,ⅤA族元素p轨道半充满,第一电离能比相邻元素大,同周期元素中第一电离能处于B和N之间有Be、C、O三种元素,同周期从左到右,元素的电负性逐渐增大,第二周期电负性最大的元素为F,占据1s、2s、2p3个能级,故答案为:3;3;由图示可知B与3个O氧原子相连,采取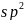 杂化,3个O原子构成平面三角形,故答案为:平面三角形;硼酸晶体中含有范德华力、氢键和
杂化,3个O原子构成平面三角形,故答案为:平面三角形;硼酸晶体中含有范德华力、氢键和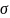 键,不含有键,故答案为:d;在
键,不含有键,故答案为:d;在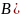 中B的杂化轨道数为4,采取
中B的杂化轨道数为4,采取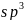 杂化,故答案为:
杂化,故答案为: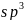 ;根据对角线规则,B与右下角的Si的性质相似,故答案为:Si;由图可知Al的配位数为8,故答案为:8;
;根据对角线规则,B与右下角的Si的性质相似,故答案为:Si;由图可知Al的配位数为8,故答案为:8;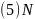 原子的半径小于As原子半径,
原子的半径小于As原子半径,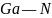 键的键长小于
键的键长小于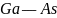 键,
键,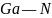 键的键能大于
键的键能大于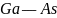 键,故GaAs的熔点低于GaN,故答案为:N原子的半径小于As原子半径,
键,故GaAs的熔点低于GaN,故答案为:N原子的半径小于As原子半径,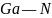 键的键长小于
键的键长小于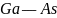 键,
键,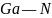 键的键能大于
键的键能大于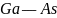 键;
键;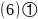 每个晶胞中含有Ga原子数为:4,As原子数:
每个晶胞中含有Ga原子数为:4,As原子数: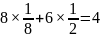 ,晶胞的质量
,晶胞的质量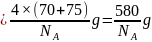 ,晶胞的边长
,晶胞的边长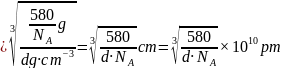 ,则6个As原子构成正八面体的边长
,则6个As原子构成正八面体的边长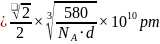 ,故答案为:
,故答案为: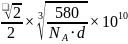 ;
;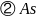 和Ga之间的最近距离
和Ga之间的最近距离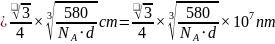 ,故答案为:
,故答案为: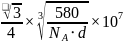 。6.【答案】
。6.【答案】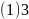 ;
;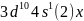 点对应的氢化物为,另外三条曲线中第二周期对应的气态氢化物分别为
点对应的氢化物为,另外三条曲线中第二周期对应的气态氢化物分别为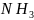 、、HF,其分子间存在氢键,导致沸点反常升高;;配位键;
、、HF,其分子间存在氢键,导致沸点反常升高;;配位键;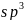
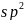 ;
;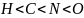 ;
;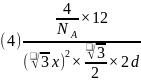 。
。
【解析】【分析】本题考查物质结构和性质,为高频考点,涉及晶胞计算、原子杂化方式判断、原子核外电子排布等知识点,侧重考查学生分析计算及空间想象能力,难点是晶胞计算,题目难度中等。【解答】第四周期中,基态4s能级半充满的元素有K、Cr、Cu,共3种元素,其中原子序数最大为Cu,其基态原子的外围电子排布式为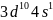 ,故答案为:3;
,故答案为:3;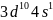 ;
;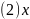 点对应的氢化物为,另外三条曲线中第二周期对应的气态氢化物分别为
点对应的氢化物为,另外三条曲线中第二周期对应的气态氢化物分别为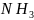 、、HF,其分子间存在氢键,导致沸点反常升高;与互为等电子体的离子为,故答案为:x点对应的氢化物为,另外三条曲线中第二周期对应的气态氢化物分别为
、、HF,其分子间存在氢键,导致沸点反常升高;与互为等电子体的离子为,故答案为:x点对应的氢化物为,另外三条曲线中第二周期对应的气态氢化物分别为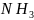 、、HF,其分子间存在氢键,导致沸点反常升高;;根据卟啉配合物叶绿素的结构示意图知,1号和3号N原子给
、、HF,其分子间存在氢键,导致沸点反常升高;;根据卟啉配合物叶绿素的结构示意图知,1号和3号N原子给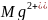 提供孤电子对形成配位键;5号C原子形成4个单键,6号C原子形成双键,其杂化方式分别为
提供孤电子对形成配位键;5号C原子形成4个单键,6号C原子形成双键,其杂化方式分别为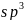 和
和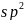 ;该分子中所含非金属元素电负性由小到大的顺序为
;该分子中所含非金属元素电负性由小到大的顺序为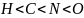 ,故答案为:配位键;
,故答案为:配位键;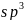
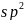 ;
;