题目
(18分)学习小组利用废银催化剂制备乙炔银(Ag2C2)-|||-和酸性乙炔银(A g2C2·nAgNO 3)。已知乙炔银和酸性-|||-乙炔银在受热时均易发生分解。-|||-(1)制取乙炔。利用如图装置-|||-制取纯净的乙炔。-|||-电石 溶液-|||-CuSO4-|||-①电石与水反应剧烈,为减缓-|||-反应速率,在不改变电石用量-|||-和大小的情况下,可采取的措施有 __-|||-__ (写两点)。-|||-②电石主要含CaC2,还含有CaS等杂质。洗气瓶中-|||-CuSO4溶液的作用是 __ o-|||-(2)制备乙炔银。向含有Ag(NH3)2OH的溶液中通入-|||-乙炔可得到乙炔银沉淀。-|||-①写出生成乙炔银的化学方程式: __(18分)学习小组利用废银催化剂制备乙炔银(Ag2C2)-|||-和酸性乙炔银(A g2C2·nAgNO 3)。已知乙炔银和酸性-|||-乙炔银在受热时均易发生分解。-|||-(1)制取乙炔。利用如图装置-|||-制取纯净的乙炔。-|||-电石 溶液-|||-CuSO4-|||-①电石与水反应剧烈,为减缓-|||-反应速率,在不改变电石用量-|||-和大小的情况下,可采取的措施有 __-|||-__ (写两点)。-|||-②电石主要含CaC2,还含有CaS等杂质。洗气瓶中-|||-CuSO4溶液的作用是 __ o-|||-(2)制备乙炔银。向含有Ag(NH3)2OH的溶液中通入-|||-乙炔可得到乙炔银沉淀。-|||-①写出生成乙炔银的化学方程式: __


题目解答
答案

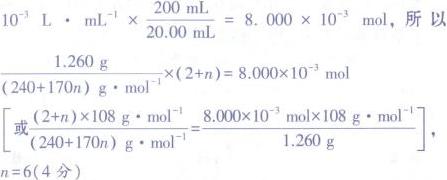
解析
- 制取乙炔:考查气体发生装置的控制反应速率方法及除杂原理。关键点在于反应物浓度和流速的控制,以及CuSO4溶液的除杂作用。
- 制备乙炔银:涉及沉淀生成反应的化学方程式书写及实验步骤补充。需注意氨水调节pH的作用及乙炔的通入条件。
- 酸性乙炔银的制备与组成测定:考查沉淀洗涤的检验方法及滴定法计算。需掌握pH试纸的使用判断洗净及滴定终点现象与计算逻辑。
(1) 制取乙炔
① 减缓反应速率的措施
- 使用饱和食盐水代替水:降低反应物浓度,减缓反应速率。
- 减缓分液漏斗液体滴加速度:控制水的滴加速度,减少反应物接触。
② 洗气瓶中CuSO4溶液的作用
- 除去H2S气体:电石中的CaS与水反应生成H2S,CuSO4与H2S反应生成CuS沉淀,起到除杂作用。
(2) 制备乙炔银
① 生成乙炔银的化学方程式
反应中乙炔与Ag(NH3)2OH反应生成Ag2C2和NH3:
$C_2H_2 + 2Ag(NH_3)_2OH + 2H_2O \rightarrow Ag_2C_2 \downarrow + 4NH_3 \cdot H_2O$
② 实验方案补充
- 加入氨水:使过量的Ag+形成可溶的$[Ag(NH_3)_2]^+$。
- 通入乙炔:至不再生成沉淀,确保Ag2C2完全析出。
- 过滤与洗涤:用去离子水洗涤,去除杂质。
(3) 酸性乙炔银的制备与组成测定
① 洗涤干净的检验
- 实验方案:取最后一次洗涤液,用pH试纸检测。若溶液呈中性,说明无$NO_3^-$残留,沉淀洗净。
② 滴定终点现象与计算
终点现象
- 红色出现且半分钟不褪色:Fe³+被还原为Fe²+,指示反应终点。
计算n的值
-
计算Ag+的物质的量:
$n(Ag^+) = 0.05000 \, \text{mol/L} \times 0.016 \, \text{L} \times \frac{200}{20} = 0.08 \, \text{mol}$ -
建立方程:
样品质量对应总物质的量:
$\frac{1.260}{240 + 170n} \times (2 + n) = 0.08$ -
解方程:
$n = 6$