题目
在298K时有电池:Pt,H2(p)|KOH(a=1),Ag2O(s)|Ag(s).已知E(Ag2O|Ag)=0.34V△H(H2O,)=-286.0kJ·mol-1.△HS(Ag2O,s)=-30.57 k]. mol-1。试求(1)电池的电动势,已知KW=1.0×10-14(2)电池反应的△Gm,△Hm,△Sm,Q和(3)若电池在短路下放电,程度与可逆反应相同时,则热效应为多少?
在298K时有电池:Pt,H2(p)|KOH(a=1),Ag2O(s)|Ag(s).已知E(Ag2O|Ag)=0.34V
△H(H2O,)=-286.0kJ·mol-1.△HS(Ag2O,s)=-30.57 k]. mol-1。试求
(1)电池的电动势,已知KW=1.0×10-14
(2)电池反应的△Gm,△Hm,△Sm,Q
和
(3)若电池在短路下放电,程度与可逆反应相同时,则热效应为多少?
题目解答
答案
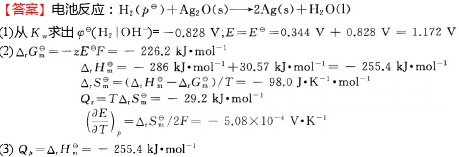
解析
步骤 1:确定电池反应
电池反应为:${H}_{2}({P}^{\theta })+{Ag}_{2}O(s)\rightarrow 2Ag(s)+{H}_{2}O(l)$
步骤 2:计算电池的电动势
已知 $E(Ag_{2}O|Ag)=0.34V$,$K_{W}=1.0\times 10^{-14}$,则 $\varphi =({H}_{2}|{OH}^{-})=-0.828V$,因此电池的电动势 $E=E'=0.344V+0.828V=1.172V$。
步骤 3:计算电池反应的 $\Delta G_{m}^{\theta }$,$\Delta H_{m}^{\theta }$,$\Delta S_{m}^{\theta }$ 和 $Q$
$\Delta G_{m}^{\theta }=-z{E}^{\theta }F=-226.2kJ\cdot {mol}^{-1}$,$\Delta H_{m}^{\theta }=-286.0kJ\cdot {mol}^{-1}+30.57kJ\cdot {mol}^{-1}=-255.4kJ\cdot {mol}^{-1}$,$\Delta S_{m}^{\theta }=\frac{\Delta H_{m}^{\theta }-\Delta G_{m}^{\theta }}{T}=-98.0J\cdot K^{-1}\cdot mol^{-1}$,$Q_{1}=T\Delta S_{m}^{\theta }=-29.2kJ\cdot {mol}^{-1}$。
步骤 4:计算电池在短路下放电的热效应
$Q_{n}=\Delta H_{m}^{\theta }=-255.4kJ\cdot {mol}^{-1}$。
电池反应为:${H}_{2}({P}^{\theta })+{Ag}_{2}O(s)\rightarrow 2Ag(s)+{H}_{2}O(l)$
步骤 2:计算电池的电动势
已知 $E(Ag_{2}O|Ag)=0.34V$,$K_{W}=1.0\times 10^{-14}$,则 $\varphi =({H}_{2}|{OH}^{-})=-0.828V$,因此电池的电动势 $E=E'=0.344V+0.828V=1.172V$。
步骤 3:计算电池反应的 $\Delta G_{m}^{\theta }$,$\Delta H_{m}^{\theta }$,$\Delta S_{m}^{\theta }$ 和 $Q$
$\Delta G_{m}^{\theta }=-z{E}^{\theta }F=-226.2kJ\cdot {mol}^{-1}$,$\Delta H_{m}^{\theta }=-286.0kJ\cdot {mol}^{-1}+30.57kJ\cdot {mol}^{-1}=-255.4kJ\cdot {mol}^{-1}$,$\Delta S_{m}^{\theta }=\frac{\Delta H_{m}^{\theta }-\Delta G_{m}^{\theta }}{T}=-98.0J\cdot K^{-1}\cdot mol^{-1}$,$Q_{1}=T\Delta S_{m}^{\theta }=-29.2kJ\cdot {mol}^{-1}$。
步骤 4:计算电池在短路下放电的热效应
$Q_{n}=\Delta H_{m}^{\theta }=-255.4kJ\cdot {mol}^{-1}$。