用原子吸收光谱确定物质中含有哪些金属元素。1.判断正误(正确的打“√”,错误的打“×”)(1)检验自来水中的氯离子时,可先用稀盐酸酸化,再加AgNO3溶液 (×)(2)加入硝酸酸化的Ba(NO3)2溶液检验某未知溶液中是否含有SO (×)(3)氯化钠在火焰上灼烧时使火焰呈黄色,是因为氯化钠发生了分解反应 (×)(4)如透过蓝色的钴玻璃能够观察到紫色火焰,则肯定有K元素,可能有Na元素 (√)2.对于某些离子的检验及结论一定正确的是( )A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有COB.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SOC.加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NHD.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+C [A项有可能是碳酸氢根离子,B项有可能形成氯化银,D项有可能形成碳酸钙。]3.做焰色反应实验用的铂丝,每实验一种样品后都必须( )A.用水洗涤2~3次后再使用B.用盐酸洗涤后,经蒸馏水冲洗,方可使用C.用滤纸擦干后才可使用D.用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用D [要保证铂丝纯净,需要用稀盐酸清洗。]物质检验的要求与步骤1.物质的检验——根据其目的和要求的不同,通常可分为:鉴定、鉴别和推断三类不同点相同点鉴定一定要根据物质的化学性质对其组成进行全面分析,对于离子化合物而言,即不仅要检出阳离子,又要检出阴离子:如鉴定某一物质是否是硫酸钾均要根据待检物质的特征反应,选用适当的试剂和方法,准确观察反应中颜色变化、沉淀的生成或溶解、气体的生成、焰色等现象加以判定鉴别对两种或两种以上物质进行区别的过程推断通过已知实验事实,根据物质的性质进行分析、推理,确认被检验是什么物质或什么物质可能存在,什么物质一定不存在的过程2.物质检验的基本要求(1)反应要有明显的现象,如颜色变化、沉淀的生成或溶解、气体的生成等。(2)试剂易得,用量要少;方法易行,操作简单,反应条件容易达到。(3)排除干扰物的影响:需要检验的物质中如果有干扰物存在,则需要选择试剂对干扰物进行排除;要注意多次加入不同的鉴别试剂进行检验时,应及时排除前次加入试剂可能引入的干扰物质。如检验Cl-时,CO外观观察 一观察颜色、状态、气味等-|||-判断预测-|||-根据观察、结合分类法、预测物质可能具有-|||-↓ 的性质或可能的成分-|||-实验验证 一设计实验方案,进行实验验证-|||-↓-|||-分析结论 一根据实验现象,分析结果,作出判断,得出结论(-1,3)(-1,3)(-1,3)能与Ag+结合,生成沉淀,故应加稀硝酸除去,来排除CO外观观察 一观察颜色、状态、气味等-|||-判断预测-|||-根据观察、结合分类法、预测物质可能具有-|||-↓ 的性质或可能的成分-|||-实验验证 一设计实验方案,进行实验验证-|||-↓-|||-分析结论 一根据实验现象,分析结果,作出判断,得出结论(-1,3)(-1,3)(-1,3)的干扰;检验SO时,CO、SO均能与Ba2+结合生成白色沉淀,故先加入稀盐酸排除上述两种离子存在的可能,但不能加入稀硝酸,因硝酸能将SO外观观察 一观察颜色、状态、气味等-|||-判断预测-|||-根据观察、结合分类法、预测物质可能具有-|||-↓ 的性质或可能的成分-|||-实验验证 一设计实验方案,进行实验验证-|||-↓-|||-分析结论 一根据实验现象,分析结果,作出判断,得出结论(-1,3)(-1,3)(-1,3)氧化成SO。3.物质检验的基本步骤外观观察 一观察颜色、状态、气味等-|||-判断预测-|||-根据观察、结合分类法、预测物质可能具有-|||-↓ 的性质或可能的成分-|||-实验验证 一设计实验方案,进行实验验证-|||-↓-|||-分析结论 一根据实验现象,分析结果,作出判断,得出结论(-1,3)(-1,3)(-1,3)外观观察 一观察颜色、状态、气味等-|||-判断预测-|||-根据观察、结合分类法、预测物质可能具有-|||-↓ 的性质或可能的成分-|||-实验验证 一设计实验方案,进行实验验证-|||-↓-|||-分析结论 一根据实验现象,分析结果,作出判断,得出结论(-1,3)(-1,3)(-1,3) 某溶液中含有MgSO4和Na2SO4两种溶质,选择适当试剂将溶液中的镁离子转化为沉淀或固体分离出来,设计实验流程如下: 下列关于物质分类的说法正确的是( )A.SO2和CO2都能和碱溶液反应,均属于酸性氧化物B.醋酸、纯碱和生石灰分别属于酸、碱、氧化物C.盐酸属于混合物,而液氯、浓硫酸均属于纯净物D.酸性氧化物一定是非金属氧化物A [SO2和CO2都能和碱反应生成盐和水,为酸性氧化物, A正确;纯碱是碳酸钠,属于盐, B错误;浓硫酸是硫酸的水溶液,属于混合物, C错误;酸性氧化物不一定都是非金属氧化物,如Mn2O7就属于酸性氧化物, D错误。]1.下列十种物质:①水 ②空气 ③铁 ④二氧化碳⑤硫酸 ⑥熟石灰 ⑦胆矾(CuSO4·5H2O) ⑧FeCl3溶液 ⑨碱式碳酸铜[Cu2(OH)2CO3] ⑩碳酸氢钠其中属于混合物的是________(填序号,下同);属于氧化物的是________;属于碱的是________;属于酸的是________;属于盐的是________。
用原子吸收光谱确定物质中含有哪些金属元素。
1.判断正误(正确的打“√”,错误的打“×”)
(1)检验自来水中的氯离子时,可先用稀盐酸酸化,再加AgNO3溶液 (×)
(2)加入硝酸酸化的Ba(NO3)2溶液检验某未知溶液中是否含有SO (×)
(3)氯化钠在火焰上灼烧时使火焰呈黄色,是因为氯化钠发生了分解反应 (×)
(4)如透过蓝色的钴玻璃能够观察到紫色火焰,则肯定有K元素,可能有Na元素 (√)
2.对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
C.加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
C [A项有可能是碳酸氢根离子,B项有可能形成氯化银,D项有可能形成碳酸钙。]
3.做焰色反应实验用的铂丝,每实验一种样品后都必须( )
A.用水洗涤2~3次后再使用
B.用盐酸洗涤后,经蒸馏水冲洗,方可使用
C.用滤纸擦干后才可使用
D.用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用
D [要保证铂丝纯净,需要用稀盐酸清洗。]
物质检验的要求与步骤
1.物质的检验——根据其目的和要求的不同,通常可分为:鉴定、鉴别和推断三类
不同点
相同点
鉴定
一定要根据物质的化学性质对其组成进行全面分析,对于离子化合物而言,即不仅要检出阳离子,又要检出阴离子:如鉴定某一物质是否是硫酸钾
均要根据待检物质的特征反应,选用适当的试剂和方法,准确观察反应中颜色变化、沉淀的生成或溶解、气体的生成、焰色等现象加以判定
鉴别
对两种或两种以上物质进行区别的过程
推断
通过已知实验事实,根据物质的性质进行分析、推理,确认被检验是什么物质或什么物质可能存在,什么物质一定不存在的过程
2.物质检验的基本要求
(1)反应要有明显的现象,如颜色变化、沉淀的生成或溶解、气体的生成等。
(2)试剂易得,用量要少;方法易行,操作简单,反应条件容易达到。
(3)排除干扰物的影响:需要检验的物质中如果有干扰物存在,则需要选择试剂对干扰物进行排除;要注意多次加入不同的鉴别试剂进行检验时,应及时排除前次加入试剂可能引入的干扰物质。
如检验Cl-时,CO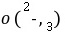 能与Ag+结合,生成沉淀,故应加稀硝酸除去,来排除CO
能与Ag+结合,生成沉淀,故应加稀硝酸除去,来排除CO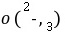 的干扰;检验SO时,CO、SO均能与Ba2+结合生成白色沉淀,故先加入稀盐酸排除上述两种离子存在的可能,但不能加入稀硝酸,因硝酸能将SO
的干扰;检验SO时,CO、SO均能与Ba2+结合生成白色沉淀,故先加入稀盐酸排除上述两种离子存在的可能,但不能加入稀硝酸,因硝酸能将SO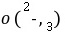 氧化成SO。
氧化成SO。
3.物质检验的基本步骤

 某溶液中含有MgSO4和Na2SO4两种溶质,选择适当试剂将溶液中的镁离子转化为沉淀或固体分离出来,设计实验流程如下:
某溶液中含有MgSO4和Na2SO4两种溶质,选择适当试剂将溶液中的镁离子转化为沉淀或固体分离出来,设计实验流程如下:
下列关于物质分类的说法正确的是( )
A.SO2和CO2都能和碱溶液反应,均属于酸性氧化物
B.醋酸、纯碱和生石灰分别属于酸、碱、氧化物
C.盐酸属于混合物,而液氯、浓硫酸均属于纯净物
D.酸性氧化物一定是非金属氧化物
A [SO2和CO2都能和碱反应生成盐和水,为酸性氧化物, A正确;纯碱是碳酸钠,属于盐, B错误;浓硫酸是硫酸的水溶液,属于混合物, C错误;酸性氧化物不一定都是非金属氧化物,如Mn2O7就属于酸性氧化物, D错误。]
1.下列十种物质:①水 ②空气 ③铁 ④二氧化碳
⑤硫酸 ⑥熟石灰 ⑦胆矾(CuSO4·5H2O) ⑧FeCl3溶液 ⑨碱式碳酸铜[Cu2(OH)2CO3] ⑩碳酸氢钠
其中属于混合物的是________(填序号,下同);属于氧化物的是________;属于碱的是________;属于酸的是________;属于盐的是________。
题目解答
答案
[答案] ②⑧ ①④ ⑥ ⑤ ⑦⑨⑩
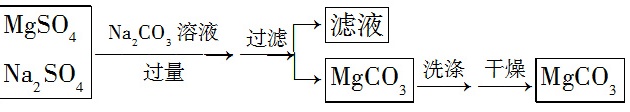
(1)欲证明滤液中存在SO、CO,选用的方案是先取少量的滤液滴加过量的________,发现有气泡生成,再向其中加入________溶液,出现白色沉淀,则可证明SO、CO均存在。
(2)如何洗涤MgCO3沉淀?______________________________
_____________________________________________________。
(3)如何检验MgCO3沉淀是否洗涤干净?__________________
_____________________________________________________。
[答案] (1)稀盐酸 BaCl2(其他答案合理也可) (2)沿玻璃棒向过滤器中注入少量蒸馏水,使水刚好浸没沉淀,让水自然流下,重复2~3次 (3)取少量最后一次洗涤液,滴加稀盐酸和BaCl2溶液,若有沉淀生成则说明没有洗净;反之,已洗涤干净(答案合理也可)
方法技巧
离子检验的方法

具体操作:一取二加三现象四结论。
草木灰中含有KCl、K2SO4和K2CO3。将草木灰溶于水,过滤,得滤液。用三支试管分别取滤液少许,第一支试管中加入________,生成无色无味、能使澄清石灰水变浑浊的气体,证明含有K2CO3;第二支试管中先加入少量________,再加入________溶液,生成白色沉淀,证明含有K2SO4;第三支试管中加入少量________溶液和________溶液,生成白色沉淀,证明含有KCl。
[答案] 稀盐酸 稀盐酸 BaCl2 AgNO3 稀HNO3(答案不唯一,合理即可)
1.检验铵盐时,可将少许待测物放入试管中,然后( )
A.加热,将湿润的红色石蕊试纸放置于试管口检验
B.加水溶解,加入酸溶液观察现象
C.加入碱溶液,加热,滴入酚酞溶液
D.加入NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口检验
D [铵盐受热分解生成氨气的同时,往往也会生成酸性气体,不利于铵盐的检验;铵盐遇酸无明显变化;铵盐与碱溶液混合后溶液呈碱性,滴入酚酞溶液变红证明溶液中有OH-,不能证明生成了氨分子;若加热,生成的氨气逸出,遇湿润的红色石蕊试纸变蓝,则可说明有氨分子生成。]
2.在未知液中加入AgNO3溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的气体生成,将气体通入澄清石灰水,石灰水变浑浊,由此判断未知液中含有( )
A.Cl-、SO B.Cl-、NO
C.Cl-、CO D.Cl-、OH-
D.Cl-、OH-
[答案] C
3.离子检验的常用方法有三种:
检验方法 | 沉淀法 | 显色法 | 气体法 |
判断的依据 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
下列离子检验的方法中不合理的是( )
A.CO——气体法 B.SO——沉淀法
C.H+——显色法 D.Cl-——气体法
D [Cl-常用AgNO3溶液和稀硝酸进行检验,即生成不溶于稀硝酸的白色沉淀,由题给信息可知,为沉淀法。]