题目
将反响H+(a1)→H+(a2)设计成电池的表示式为:___________________________________________。
将反响H+(a1)→H+(a2)设计成电池的表示式为:___________________________________________。
题目解答
答案
[答] Pt,H2(p)|H+(a2)||H+(a1)|H2(p),Pt 三、计算题
1
[答] 电池反响为:
AgCl(s)→Ag(s)+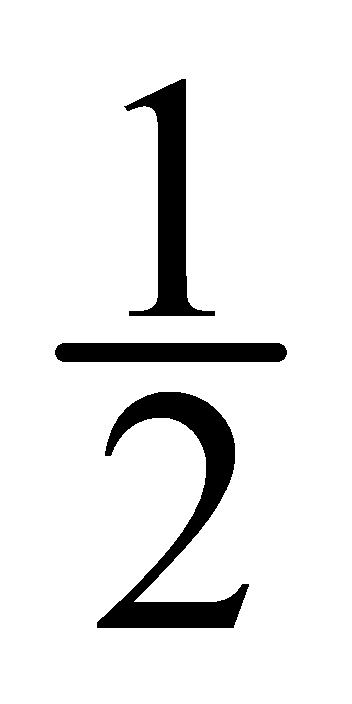 Cl2(p)
Cl2(p)
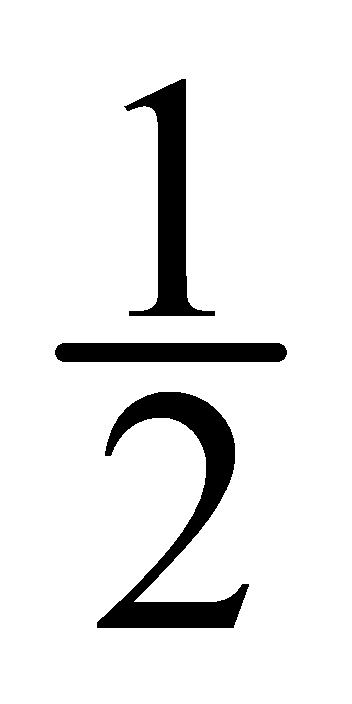 Cl2(p)
Cl2(p)得 E= - 1.105 V
⑵ Qr=TrSm×104 J
2
[答]
Ag2O(s)│Ag(s)│OH-(a)│O2p)│Pt
电池反响: 2Ag(s) + (1/2)O2p) ─→ Ag2O(s)
E = E- RT/2F×ln (1/a(O2))1/2
= f (O2,OH-) - f (Ag2×lg 1/(0.21)1/2
= 0.0470 V
E > 0 电池为自发的,说明 Ag 在 OH- 溶液中会被氧化,参加 CN-
后,f (Ag(CN),Ag) = -0.31 V < f $ (Ag2O,Ag) ,这时负极发生 Ag
氧化成Ag(CN) 的反响,而不是生成 Ag2O 的反响。
的反响,而不是生成 Ag2O 的反响。
 的反响,而不是生成 Ag2O 的反响。
的反响,而不是生成 Ag2O 的反响。解析
步骤 1:确定电池的组成
为了设计一个电池,我们需要确定电池的正极和负极。根据题目中的反应H+(a1)→H+(a2),我们可以看出这是一个涉及氢离子浓度变化的反应。因此,我们可以选择氢气作为电极反应的物质,因为氢气可以与氢离子发生氧化还原反应。
步骤 2:确定电极反应
在电池中,氢离子浓度较低的一侧(a1)作为负极,发生氧化反应,氢气被氧化成氢离子。氢离子浓度较高的一侧(a2)作为正极,发生还原反应,氢离子被还原成氢气。
步骤 3:写出电池表示式
根据上述分析,我们可以写出电池的表示式。电池的表示式通常按照负极│电解质│正极的顺序书写。因此,电池的表示式为:Pt,H2(p)|H+(a2)||H+(a1)|H2(p),Pt。其中,Pt表示铂电极,H2(p)表示氢气,H+(a1)和H+(a2)分别表示氢离子浓度较低和较高的溶液。
为了设计一个电池,我们需要确定电池的正极和负极。根据题目中的反应H+(a1)→H+(a2),我们可以看出这是一个涉及氢离子浓度变化的反应。因此,我们可以选择氢气作为电极反应的物质,因为氢气可以与氢离子发生氧化还原反应。
步骤 2:确定电极反应
在电池中,氢离子浓度较低的一侧(a1)作为负极,发生氧化反应,氢气被氧化成氢离子。氢离子浓度较高的一侧(a2)作为正极,发生还原反应,氢离子被还原成氢气。
步骤 3:写出电池表示式
根据上述分析,我们可以写出电池的表示式。电池的表示式通常按照负极│电解质│正极的顺序书写。因此,电池的表示式为:Pt,H2(p)|H+(a2)||H+(a1)|H2(p),Pt。其中,Pt表示铂电极,H2(p)表示氢气,H+(a1)和H+(a2)分别表示氢离子浓度较低和较高的溶液。